【题目】早在春秋战国时期,我国就开始生产和使用铁器.工业上炼铁的原理是利用一氧化碳和氧化铁的反应.某化学兴趣小组利用下图装置进行实验探究,请按要求填空:
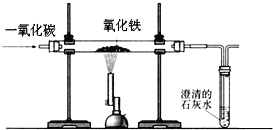
对实验进行分析并回答:
(1)给玻璃管加热的仪器叫酒精喷灯,要用其 (填“外焰”、“内焰”或“焰心”)进行加热.
(2)实验中玻璃管里氧化铁粉末的颜色变化是 ,观察到澄清石灰水的现象是 .
(3)实验前“通入CO”与“开始加热”的顺序是 ;
(4)实验要在装置末端a处燃着一盏酒精灯,其作用是 .
(5)该反应的化学方程式为 .
参考答案:
【答案】(1)外焰;
(2)红色粉末变黑色; 石灰水变浑浊;
(3)通入CO,再开始加热;
(4)除去反应剩余的CO,防止空气污染;
(5)3CO+Fe2O3![]() 2Fe+3CO2.
2Fe+3CO2.
【解析】
试题分析:(1)根据火焰的温度来分析;
(2)根据反应物和生成物,分析实验中玻璃管里氧化铁粉末的颜色变化.根据二氧化碳能与氢氧化钙反应分析澄清石灰水的现象;
(3)根据玻璃管内有空气,通入一氧化碳易发生爆炸分析;
(4)根据一氧化碳是对大气有污染的气体分析;
(5)根据炼铁的原理来分析.
解:(1)酒精喷灯外焰的温度最高,所以用外焰进行加热;故填:外焰;
(2)由于在高温下,一氧化碳将氧化铁还原为铁,同时生成了二氧化碳.所以,实验中玻璃管里氧化铁粉末的颜色变化是红色粉末变黑色;二氧化碳能与氢氧化钙反应生成了碳酸钙沉淀和水.所以,观察到澄清石灰水的现象是:石灰水变浑浊;故填:红色粉末变黑色; 石灰水变浑浊;
(3)由于玻璃管内有空气,通入一氧化碳高温时易发生爆炸.所以实验前先通入CO,排净玻璃管中的空气再开始加热.故填:通入CO,再开始加热;
(4)为了防止一氧化碳对大气的污染,所以实验时要在装置末端a处燃着一盏酒精灯除去反应剩余的CO.故填:除去反应剩余的CO,防止空气污染;
(5)一氧化碳还原氧化铁的反应原理为:3CO+Fe2O3![]() 2Fe+3CO2;故填:3CO+Fe2O3
2Fe+3CO2;故填:3CO+Fe2O3![]() 2Fe+3CO2.
2Fe+3CO2.
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是水电解实验的示意图:
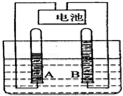
(1)由实验现象确定A端接电池 极
(2)A试管里产生的是 气;A、B两试管中气体的体积比是 ;质量比为 ;B试管里的气体可用 来检验.
(3)该反应的化学方程式是: .
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列关于水的说法正确的是( )
A.所有物质都易溶于水 B.可将工业废水任意排入内河
C.生活中常用肥皂水检验软水和硬水 D.水电解过程与电源正极连接的一端产生氢气
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列实验现象的描述中,正确的是( )
A.铁丝在氧气中燃烧,火星四射,生成黑色固体
B.硫在氧气中燃烧,发出淡蓝色火焰
C.红磷在空气中燃烧产生大量的白雾
D.木炭在氧气中燃烧,生成有刺激性气味的气体
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究.
(1)如图所示装置和药品进行实验,实验中可观察到的现象是?打开止水夹后观察到的现象是?
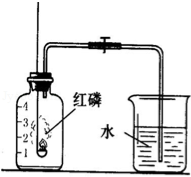
(2)根据实验现象得出的结论是?
(3)集气瓶内发生反应的符号表达式?
(4)根据实验推测剩余氮气具有的性质是?
(5)小芳同学测定空气中氧气的含量.结果却发现倒吸的水量远远不足集气瓶的
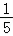 .你认为造成此现象的原因可能是 : .
.你认为造成此现象的原因可能是 : . -
科目: 来源: 题型:
查看答案和解析>>【题目】如图是实验室常用的实验仪器与装置.依据题目要求回答下列问题:
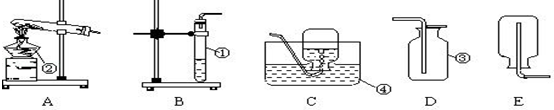
(1)写出标号仪器的名称 ① ; ② .
(2)写出用A装置制取氧气的符号表达式 ;另外选择装置A还可以用其他的药品为原料制取氧气时,甲同学还在该装置试管内的导管口处添加了一团棉花,其目的是 ;甲同学做完实验后,发现试管炸裂了,可能的原因有 (请讲出其中的一条).
(3)实验室用高锰酸钾制氧气的试验中,不需要用到的一组仪器是
A.烧杯、玻璃棒B.大试管、集气瓶C.酒精灯、铁架台D.导管、单孔塞
(4)小强同学用二氧化锰和过氧化氢反应来制取氧气,其反应的符号表达式为 ,发生装置选择 (填字母);收集装置选择 (填字母),选择该收集装置的依据是 ,收集气体后如何检验集气瓶中装的是否是氧气?
(5)小明将B与C相连,用高锰酸钾制取氧气.实验操作有:a.停止加热b.固定试管c.将导管从水槽中取出d.装药品和放棉花e.加热,收集氧气.上述过程中缺少的一步操作是 .
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是电解水中水分子分解过程示意图,
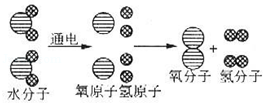
(1)反应前有 种分子,属于 物(纯净物、混合物)
(2)由该反应知:化学变化中 可分 不可再分;同时说明化学变化的实质是
(3)请写出该反应的符号表达式: .
相关试题

