
【题目】某化学兴趣小组的同学在探究Mg、Cu、Fe三种金属的有关性质时进行了如下实验:
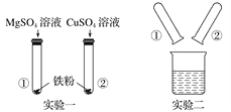
(1)实验一:发生反应的化学方程式________________________________________________,该实验可得出三种金属的活动性由强到弱的顺序为______________________。
(2)实验二:将实验一后①、②试管内的物质倒入烧杯中,发现烧杯内的红色固体明显增多,一段时间后过滤。滤渣中一定含有的物质是________________,可能含有的物质是________________,为了进一步确定可能有的物质是否存在,同学们设计了如下方案:
实验步骤 | 实验现象 | 结论 |
取少量滤渣于试管中,向其中滴加_______________ | 没有气泡产生 | ________ |
滤液中含有的金属离子可能是____________。
①Mg2+ ②Mg2+、Fe2+ ③Mg2+、Fe3+ ④Cu2+、Fe2+ ⑤Mg2+、Fe2+、Cu2+
【答案】(1)Fe + CuSO4="=" FeSO4+ Cu ; Mg Fe Cu
(2)Cu ; Fe
实验步骤 | 实验现象 | 结论 |
取少量滤渣于试管中,向其中滴加HCl(H2SO4) | 没有气泡产生 | 滤渣中没有铁 |
②⑤
【解析】
(1)铁粉与硫酸镁溶液不反应说明金属活动性镁>铁,铁粉与硫酸铜溶液反应,说明金属活动性铁>铜,故三种金属的活动性由强到弱的顺序为镁>铁>铜.(2)②试管内发生反应生成了铜,由于烧杯内的红色固体明显增多,说明②试管内硫酸铜有剩余,在烧杯内铁与硫酸铜也发生了反应,但反应后铁不一定有剩余.因此,滤渣中一定含有铜,可能含有铁.证明铁存在的化学方法是向滤渣中滴加盐酸或稀硫酸,没有气泡产生,说明滤渣中不含铁.滤液中一定含有生成的亚铁离子和没反应的镁离子,可能含铜离子.


科目:初中化学 来源: 题型:
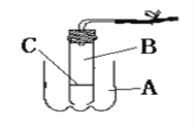
【题目】实验室用下图装置来制取氧气,请按要求填写;
(1)写出图中有标号的仪器的名称
①_______②_______③_____________④_____________

(2)用带导管的橡皮塞塞住试管口,把导管的一端浸在水里,两手紧贴其外壁,此项操作的目的是__________________________________________。
(3)若用高锰酸钾来制取氧气时,则要将一团棉花放在试管口的地方,此项操作的目的是___________________________________________。
(4)只有加热到气泡连续地并比较均匀地放出时,才能收集氧气,原因是_____________________________ 。
(5)收集完毕氧气后,先要___________,然后再__________________。
(6)如果用向上排空气法收集时,如何证明该瓶内的氧气已满:___________________________;
(7)实验室高锰酸钾制氧气应选用的发生装置是_____,收集装置_________。
(8)实验室用双氧水制取并且收集得较纯氧气时应选用的发生装置是______,收集装置为________。用化学式表示化学反应式__________________________.
(9)实验室用氯化铵与熟石灰两种固体加热制取氨气,氨气的密度比空气小,极易溶于水。推断:实验室制取氨气应选用的发生装置为_____,收集装置为____。
(10)利用废弃的可乐瓶和底部有小孔的试管组成制取氧气的装置,该装置A应盛放__________,B处应放进____________,C是用带小孔的塑料片。放置C以后使该装置具有_________________________________________________优点。若使正在发生的反应停止,可以通过操作____________来实现,可看到的现象是_______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验设计不能达到其对应实验目的的是( )
选项 | 实验 | 现象 | 结论 |
A |
| 铁片表面有少量气泡,锌丝表面有较多气泡 | 说明铁与锌的活泼性 Fe<Zn |
B |
| 硫磺在空气中燃烧发出微弱的淡蓝色火焰,在氧气中发出明亮的蓝紫色火焰 | 说明硫磺在氧气中燃烧更旺盛 |
C |
| ①试管中没有明显现象 ②试管中铁钉生锈 | 说明铁生锈需要水 |
D |
| 试管中白磷燃烧,热水中白磷不燃烧 | 说明燃烧需要氧气 |
A. AB. BC. CD. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文。
表面地球有2/3以上都是海洋,海水为弱碱性,海洋表层水的pH约为8.2。海洋能够吸收大量空气中的二氧化碳,使地球大气层中的二氧化碳浓度降低,从而降低了地球的温室效应。
人类活动排放的二氧化碳有30%~40%会溶解于海洋等水体中。溶解的二氧化碳中的一部分会与水反应生成碳酸,导致海水的pH逐渐降低,这种现象被称为海洋酸化。
海洋酸化是对海洋生物多样性的一种威胁。在2.5亿多年前,地球经历了一次最引人注目的灭绝事件,大约90%的海洋生物和70%的陆地生物绝迹了。科学家认为,空气中二氧化碳含量的上升引起的海洋酸化,可能在古代生物灭绝事件中起到了至关重要的作用。尤其是长有坚硬外壳(主要成分是碳酸钙)的生物,如珊瑚和软体动物等,在海洋酸化的情况下,会出现外壳溶解现象而难易生存。
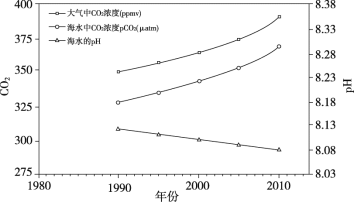
由于吸收了过多的二氧化碳,海洋正以前所未有的速度酸化。图中显示1990-2010年间某海域中二氧化碳浓度及海水pH的变化趋势。
海洋酸化正在改变海洋生物赖以生存的化学环境,从而影响海洋生物的生存,导致整个海洋生物群落的发展不稳定,最终海洋将面临巨大的灾难。
依据文章内容,回答下列问题:
(1)海水中溶解的二氧化碳与水反应的化学方程式为________。
(2)珊瑚和软体动物难以在酸性条件下生存的主要原因是________。
(3)下列说法正确的是________(填字母序号)。
A 燃烧化石燃料会使空气中CO2含量上升
B 海洋吸收CO2,降低了地球的温室效应
C 海洋酸化可能在古代生物灭绝事件中起到至关重要的作用
(4)结合图中信息,解释海洋不断酸化的原因_________。
(5)写出一条解决海洋酸化问题的有效方法_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
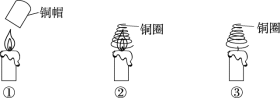
【题目】实验小组同学验证可燃物燃烧的条件,进行如下实验。
编号 | 实验操作 | 实验现象 |
① | 铜帽加热后,立即罩在蜡烛火焰上 | 蜡烛熄灭 |
② | 铜圈加热后,立即罩在蜡烛火焰上 | 蜡烛继续燃烧 |
③ | 铜圈不加热,直接罩在蜡烛火焰上 | 蜡烛熄灭 |
(1)验证可燃物燃烧需要O2的现象是______。
(2)对比实验②和③,可以得出可燃物燃烧的条件是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一支试管中放入一小段镁条(已擦去氧化膜),再向试管中加入一定量的盐酸,镁条表面有________产生,反应的化学方程式是________________________________________________________。
[发现问题]为了再次观察上述反应现象,小林同学用较长的镁条重做上述实验,但发现了异常现象,试管中出现了白色沉淀。
[实验验证1]小林同学针对两次实验的不同,设计对比实验方案,探究出现异常现象的原因。
试管(盛有同体积同浓度的盐酸) | ① | ② | ③ | ④ |
镁条长度 | 1cm | 2cm | 3cm | 4cm |
相同的实验现象(省略题干现象) | 快速反应,试管发热,镁条全部消失 | |||
沉淀量差异(恢复至20℃) | 无 | 少量 | 较多 | 很多 |
[得出结论]镁条与盐酸反应产生白色沉淀与________有关。
[追问]白色沉淀是什么物质?
[查阅资料]①20 ℃时,100 g水中最多能溶解氯化镁54.8 g;
②镁能与热水反应产生一种碱和氢气;
③氯化银既不溶于水也不溶于稀硝酸。
[做出猜想]猜想一:镁;猜想二:氯化镁;猜想三:氢氧化镁,猜想的依据是____________________(用化学方程式表示)。
[实验验证2]将白色沉淀洗涤干净,分别取少量沉淀于A、B、C试管中,进行如表实验:
试管 | 操作 | 现象 | 结论 |
A | 加入足量盐酸 | ________,白色沉淀________ | 猜想一不正确,但这种白色沉淀能溶于盐酸 |
B | 加入足量水 | 白色沉淀________ | 猜想二不正确 |
C | 加入适量稀硝酸 | 白色沉淀消失 | 原白色沉淀中含有的离子是: |
继续滴加几滴硝酸银溶液 | 出现大量白色沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D是初中化学常见物质,如图是包含A、B、C、D和盐酸5种物质的“化学拼图”,相邻两张卡片所标的物质(或其溶液)间能发生反应。

(1)单质A不可能是_____(填序号)。
①Mg ②Fe ③Cu ④C
(2)若B为铁锈的主要成分Fe2O3,则B与盐酸反应的化学方程式为_____。
(3)若D为苛性钠,写出属于中和反应的化学方程式:_____。
(4)若C为碳酸钠,将二氧化碳通入C溶液,可化合生成碳酸氢钠,该反应的化学方程式为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com