【题目】A、B、C三种物质的溶解度曲线如图所示,下列分析不正确的是
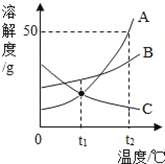
A. t1℃时,A、C两种物质的饱和溶液中溶质的质量相等
B. t2℃时,把50g水中能得到A的饱和溶液,其中溶质和溶液的质量比为1:3
C. 将t2℃时,A、B、C三种物质的饱和溶液降温至t1℃时,所得溶液的溶质质量分数的大小关系是B>A>C
D. 将C的饱和溶液变为不饱和溶液,可采用降温的方法
参考答案:
【答案】A
【解析】本题主要考查固体溶解度曲线及其作用;饱和溶液和不饱和溶液相互转变的方法;溶解性和溶解度的关系。据溶解度曲线可比较同一温度下不同物质的溶解度大小。
A、由图可知,t1℃时,A、C两种物质的溶解度相等,但没有指明溶液的质量,故无法比较溶质的质量。错误
B、t2℃时,a的溶解度是50g,即100g水中最多溶解50g的a,溶质:溶液=50g:(100g+50g)=1:3,正确
C、ab的溶解度随温度升高而增大,c的溶解度随温度升高而减小,所以将t2℃时a,b,c三种物质的饱和溶液降温至t1℃时,ab析出晶体,溶质的质量分数减小,c溶解度增大,溶质的质量分数不变,与降温前相等;据饱和溶液中溶质的质量分数的计算式,即溶解度越大质量分数也就越大,而t1℃时b的溶解度大于a的溶解度大于t2℃时c的溶解度,所以此时溶液的质量分数关系是b>a>c,正确
D、c的溶解度随温度的降低而增大,所以将c的饱和溶液变为不饱和溶液,可采用降温的方法,正确;
故选:A
-
科目: 来源: 题型:
查看答案和解析>>【题目】“五一”假期,小兵对“锌与硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸的质量分数有关;b.可能与锌的形状有关。
【设计并实验】小兵用不同质量分数的硫酸和不同形状的锌进行如下实验。
实验编号
硫酸的质量分数
(均取20mL)
锌的形状
(均取1g)
氢气的体积(mL)
(均收集3分钟)
①
20%
锌粒
31.7
②
20%
锌片
50.9
③
30%
锌粒
61.7
④
30%
锌片
79.9
(1)写出稀硫酸与锌反应的化学方程式________________________________________。
(2)小兵用下图装置收集并测量氢气的体积,其中量筒的作用是_______________________,氢气应从________(填e或f或g)管通入。

【收集证据】
(3)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是____________。
【得出结论】
(4)结论是___________________________________________。
【评价与反思】(注意:若答对(5)(6)两小题奖励4分,化学试卷总分不超过60分)
(5)下表是小兵第①组实验的详细数据。
时段(均为1分钟)
第1分钟
第2分钟
第3分钟
第4分钟
第5分钟
第6分钟
H2的体积
3.1mL
16.7mL
11.9mL
9.6mL
7.6mL
6.0mL
请描述锌与硫酸反应的快慢的变化并解释原因______________________________。
(6)锌与硫酸反应的快慢可能还受哪些因素影响?设计实验验证。
_____________________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图为实验室制取气体时常见的装置(其中G、I为干燥装置),根据装置回答下列问题:
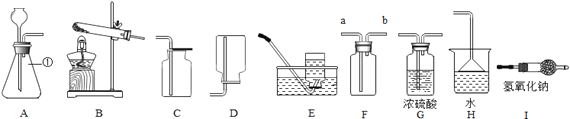
(1)仪器①的名称______.
(2)用B装置制取的某气体可使带火星的木条复燃,请写出用B装置制取该气体的化学方程式______.
(3)现用C装置收集到一瓶无色无味的气体,欲检验其是否为CO2的方法是______;若改用F装置收集该气体,则气体应从______(填“a”或“b”)通入.
(4)常温下,氨气(NH3)是一种有刺激性气味的气体,极易溶于水,密度比空气小,溶液呈碱性.实验室制取氨气的原理是NH4C1(固)与Ca(OH)2(固)混合共热.选择的发生装置是_____,收集装置是_______ 。现要制得干燥的氨气,可将气体通过___________(填装置序号)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某工厂欲从含有CuS04的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如图:
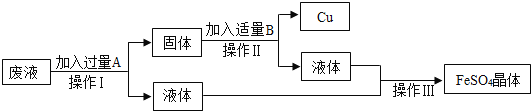
(1)操作Ⅰ的名称是______,需用到的玻璃仪器除烧杯之外还有______.
(2)加入过量A物质的化学式是______,A过量的目的是______,
反应的化学方程式是______.
(3)加入适量B物质的化学式是______.
-
科目: 来源: 题型:
查看答案和解析>>【题目】ClO2是新一代自来水消毒剂.如图为制取ClO2反应的微观示意图.下列有关该反应的说法正确的是
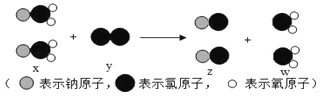
A. 该反应的化学方程式为:2NaClO2+Cl2═2NaCl+ClO2 B. x是化合物,y单质
C. z、w都是氧化物 D. 该反应属于置换反应
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列化肥中属于复合肥的是
A. KNO3 B. 钙镁磷肥 C. NaH2PO4 D. NH4NO3
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据如图装置,回答下列有关问题:
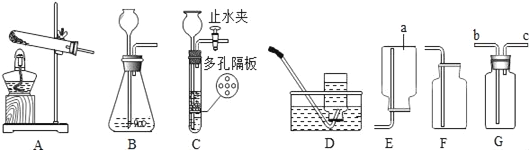
(1)装置图中仪器a的名称为______.
(2)采用加热氯酸钾和二氧化锰的混合物制取氧气,可选用的发生装置和收集装置的组合分别是______.
(3)G装置在化学试验中有广泛的应用,若用G装置采用排空气法收集氢气,氢气应从______进.若要收集到干燥的氢气,则在G 瓶中应装入的试剂是__________,氢气应从______进,用E装置收集。
(4)制取二氧化碳最好选用的发生装置是______,该装置与另一个可选用的装置相比,其主要优点是______.
相关试题

