【题目】Ⅰ.下列各图是进行O2、CO2的实验室制取和有关性质的实验装置.
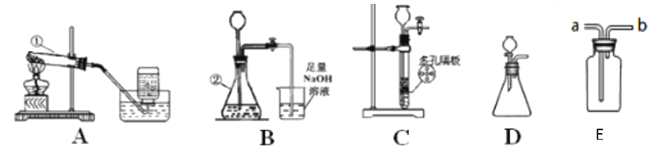
(1)标号仪器的名称:①______________②______________。
(2)用氯酸钾固体制取O2,应选用上图中的_____装置(填字母);反应的化学方程式为______。
(3)能控制反应速率的气体发生装置为____________,写出此装置制取氧气的化学方程式___________;若用E装置排水取气法收集一瓶氧气,气体应从_____端进入(填a或b)。
(4)用稀盐酸和大理石在B装置中反应制取CO2化学方程式为___________________。检验二氧化碳有关性质,观察到烧杯中导管口有气泡冒出,但无其它明显现象.若证明CO2与NaOH溶液发生了化学反应,以下方案不合理的是______________(填序号).
A.取少量烧杯中液体滴加无色酚酞 B.取少量烧杯中液体滴加足量稀盐酸
C.取少量烧杯中液体滴加氯化钙溶液 D.取少量烧杯中液体滴加氢氧化钙溶液,若用上述实验方案测出CO2与NaOH溶液发生了化学反应,反应的化学方程式为______
(5)用C装置代替B中的气体发生装置制备CO2,优点是___________________________;
参考答案:
【答案】 试管 锥形瓶 A 2KClO3 ![]() 2KCl+3O2↑ D 2H2O2
2KCl+3O2↑ D 2H2O2 ![]() 2H2O+O2↑ b CaCO3 + 2HCl == CaCl2 + H2O + CO2↑ A 2NaOH+CO2==Na2CO3+H2O 控制反应的发生和停止
2H2O+O2↑ b CaCO3 + 2HCl == CaCl2 + H2O + CO2↑ A 2NaOH+CO2==Na2CO3+H2O 控制反应的发生和停止
【解析】(1)图中①是试管,②是锥形瓶;
(2)用氯化钾固体制取O2,是固体的加热反应,氧气不易溶于水,所以可用装置A进行,反应方程式是:2KClO3 ![]() 2KCl+3O2↑;
2KCl+3O2↑;
(3)装置D中可以控制分液漏斗的活塞来控制液体的加入量,从而控制反应速率;适用于过氧化氢制氧气,化学方程式为:2H2O2 ![]() 2H2O+O2↑;由于氧气的密度小于水,所以氧气应从b管进入将水从a管排除;
2H2O+O2↑;由于氧气的密度小于水,所以氧气应从b管进入将水从a管排除;
(4)大理石的主要成分是碳酸钙,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl =CaCl2 +H2O+CO2↑;A、二氧化碳与氢氧化钠反应生成碳酸钠溶液显碱性,反应发生变红,不反应也变红,错误;B、碳酸钠和稀盐酸反应有二氧化碳气体生成,可以证明CO2与NaOH溶液发生了化学反应,正确;C、碳酸钠和氯化钙反应生成碳酸钙沉淀,可以证明CO2与NaOH溶液发生了化学反应,正确;D、碳酸钠和石灰水反应生成碳酸钙沉淀,可以证明CO2与NaOH溶液发生了化学反应,正确。二氧化碳与氢氧化钠反应生成碳酸钠和水,化学方程式为:2NaOH+CO2=Na2CO3+H2O;
(5)通过C装置中的多孔隔板和阀门可以随时控制反应的发生和停止。
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中不正确的是
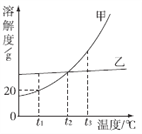
A. t1 ℃时,60 g甲的饱和溶液中溶解了10 g的甲
B. 将t2 ℃甲、乙两种物质的饱和溶液升温至t3 ℃(溶剂的量不变),两种溶液中溶质的质量分数相等
C. t2 ℃时,要使接近饱和的乙溶液达到饱和状态,可蒸发溶剂
D. t2 ℃甲、乙两种物质的饱和溶液中所含溶质的质量相等
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列图像不能正确反映其对应变化关系的是
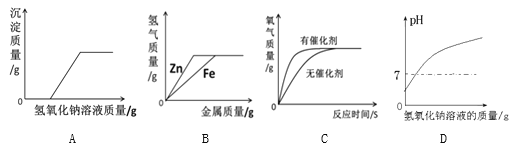
A.向一定质量的硫酸铜和稀硫酸的混合溶液中逐滴加入氢氧化钠溶液
B.向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉
C.用等质量、等溶液的过氧化氢溶液在有无催化剂条件下制氧气
D.一定质量稀盐酸中逐滴加入氢氧化钠溶液
-
科目: 来源: 题型:
查看答案和解析>>【题目】Ⅰ.请你根据所学知识,从A.干冰 B.硝酸钾 C.金刚石 D.碳酸氢钠E.甲烷五种物质中选择恰当物质的序号填空。
(1)农业上可用作复合肥的是_____;(2)可用于人工降雨的是______
(3)焙制糕点所用的发酵粉主要成分之一________;(4)可做玻璃刀的是_________
(5)天然气的主要成分_______。
Ⅱ.用化学用语填空:
(1)标出二氧化硫中硫元素的化合价_________;(2)2个铵根离子_______;
-
科目: 来源: 题型:
查看答案和解析>>【题目】某些食品的包装袋内,放有装有白色颗粒状固体的小纸袋,上面写着“干燥剂,主要成分为生石灰”。某同学对一袋久置空气中的干燥剂进行了探究。
他先取部分久置干燥剂倒入适量水中,充分搅拌、过滤,得到白色固体和滤液。然后对滤液的酸碱性和白色固体的组成作了探究。
(实验探究一)探究滤液的酸碱性
该同学测定了滤液的酸碱性,你认为该滤液显____________性。
(实验探究二)探究过滤后白色固体的组成
该同学认为白色固体中可能含有的物质是CaO、Ca(OH)2、CaCO3。
他查阅有关资料得知:CaO是一种白色固体,俗称生石灰,能与水反应生成氢氧化钙,并放出热量。氢氧化钙微溶于水。
(分析判断)你认为该过滤后得到的白色固体中一定不含有的物质是_______。
(实验操作)下面是该同学设计的进一步探究白色固体组成的实验方案,请你和他一起完成实验报告。
实验操作
实验现象
实验结论
①取少量白色固体,倒入适量水,充分搅拌、静置;
②向上层清液中滴加无色酚酞溶液
上层清液呈____色
白色固体中一定含有氢氧化钙
另取少量白色固体放入试管中,滴加稀盐酸
_________
白色固体中一定含有碳酸钙
(总结反思)
只通过以上实验,还不能证明这袋久置于空气中的干燥剂中是否含有CaO。请你简述一个证明这袋干燥剂中含有较多量CaO的简易实验:____。用化学方程式表示其中的反应_____。
(实验探究三)探究干燥剂样品中碳酸钙的质量分数
取上述干燥剂样品10g放入如图的装置中,充分反应后,测出了量筒中的水的体积为220mL,(此状况下二氧化碳的密度是2g/L),则此干燥剂中碳酸钙的质量分数为___________(通过计算填空)
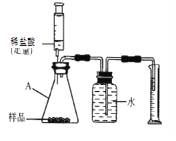
(总结反思)(实验探究三)中实验设计的不合理之处_________
-
科目: 来源: 题型:
查看答案和解析>>【题目】为了测定空气中氧气的含量,某课外活动小组设计并进行了如图所示的实验探究。下列有关说法不正确的是( )
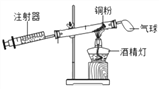
A. 该实验可用碳粉来代替铜粉进行测定
B. 该实验方法利用的是间接测量的方法
C. 造成该实验出现误差的原因可能是铜粉的量不足
D. 实验结束后,密闭装置内剩余气体的化学性质比较稳定
-
科目: 来源: 题型:
查看答案和解析>>【题目】清华大学研究人员成功研出一种纳米纤维催化剂,可将二氧化碳催化转化成液体燃料甲醇,下图为该反应的微观模拟示意图(图中微粒恰好完全反应)。下列有关说法正确的是( )
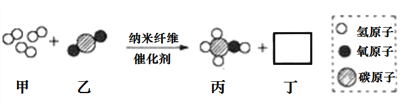
A. 该反应类型为复分解反应
B. 参加反应的甲、乙质量之比为3:1
C. 生成物丙和丁均为氧化物
D. 该反应实现了无机物到有机物的转化
相关试题

