【题目】海洋中蕴藏着丰富的化学资源,如NaCl、MgCl2、CaCl2等物质。从海水中提取金属镁的主要流程如下:

(1)电解熔融的无水MgCl2可以得到金属镁。该反应属于基本反应类型中的 反应。
(2)将海水中的镁提取出来,首先要让海水中的镁离子形成沉淀而富集起来。结合表中数据分析,为了使氯化镁转化为沉淀,应加入溶液A可能是 。
室温下几种物质的溶解度
物质 | MgCO3 | CaCO3 | Mg(OH)2 | Ca(OH)2 |
溶解度/g | 0.01 | 0.0013 | 0.0029 | 0.16 |

(3)结合MgCl2的溶解度曲线分析,操作I:蒸发浓缩、 、过滤。
参考答案:
【答案】(1)分解(2)Ca(OH)2溶液或NaOH溶液 (3)降温结晶
【解析】
试题分析:电解熔融的无水MgCl2可以得到金属镁和氯气,属于分解反应。(2)依据溶解度图转化成Mg(OH)2更能把镁离子富集, 故A为Ca(OH)2溶液或NaOH溶液 ;(3)MgCl2的溶解度随温度升高而增大,故降温结晶。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列出去物质中的少量杂质(括号内为杂质)的方法,错误的是
A.N2 ( O2 )——通入足量的灼热铜网
B.Ca(OH)2 ( CaO ) ——加入适量稀盐酸
C.MnO2粉末 ( KCl )——溶解、过滤、洗涤、干燥
D.H2 (水蒸气)——通过盛有足量浓硫酸的洗气瓶
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下图回答问题。
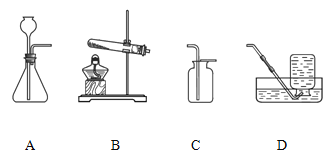
(1)实验室制取二氧化碳,选用的发生装置是 (填序号)。
(2)用装置B制氧气,其反应的化学方程式是
(3)用装置D收集氧气时,下列实验操作正确的是 (填序号)。
a.加热前,将集气瓶装满水,用玻璃片盖住瓶口,倒立在盛水的水槽中
b.加热后,观察到水中导管口开始有气泡时,立即收集气体
c.待集气瓶里的水排完后,在水面下用玻璃片盖住瓶口,移出水槽正放 在桌面上
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲、乙、丙、丁、戊五种常见物质,由氢、碳、氧、钠、氯、钙6种元素中的2~3种组成。
(1)甲的溶液可用于实验室制氧气,甲是 。
(2)向乙的溶液中放入铁钉,会有气泡冒出,一段时间后还能观察到 ,该反应的化学方程式是 。
(3)如图所示,分别取少量丙、丁、戊三种白色固体于A、B、C三支试管中,进行
如下连续实验。
步骤1:加入一定量水充分溶解,A中固体不减少,B和C中的固体消失;
步骤2:再滴加几滴酚酞溶液,振荡,A中无明显现象,B和C中无色液体变红;
步骤3:继续加入一定量乙的溶液,A和B中产生大量气泡,B和C中红色褪去。
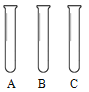
分析:①丙和乙反应的化学方程式是 。
② 若步骤3中,B和C所得溶液除酚酞和水外,还一定含有一种相同的物质,则丁和戊分别是 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】比较推理是化学学习中常用的思维方法,下列推理正确的是
A.石墨能导电,故金刚石也能导电 B.生铁比纯铁硬,故黄铜也比纯铜硬
C.烧碱属于碱,故纯碱也属于碱 D.碘难溶于水,故碘也难溶于汽油
-
科目: 来源: 题型:
查看答案和解析>>【题目】“煤化工”是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。请回答下列问题:
(1)煤的加工产品有很多用途,其中焦炭广泛应用于炼铁。下列说法正确的是 (填序号)。
a.煤是复杂的混合物,主要含碳元素
b.煤加工成焦炭的变化属于物理变化
c.煤燃烧排放的二氧化硫、二氧化氮是形成酸雨的主要物质
(2)以煤、空气、水为原料还可以合成氨(NH3)。主要生产流程如下:
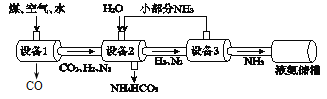
设备1中主要反应:① C + O2
 CO2; ② C + H2O
CO2; ② C + H2O CO + H2。为了保持炉温,提高H2的产量,需要交替通入空气和水蒸气。
CO + H2。为了保持炉温,提高H2的产量,需要交替通入空气和水蒸气。判断:设备1中反应② (填“放出”或“吸收”)热量。设备2中发生反应的化学方程式是 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质属于纯净物的是
A.食盐 B.食醋 C.牛奶 D冰水混合
相关试题

