【题目】甲乙小组按右图所示实验探究蜡烛的燃烧产物,获得了不同的实验现象。

甲组:烧杯内壁有无色液滴
乙组:烧杯内壁有无色液滴,烧杯底部附着有黑色固体
【提出问题】 同学们查阅教材实验,得知无色液滴是水,但黑色固体是什么呢?
【猜想】 同学们猜想黑色固体的主要成分是碳。
【实验验证】利用下图所示装置,甲、乙小组的同学分别设计了以下方案进行验证
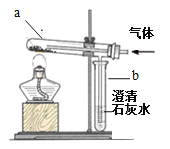
实验操作 | 实验现象 | |
甲组 | 取少量该黑色固体于a中,通入空气,点燃酒精灯加热。 | 黑色固体燃烧,①___________, b中溶液变浑浊。 |
乙组 | 取少量该黑色固体于a中,通入 ②________,点燃酒精灯加热。 | 黑色固体剧烈燃烧,发出白光,b中溶液变浑浊。 |
【分析与结论】
(1)实验结束时,停止通入气体,后续实验操作顺序应是_____(填字母序号)。
A. 熄灭酒精灯,停止加热 B.将试管b移走
(2)b中的实验现象说明黑色固体燃烧生成了_______,由此可推断猜想正确,理由是_________________________。
【反思】
进一步实验发现,罩在火焰上方的烧杯位置越低,产生黑色固体越多。查阅资料可知:蜡烛+氧气(足量)→二氧化碳 + 水;蜡烛+氧气(少量)→ 一氧化碳 + 水;
由此推测乙组实验产生黑色固体的原因是________________。
参考答案:
【答案】 发出红光(或红热 红亮) 氧气 BA CO2 化学反应前后元素种类不变,二氧化碳的碳元素一定来紫黑色固体 烧杯位置降低使氧气的量减少,氧气的量少到一定程度时蜡烛和氧气反应产生黑色固体碳
【解析】【试题分析】本题考查了蜡烛燃烧的探究实验。包括实验现象、燃烧的条件、质量守恒定律等。
【实验验证】碳为黑色固体,通入空气,点燃酒精灯加热,黑色固体燃烧,发出红光,b中溶液变浑浊.
取少量该黑色固体于a中,通入氧气,点燃酒精灯加热,黑色固体剧烈燃烧,发出白光,b中溶液变浑浊.
【分析与结论】
(1)实验结束时,停止通入气体,后续实验操作顺序应是将试管b移走,再熄灭酒精灯,停止加热;
(2)b中溶液变浑浊,说明有二氧化碳生成,根据质量守恒定律,化学反应前后元素的种类不变,二氧化碳中的碳元素一定来源于黑色固体,故黑色固体为碳;
【反思】
烧杯位置降低使氧气的量减少,氧气的量少到一定程度时,蜡烛和氧气反应生成黑色固体碳,
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列有关铁的性质中属于化学性质的是
A. 有良好的导电、导热性 B. 有良好的延展性
C. 在潮湿空气中易生锈 D. 具有银白色金属光泽
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下图所示实验装置回答问题:
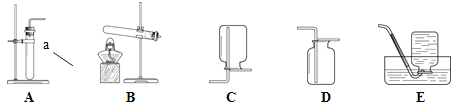
(1)图中仪器a的名称为 ________。
(2)实验室用过氧化氢制取氧气,应选用的发生装置是 _____(填字母序号),该反应的符号表达式为 __________________________。
(3)若用B装置制备氧气,发生反应的符号表达式为 __________________________。
(4)若用E装置收集满氧气后,取出的集气瓶应_____(填“正””或“倒”)放在实验台上。若用排气法收集氧气时,检验氧气是否收集满的方法是 _____。
(5)已知甲烷(CH4)气体难溶于水,密度小于空气。若要收集干燥的甲烷气体,应选用的装置是_____。
-
科目: 来源: 题型:
查看答案和解析>>【题目】金刚石、石墨和C60都是由碳元素组成的单质,下列说法正确的是( )
A.它们是同一种物质 B.它们碳原子的排列方式不同
C.它们的化学性质不同 D.它们的物理性质不同
-
科目: 来源: 题型:
查看答案和解析>>【题目】在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如图.下列说法中不正确的是( )
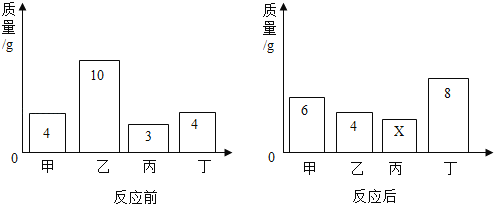
A..该反应为分解反应
B..丙可能为该反应的催化剂
C.参加反应的乙、丁质量比为3:2
D.丁相对分子质量是甲的2倍
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列变化中,属于物理变化的是
A. 铁锅生锈 B. 西瓜腐烂 C. 煤气燃烧 D. 分离液态空气
-
科目: 来源: 题型:
查看答案和解析>>【题目】我校初三年级化学兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验。
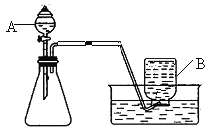
甲同学选用如上图所示的装置制取氧气。
写出仪器B的名称:______。
甲同学应选取的试剂是MnO2和_______(填化学式),Mn02固体在该反应中起_______作用。该反应的化学方程式为:________________________。
实验前,甲同学先向仪器A中加入水,然后将导管放人水槽中,并打开仪器A的活塞,观察导管口是否有连续的气泡出现。该实验操作的目的是_____________
乙同学称取一定质量KMn04放在大试管中,将温度控制在250℃加热制取O2,该反应的化学方程式为________。实验结束时,乙同学发现收集到的O2大于理论产量,针对这一现象,同学们进行了如下探究:
【提出猜想】猜想Ⅰ:反应生成的MnO2分解放出02;
猜想Ⅱ:反应生成的K2Mn04分解放出O2
做出上述猜想的理由是_______。
【实验验证】同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的Mn02,在250℃条件下加热一段时间,冷却后测得Mn02的质量不变。则猜想________________错误。
②第二组同学取K2Mn04在250℃条件下加热,没有用测定质量的方法得出了猜想Ⅱ正确的结论。该组同学选择的实验方法是_________________ 。
相关试题

