【题目】同学们,你们都看过科幻小说《海底万里行》吧!在文章中描述的尼摩船长和他的“鹦鹉螺号”潜艇在大海中畅游的故事,相信给你们留下了深刻的印象。在潜水艇里常要配备氧气的再生装置,其反应原理:在常温下用过氧化钠固体(Na2O2)与二氧化碳反应生成碳酸钠(Na2CO3)和氧气,保证长时间潜航。假设每一个船员每小时所需的氧气等于100L空气中所含的氧气,那么“鹦鹉螺号”潜艇一次贮气15000000L空气。(已知:标准状况下,O2的密度为1.429g/L,氧气在空气中的体积分数均按1/5计算)请解答:
(1)写出氧气再生装置里反应的符号表达式___________
(2)这些空气中所含氧气的质量是多少Kg_______?
(3)这些空气可供50名船员在潜航状态下持续使用多少天______?
参考答案:
【答案】Na2O2 + CO2![]() Na2CO3 + O2 4287Kg 125
Na2CO3 + O2 4287Kg 125
【解析】
(1)在常温下,过氧化钠固体(Na2O2)与二氧化碳反应生成碳酸钠和氧气,该反应的符号表达式为:Na2O2+CO2![]() Na2CO3+O2;
Na2CO3+O2;
(2)这些空气中所含氧气的质量是=15000000L![]() 1.429g/L
1.429g/L![]() 1/5=4287Kg;
1/5=4287Kg;
(3)这些空气可供50名船员在潜航状态下持续使用的天数=4287Kg![]() 100L
100L![]() 1.429g/L
1.429g/L![]() 1/5
1/5![]() 50=125天。
50=125天。
-
科目: 来源: 题型:
查看答案和解析>>【题目】解答下列各题。
(1)写出下列反应的符号表达式,在括号内注明反应的基本类型。
①细铁丝在氧气中剧烈燃烧_________(__________)
②加热一种暗紫色固体制氧气_______(________)
(2)在下列物质中:①液氧;②氯化钠;③二氧化氮;④空气;⑤冰水(用序号填空,下同)含有氧分子的是____,属于化合物的是________,属于单质的是__________,属于氧化物的是______。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图是部分元素周期表和砷元素(As)的信息,据此回答下列问题:
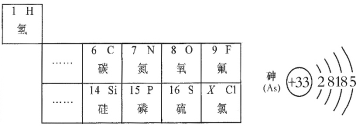
(1)空气中含量最多的元素的原子序数是_________。
(2)画出原子序数为X的原子的结构示意图 _________,化学反应中该原子容易_______(填“得到”或“失去”)电子。
(3)砷(As)元素位于元素周期表第___周期,____主族,砷元素与表中磷元素的化学性质________,(填“相似”或“不相似”)。
(4)查阅资料:具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下列各组粒子中属于等电子体是_____(填字母序号)
A. NO和O2 B. CH4和NH4+ C. H2O和CO2 D. PO43ˉ和CO32ˉ
-
科目: 来源: 题型:
查看答案和解析>>【题目】图是初中化学中常见的实验装置,回答下列问题:

(1)B中仪器a的名称是_______。实验室用氯酸钾和二氧化锰制取氧气,可选用的发生装置为__(填装置编号),该反应的符号表达式为_____小明将高锰酸钾混入氯酸钾中,加热时发现氯酸钾的反应速率加快,在此反应中高锰酸钾______(填“是”或“不是”)催化剂。
(2)小明若用D装置来收集氧气,则检验氧气收集满的方法是________。
(3)小明用排水法收集氧气实验完毕后,拆卸装置的正确排序是_________(填序号)
①撤去酒精灯 ②从水槽中移出导气管
③从铁架台上拆下试管 ④清洗仪器并放回指定位置
(4)实验室进行实验需要制取少量的乙炔气体,小婷同学查得相关资料如下:
Ⅰ.乙炔(C2H2)是一种无色、无味、无嗅,比空气轻,微溶于水,易燃烧。
Ⅱ.(A)天然气在电炉高温下反应可生成乙炔:CH4
 C2H2 + H2
C2H2 + H2 (B)固体碳化钙(CaC2)与水反应可生成:CaC2+ H2O
 Ca(OH)2 + C2H2↑则实验室制取乙炔气体应选择的反应是________(填“A”或“B”),制取乙炔的发生装置是_____(填装置编号,下同),收集装置是______。
Ca(OH)2 + C2H2↑则实验室制取乙炔气体应选择的反应是________(填“A”或“B”),制取乙炔的发生装置是_____(填装置编号,下同),收集装置是______。(5)已知:氨气(NH3)的密度比空气小,极易溶于水形成氨水。实验室收集氨气时,为防止多余的氨气逸散到空气中,最好选用上面的____(填“E”或“F”)装置吸收。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列化学反应中,属于四大基本反应类型是(______)
A. CO+CuO
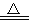 Cu+CO2 B. 2H2O2
Cu+CO2 B. 2H2O2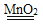 2H2O+O2↑
2H2O+O2↑C. CH4+2O2
 CO2+2H2O D.____________
CO2+2H2O D.____________ -
科目: 来源: 题型:
查看答案和解析>>【题目】如图所示,在烧杯A中装入20mL蒸馏水,滴入2-3滴酚酞试液。在烧杯B中装入10mL浓氨水。然后用一只大烧杯把A、B两烧杯溶液罩在一起。过几分钟,可以观察到烧杯A中的溶液变成_______色。
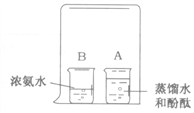
通过上述现象,得出的结论有:分子________________,浓氨水呈______(填“酸性”或“碱性”)。
还可以通过什么方法检测氨水的酸碱性呢?所用的药品的名称__________,产生的现象是______________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】在学习碳酸钠的性质时,做过“向盛有少量碳酸钠溶液的试管里滴入澄清的石灰水”的实验,发现没有看见白色沉淀的现象。经分析,可能是石灰水变质了,变质的原因是(用化学方程式表示)_____________________________。用实验来证明石灰水完全变质,所用的试剂是________,产生的现象是______________________________。若不考虑用错药品,还有可能导致没有看见白色沉淀的现象的原因____________________________。(此空2分)
相关试题

