【题目】在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表:
物质 | 甲 | 乙 | 丙 | 丁 |
反应前的质量(g) | 54 | 17 | 20 | 0 |
反应后的质量(g) | 10 | 0 | 2 | X |
下列说法正确的是( )
A.甲物质全部反应完 B.x为79
C.参加反应的丙物质的质量为20g D.该反应为分解反应
参考答案:
【答案】B
【解析】
试题分析:根据题中提供的信息及质量守恒定律可知甲,物质为反应物,变化的质量为44g,乙物质为反应物变化的质量为17g,丙物质为反应物,变化的质量为18g,故X=79,是正确的叙述,答案选择B
-
科目: 来源: 题型:
查看答案和解析>>【题目】某研究性学习小组欲利用下列装置进行相关气体制取的探究,请你分析并填空:
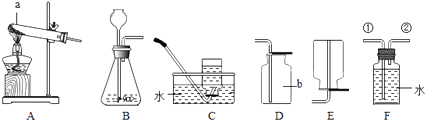
(1)写出图中仪器a名称 .
(2)实验室中既可以用来制取氧气,又可以用来制取二氧化碳的装置是(填字母).
(3)用装置A与C连接制取并收集氧气,则装置A中反应的化学方程式为 . 若用盛满水的F装置收集氧气,应从导管(填①或②)通入.
(4)甲烷是一种无色、无味、难溶于水、密度小于空气密度的气体,实验室用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷,则实验室制取并收集甲烷应选择的装置组合是 -
科目: 来源: 题型:
查看答案和解析>>【题目】实验室模拟“侯氏制碱法”制纯碱,其原理是NaCl+NH4HCO3=NaHCO3+NH4Cl,再将碳酸氢钠加热分解得到纯碱。下图是NaCl、NH4Cl、NaHCO3的溶解度曲线,下列说法正确的是( )
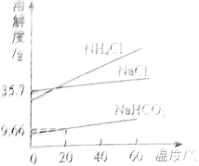
A.NaHCO3从溶液中分离出,可采用的操作是蒸发结晶
B.NH4Cl饱和溶液的溶质质量分数一定大于NaCl饱和溶液的溶质质量分数
C.40℃时,溶解度大小关系是:NH4Cl>NaCl>NaHCO3
D.20℃时,100g水中加入11.7g NaCl和15.8g NH4HCO3固体,充分反应后,理论上可析出7.14g NaHCO3晶体
-
科目: 来源: 题型:
查看答案和解析>>【题目】用分子的观点解释下列现象,错误的是
A. 热胀冷缩──分子大小随温度的变化而改变 B. 花香四溢──分子不停地运动
C. 食物腐败──分子发生了变化 D. 水结成冰──分子间隔发生变化
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质属于纯净物的是
A. 纯净的盐水 B. 硬水 C. 冰水混合物 D. 洁净的空气
-
科目: 来源: 题型:
查看答案和解析>>【题目】决定元素化学性质的是( )
A.元素的相对原子质量 B.原子核内的中子数
C.原子核内的质子数 D.原子核外的最外层电子数
-
科目: 来源: 题型:
查看答案和解析>>【题目】请结合下图回答问题:
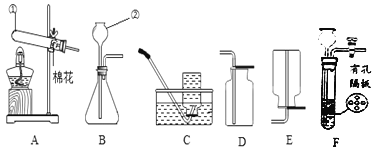
(1)写出有标号的仪器名称:① ,② 。
(2)实验室用高锰酸钾制取O2的化学方程式为 ,用A、D装置制取O2时,为防止高锰酸钾进入导管,可采取的措施是 。
(3)实验室用B、C装置制取CO2的化学方程式为 ,若将发生装置由B改为F,其优点是 。
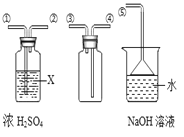
(4)SO2是无色有刺激性气味的有毒气体,密度比空气大,易溶于水。SO2的某些化学性质与CO2相似,实验中常用NaOH溶液吸收SO2尾气。用下图所示装置收集一瓶干燥的SO2,装置中导管按气流方向连接顺序是①→②→ → →⑤(填序号);图中漏斗的作用是 ;烧杯中NaOH溶液的 (用化学方程式表示)。
相关试题

