【题目】废旧酸性锌锰干电池结构及主要成分示意如图。
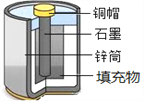

某兴趣小组拟采用如下方法回收其中的几种物质。试回答下列问题。
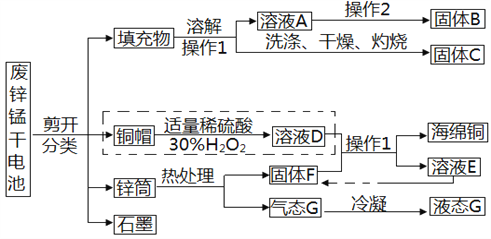
(1)回收废旧干电池可以减少固体废弃物和_________________________对环境的污染。
(2)实验室进行操作1时,用到的玻璃仪器有:烧杯、玻璃棒、_______________。
(3)固体B回收后常用作化肥,则检验固体B中阳离子的方法是:_____________________。
(4)回收过程中要除去溶液D中过量的H2O2后才能进行后续操作,如利用流程中的物质达到此目的,操作过程是:_______________________________________。
虚线框里发生反应的方程式为:____________________________________。
请另设计一种方案完成虚线框内流程:________________________________________。
参考答案:
【答案】 重金属离子 漏斗 取样,加氢氧化钠(碱)溶液,加热,生成使湿润的红色石蕊试纸变蓝的气体 加入固体C直到无气体产生,过滤 Cu+H2O2+H2SO4== CuSO4+2H2O 在空气中充分灼烧后再加适量稀硫酸
【解析】(1)废旧干电池含有重金属离子,回收可以减少重金属离子对环境的污染。
(2)操作1将固体和液体分开,所以操作1是过滤,用到的玻璃仪器有:烧杯、玻璃棒、漏斗;
(3)干电池的填充物中含有氯化铵,溶解后进入溶液A,所以固体B用作化肥,为氯化铵,验证铵根离子可以,取样,加氢氧化钠(碱)溶液,加热,生成使湿润的红色石蕊试纸变蓝的气体;
(4)过氧化氢在二氧化锰的催化下生成水和氧气,所以要除去溶液D中过量的H2O2,可以加入固体C直到无气体产生,过滤;铜与过氧化氢及硫酸反应生成硫酸铜和水,化学方程式为Cu+H2O2+H2SO4=CuSO4+2H2O;也可以将铜帽在空气中充分灼烧后再加适量稀硫酸,得到硫酸铜。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某同学利用如图装置探究铁与氧化铁化合的生成物成分。
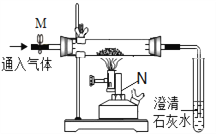
【认识仪器】由仪器N可知该反应的条件是_____________。
【查阅资料】铁的氧化物中只有Fe3O4能被磁铁吸引。
某些铁的氧化物加热时能与氧气反应。
【提出猜想】猜想①是FeO;
猜想②是Fe3O4;
猜想③是FeO和Fe3O4混合物。
【实验步骤】
①连接组装仪器,检查装置的气密性,方法是:关闭弹簧夹M,_________________________________________________________。
②称取16.0g氧化铁粉末与质量为m的铁粉,均匀混合后,放入玻璃管。
③通入CO2,当观察到明显现象时,夹上弹簧夹M,开始加热玻璃管。
④当固体全部呈黑色后,停止加热,______________________________________。将玻璃管中黑色粉末倒在滤纸上,取样,滴加稀盐酸,无气泡产生,用磁铁吸引,粉末被部分吸引。
【实验结论】猜想_________成立。所加铁粉质量m的范围是_________________。
【问题讨论】实验中澄清石灰水的主要作用是______________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列课外实验不能成功的是
A. 用淬火后的缝衣钢针制作钓鱼钩
B. 用酒精浸泡捣烂的紫罗兰花瓣制酸碱指示剂
C. 用6B铅笔芯、电池、小灯泡和导线,验证石墨的导电性
D. 用石英砂、活性炭和小石子等制简易净水器
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学造福生活。
1926年,英国科学家贝纳尔提出预言:只要有足够的压强,任何元素都能变成金属.如把氢气放到-260℃和250至260个标准大气压下,就能把每个氢原子非常紧密地挤在一起,而得到金属氢。现在,预言终于在实验室里实现了。金属氢是一种高密度的储能材料.金属形成后,可保持稳定的状态。
请回答下列问题:
(1)大规模制取氢气较合适的方法是在催化剂作用下,利用太阳能分解水,反应的化学程式是:
______________________________________。
(2)氢气被看作是理想的“绿色能源”,主要原因是___________________________________。
目前氢能的开发和利用面临着许多困难,金属氢的使用主要解决氢能开发利用中的困难是________________________________________。
(3)金属氢中氢元素的化合价为___________。从微观的角度来分析,氢气和金属氢的主要区别是
_______________________________________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物品所使用的主要材料为金属材料的是
A. 陶瓷花瓶 B. 纯棉帽子 C. 黄金首饰 D. 塑料油瓶
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列过程中发生了化学变化的是
A. 汽油挥发 B. 风力发电 C. 铁矿石炼铁 D. 太阳能取暖
-
科目: 来源: 题型:
查看答案和解析>>【题目】将黑色粉末A和无色液体B混合,生成一种无色无味的气体C;加热暗紫色固体E,可同时得到A和C;无色气体C能使带火星的木条复燃。若将银白色金属D放在盛有C的集气瓶中燃烧,火星四射,生成一种黑色固体F,并放出热量。下列说法错误的是
A、A是二氧化锰 B、B是过氧化氢 C、C是氧气 D、E是氯酸钾
相关试题

