【题目】下表是元素周期表中第2、3周期的元素,请回答有关问题。
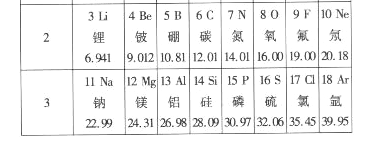
(1)下列各组具有相似化学性质的元素是________(填字母序号);
A.Na、Cl B.O、S C.F、C1 D.Cl、Ar
(2)写出一条第三周期元素原子的核外电子排布规律__________;
(3)笫7号元素与笫12号元素的原子形成化合物的化学式为__________;
(4)某粒子的结构示意图为 ,当x-y=8时,该粒子的符号为__________;
,当x-y=8时,该粒子的符号为__________;
(5)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下列各组粒子中属于等电子体的是________(填字母序号)。
A.NO和O2 B.CO和 N2 C.SO2和 CO2 D.PO43-和SO42-
参考答案:
【答案】(1)BC;(2)同一周期的元素的原子,核外电子层数相同;(3)Mg3N2;(4)S2-;(5)BD
【解析】(1)原子的最外层电子数相同,元素的化学性质相似,故选BC。(2)同一周期的元素的原子,核外电子层数相同,最外层电子数逐渐增多。(3)笫7号元素是氮元素,在化合物中一般显-3价,笫12号元素是镁元素,在化合物中一般显+2价,两种元素的原子形成化合物的化学式为Mg3N2;(4)x-y=8,即x=8+y,是原子得到了2个电子,故该粒子的符号为S2-(5)A.NO和O2,不是等电子体,错误;B.CO和N2,都是一个分子中有2个原子,每个分子中有14个电子,正确;C.SO2和 CO2,不是等电子体,错误;D.PO43-和SO42-,每个离子中都有5个原子,每一个离子中都有50个电子,正确。故选BD。
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学是研究物质的组成、性质以及变化规律的科学。化学学习过程要关注物质的性质以及能发生哪些变化和发生变化过程中的现象。现有A、B、C三种物质,它们可能是O2、Fe、H2O、H2O2、CaO、Fe2O3、HCl、NaOH、Ca(OH)2、Na2CO3中的—种。
(1)若A、B是由相同元素组成的化合物,且B分解能产生A和C。请写出该化学反应方程式______。
(2)若A、B中含有相同的金属元素,并均可与C的溶液反应,生成金属元素化合价不同的两种盐溶液。则C的化学式是______;请写出能产生黄色溶液的化学反应方程式______。
(3)若A、B、C是三种不同类别的物质,分别属于酸、碱和盐,将它们依次加入同一个烧杯中:
① 若均无明显现象,则A、B、C分别是______ (填化学式);
② 若能产生白色沉淀,请写出酸、碱中和的化学反应方程式______。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列实验现象描述正确的是
A.硫燃烧后生成有刺激性气味的气体 B.木炭燃烧后生成黑色固体
C.铁丝在空气中剧烈燃烧,火星四射 D.红磷在空气中燃烧产生白雾
-
科目: 来源: 题型:
查看答案和解析>>【题目】金属材料在生产、生活中有着广泛的应用,人类的生产和生活都离不开金属。
(1)新型材料纳米级铁粉具有广泛的用途,它比普通铁粉更易与氧气反应,其制备的主要流程如图所示。

髙温反应器中反应的化学方程式为________。反应前需向反应器中通入氮气,目的是__________;
(2)金属活动性顺序有重要的应用。铜、铝、铁为日常生活中常见的金属,某化学兴趣小组的同学在探究铝、铜、铁三种金属的有关性质时,进行了如图的实验:

在A实验中发生反应的化学方程式为__________。将A实验结束后①、②试管内的物质倒入烧杯中,发现烧杯中的红色固体物质明显增多,其原因是__________,一段时间后过滤,滤液中的溶质一定有________(填化学式);
(3)某同学在—定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉,充分反应后,他对反应过程进行了分析,得到了以下几个图像(横坐标表示加入铁的质量),其中错误的是_______(填字母序号)。

-
科目: 来源: 题型:
查看答案和解析>>【题目】某博物馆藏有一柄古代铁剑,为防止其生锈,下列做法合理的是
A.定期用清水冲洗,除去灰尘 B.放于体验区,让观众触摸
C.用盐水除去铁剑上的锈斑 D.放在充满氮气的展览柜中
-
科目: 来源: 题型:
查看答案和解析>>【题目】用符合要求的物质的序号填空。
①生石灰 ②盐酸 ③石墨 ④碘酒
(1)可用于伤口消毒的是 。
(2)可用于制作铅笔芯的是 。
(3)可用作食品干燥剂的是 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】碳酸氢钠是小苏打的主要成分,在生产和生活中有许多重要的用途。化学课上,同学们为了解碳酸氢钠的性质,将一定质量的碳酸氢钠和稀硫酸混合,充分反应后,有气体逸出,写出该反应的化学方程式_______,同学们对反应后溶液中溶质的成分进行了探究:认为除一定含有硫酸钠外可能还含有其他成分,因此进行了猜想并做了如下实验:
【实验用品】pH试纸、锌片、氧化铜粉末、稀硫酸、氢氧化钠溶液、氯化钡溶液。
【猜想与假设】反应后溶液中溶质的可能组成成分
猜想一:硫酸钠 猜想二:硫酸钠、碳酸氢钠 猜想三:硫酸钠、硫酸
【实验探究】同学们取反应后的溶液用不同方案进行如下实验,请根据结论完成下表实验现象中的①②③。
实验方案
A
B
C
D
实验操作




实验现象
①
产生白色沉淀
试纸变色,对照标准比色卡,pH ②7
③
实验结论
猜想二不正确
猜想三正确
猜想三正确
猜想三正确
【得出结论】猜想三正确。
【评价反思】
(1)老师对同学们能用多种方案进行探究,并且得出正确的实验结论给予了肯定,同时指出探究中存在一处明显操作错误是:__________;
(2)有同学对实验方案B的结论提出了质疑,认为仅凭此现象不能得出猜想三正确,请说明理由________。
【总结提高】依据所给实验用品,设计不同的方案确认猜想三是正确的。请写出你的实验方案________。
相关试题

