【题目】某班学生在野炊时用石灰石堆成简易灶台做饭.野炊后有同学从灶台内侧敲下几小块石片,带同实验室研究其在灼烧过程中是否有新的物质生成.请你参与此项研究.
(1)根据你的知识和经验提出假设:反应中可能有__________生成,支持这个假设的依据是(用化学方程式表示):_______________________________________________.
(2)请你设计实验验证假设:________________

(3)如果要研究某块石片中参加反应的碳酸钙质量,请你再设计一个简单的实验方案(写出简要实验步骤,不要求具体计算):
步骤一:_______________________________________________________;
步骤二:_______________________________________________________;
步骤三:_______________________________________________________;
步骤四;________________________________________________________.
参考答案:
【答案】 CaO CaCO3![]() CaO+CO2↑
CaO+CO2↑
步骤和方法 | 现象 | 分析有关化学方程式 |
1.用刀在石片表层刮下一些粉末,放进小烧杯中 2.在烧杯中加入蒸馏水,然后滴加无色酚酞试液 | 溶液变红 *溶液不变红 | 溶液显碱性.说明石片中有CaO生成.CaO+H 2O ===Ca(OH) 2 *说明石片中无CaO生成 |
称量石片的质量 将石片放在大量水中浸泡或用水冲洗 将石片洗净、烘干、称量 计算(其他合理方法均给分)
【解析】(1)石灰石的主要成分为碳酸钙,碳酸钙高温下分解生成固体氧化钙,同时放出气体二氧化碳;因此可猜测带回的石片中可能含氧化钙;化学方程式为:CaCO3![]() CaO+CO2↑;(2)取下石片上一些粉末,放入适量水中,滴加无色酚酞,若溶液变红则说明石片上含氧化钙;若溶液无颜色变化,则石片上不含氧化钙;化学方程式为:CaO+H 2O
CaO+CO2↑;(2)取下石片上一些粉末,放入适量水中,滴加无色酚酞,若溶液变红则说明石片上含氧化钙;若溶液无颜色变化,则石片上不含氧化钙;化学方程式为:CaO+H 2O
=Ca(OH) 2;(3)称取一定量样品,加入足量的水,彻底溶掉分解形成的氧化钙,将石片取出烘干后称量剩余固体的质量,清除前后的质量差即为碳酸钙分解生成的氧化钙的质量,根据碳酸钙分解的化学方程式计算出分解的碳酸钙的质量。
-
科目: 来源: 题型:
查看答案和解析>>【题目】用化学符号填空:
两个氢原子_______;干冰_______;锌离子_______;硝酸铁_______;乙醇_______;氧化镁中镁元素的化合价为+2价______。
-
科目: 来源: 题型:
查看答案和解析>>【题目】从太空观察,地球是一个美丽、蔚蓝色的星球,海洋资源丰富.一地处海边的化工厂,按如下步骤进行生产:①以煤为燃料煅烧石灰石;②用加压降温的方法使产生的二氧化碳变成干冰;③使得到的生石灰与水反应;④把海水引入反应池中,使熟石灰与海水中的氯化镁反应以获取氢氧化镁;⑤用盐酸溶解氢氧化镁,再将所得溶液蒸发、浓缩、结晶.
(1)该厂的产品是____________________________________.
(2)按要求写出下列各步反应的化学方程式并注明反应基本类型:
①煅烧石灰石__________________________________(________);
②生石灰与水反应_____________________________________(________);
③熟石灰与氯化镁反应________________________________(________);
④盐酸溶解氢氧化镁___________________________(________).
-
科目: 来源: 题型:
查看答案和解析>>【题目】育才中学实验室模拟工厂治污原理,设计了如下图的装置,一方排出含2%HCl,其密度为1.03g/mL,一方排出含4%NaO0H,其密度也为1.03g/mL,然后在池中混合,充分反应后再排放.
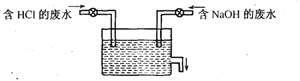
请你回答下列问题:
(1)当处理后废水pH为8时,此时控制含NaOH废水的阀门应调_____(填“大”或“小”)
(2)当处理后的废水pH约为7时,如果含HCl的废水流量为8L/s,则含Na0H废水的流量约为________L/s(精确到小数点后一位) .
-
科目: 来源: 题型:
查看答案和解析>>【题目】氯化铁是一种良好的净水剂,化学上可以用多种方法来制取.请写出四种用铁及某化合物通过一步化学反应制取氯化铁的三个化学方程式:
(1)________________________________________;
(2)____________________________________;
(3)__________________________________ . (碳酸钠不要作为反应物)
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图是工业上在一定条件下制取乙醇反应的微观示意图(其中“
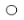 ”代表氢原子,“
”代表氢原子,“  ”代表碳原子,“
”代表碳原子,“ ”代表氧原子)。下列叙述中,不正确的是
”代表氧原子)。下列叙述中,不正确的是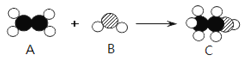
A.反应物A的化学符号为2CH2
B.反应前后三种物质的分子个数比为1:1:1
C.乙醇中碳、氢、氧三种元素的质量比为12:3:8
D.1个乙醇分子由1个氧原子、2个碳原子、6个氢原子构成
-
科目: 来源: 题型:
查看答案和解析>>【题目】几种常见物质之间的相互转化关系如图所示(每个字母各代表一种物质,每个箭号各表示一个化学反应,部分反应物、生成物及反应条件略去)。已知五种物质均由C、H、O中部分元素组成,A和B所含元素相同,D和E所含元素相同,X为单质,A为有毒气体,B和D可以发生化合反应。
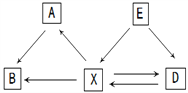
(1)A的名称是_______,E的名称是________,B的一种用途是__________________。
(2)写出X→D转化的化学方程式:_________________ 。
(3)实现A→B转化的化学反应类型____________(填“一定”或“不一定”)属于化合反应。
相关试题

