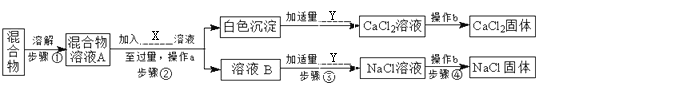
【题目】实验室里有一包含有NaCl和CaCl2两种固体的混合物,现准备将它们分离开,设计如下方案。
请完成下列问题:
(1)步骤②中发生反应的化学方程式是________________。操作b的名称是______。
(2)步骤③中加适量Y的作用是______________。
(3)在步骤④操作b中, 盛装NaCl溶液的仪器名称是__________,此操作中玻璃棒的作用是______。
参考答案:
【答案】 Na2CO3 + CaCl2 =CaCO3↓ +2NaCl 蒸发 反应过量的Na2CO3溶液 。 蒸发皿 , 搅拌,使受热均匀 。
【解析】(1)NaCl和CaCl2混合物样品加入过量的碳酸钠溶液,氯化钠不反应,氯化钙和碳酸钠反应生成碳酸钙白色沉淀和氯化钠,方程式是:Na2CO3+CaCl2═CaCO3↓+2NaCl;通过操作a固体和液体分离开来,因此操作a是过滤;碳酸钙和盐酸发生反应得到氯化钙溶液,经蒸发可得到氯化钙固体;操作b的名称是蒸发;(2)由于碳酸钠过量,所以通过a过滤后的溶液B中含有氯化钠和过量的碳酸钠,因此要得到纯净的氯化钠就需要除去碳酸钠,加入稀盐酸,碳酸钠和稀盐酸生成氯化钠和水和二氧化碳,盐酸中的溶质是氯化氢气体,蒸发时氯化氢挥发出去,蒸发后最后的固体物质是氯化钠。所以:步骤③中所加适量试剂是稀盐酸,作用是除去过量的碳酸钠;(3)步骤④要由氯化钠溶液得到氯化钠固体,操作是蒸发结晶,蒸发使用的仪器是蒸发皿,该操作中玻璃棒的作用是搅拌,使液体受热均匀,防止液滴飞溅。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列图像与对应的说法正确的是( )
A.
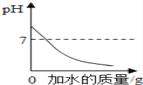 向NaOH溶液中加水稀释
向NaOH溶液中加水稀释B.
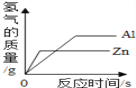 等质量的Al、Zn与足量的稀硫酸反应
等质量的Al、Zn与足量的稀硫酸反应C.
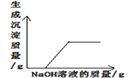 向H2SO4与CuSO4混合溶液中加入NaOH溶液
向H2SO4与CuSO4混合溶液中加入NaOH溶液D.
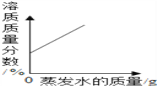 在恒温的条件下,适量蒸发饱和NaCl溶液的水分
在恒温的条件下,适量蒸发饱和NaCl溶液的水分 -
科目: 来源: 题型:
查看答案和解析>>【题目】如图是A、B、C三种物质的溶解度曲线。看图回答问题:
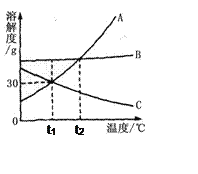
(1)在________℃时,A、B两种物质的溶解度相同。
(2)在t1℃时,将20 g A物质放入50 g水中充分搅拌,所得溶液的质量是_________g。
(3)t1℃时A、B、C三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数大小关系是___。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某校进行中考化学实验操作考查,给出以下三个考题:
a.粗盐提纯; b.二氧化碳的制取和收集; c.氧气的制取和收集
考查规定由学生抽签确定考题,某同学抽签后被监考老师引导至准备了下列仪器和药品的实验台前:
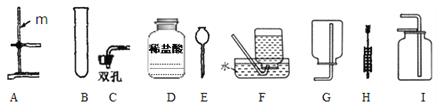
(1)上图仪器m的名称是______;甲同学抽到的考题是_____(选填a、b、c);实验前该同学发现其中缺少了一种药品,该药品名称是________;写出用以上仪器制取氧气的化学方程式_____________。
(2)下图是甲同学实验时的主要步骤,这些步骤的正确顺序是______(填编号),其中有一步骤可能导致实验失败,其改正的方法是_______________。
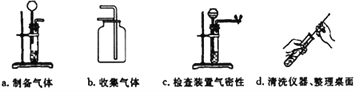
-
科目: 来源: 题型:
查看答案和解析>>【题目】恩施州内的很多景点都已经在全国乃至世界享有盛名,如“腾龙洞”、“恩施大峡谷”等;而形成这些奇谷异洞的根本原因与当地的石灰石有关。某中学的“化学兴趣小组”为了测定“腾龙洞”内石灰石样品中CaCO3的含量。取8g样品研碎后放入烧杯中,再加入100g稀盐酸恰好完全反应后,烧杯中剩余物质105.8克(假设样品中杂质不溶也不反应,不考虑水的蒸发及CO2的溶解等因素,结果保留百分号前一位小数)。试计算:
(1)样品中CaCO3的质量分数是多少_________?
(2)所得溶液中溶质的质量分数是多少_________?
-
科目: 来源: 题型:
查看答案和解析>>【题目】A常用于切割金属,在点燃条件下,A和B反应能生成C和D。反应前后分子变化的微观示意图如图所示,有关该反应的说法不正确的是

A. A物质具有可燃性 B. 该反应属于放热反应
C. 上述反应中A与D的质量比为14∶9 D. 反应类型是置换反应
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图为A、B、C三种固体物质的溶解度曲线。下列有关说法错误的是
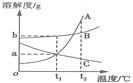
A. t1℃三种物质中B物质的溶解度最大
B. t2℃三种物质的饱和溶液中,溶质的质量分数最大的是A
C. t2℃时可用降低温度的方法使C的不饱和溶液变为饱和溶液
D. t1℃时,bgC物质完全溶解在100g水中,溶液质量为(100+a)g
相关试题

