【题目】请结合下图回答问题。
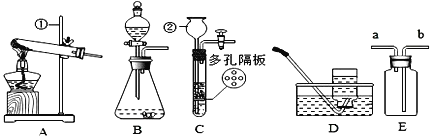
(1)仪器②的名称:____________。
(2)用氯酸钾和二氧化锰制取氧气,可选用装置____________(选填序号)和装置D组合,反应的化学方程式为____________,二氧化锰的作用是____________,若用B和D组合制取氧气,其反应的化学方程式为_____。
(3)实验室可用装置B或C制H2,C装置相对于B的优点有______,用E装置收集H2,气体应从______(选填“a”或“b”)端通入。
(4)某些大理石中含少量硫化物,使制得的CO2中混有H2S等气体。欲获取纯净、干燥的CO2,设计实验如下:
查阅资料:I.H2S能与NaOH、CuSO4等物质反应。
Ⅱ.CO2中混有的HC1气体可用饱和NaHCO3溶液吸收。
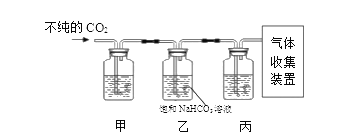
①装置甲中所盛试剂应选用____________(填字母)。
a.浓硫酸 b.NaOH溶液 c.澄清石灰水 d.CuSO4溶液
②装置丙的作用是____________。
参考答案:
【答案】 长颈漏斗 A 2KClO3![]() 2KCl+3O2↑ 催化 2H2O2
2KCl+3O2↑ 催化 2H2O2![]() 2H2O+O2↑ 能够控制反应的进行与停止 a d 干燥CO2或除去水蒸气
2H2O+O2↑ 能够控制反应的进行与停止 a d 干燥CO2或除去水蒸气
【解析】本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的除杂等,综合性比较强。气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关。
(1)仪器②的名称是长颈漏斗;
(2)用氯酸钾和二氧化锰制氧气需要加热,发生装置选用A,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,化学方程式是:2KClO3 ![]() 2KCl+3O2↑;其中二氧化锰起催化作用;若用B和D组合制取氧气,是用过氧化氢与二氧化锰混合生成氧气和水反应的化学方程式为2H2O2
2KCl+3O2↑;其中二氧化锰起催化作用;若用B和D组合制取氧气,是用过氧化氢与二氧化锰混合生成氧气和水反应的化学方程式为2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(3)C装置相对于B的优点有:控制反应的发生和停止;氢气的密度比空气小,用E装置收集H2,气体应从a端通入;
(4)①装置甲中所盛试剂是为除去H2S,浓硫酸不能除去H2S,不能选用,NaOH溶液和澄清石灰水都能与二氧化碳反应不能选用,CuSO4溶液能吸收H2S,不能与二氧化碳反应,能选用,故选D;
②从装置乙中出来的气体中含有水蒸气,欲获取纯净、干燥的CO2,装置丙的作用是干燥CO2或除去水蒸气。
-
科目: 来源: 题型:
查看答案和解析>>【题目】一碳化学是以分子中只含一个碳原子的化合物(如CO2、CH4等)为原料来合成一系列化工原料和燃料的化学。下图为利用合成气(CO和H2)合成新型燃料二甲醚(CH3OCH3)及冶炼铁的部分生产过程。下列有关说法不正确的是:( )
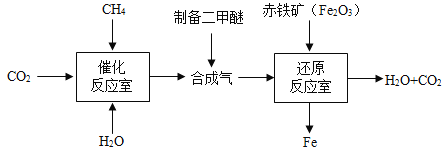
A. 催化反应室中发生的反应有利于减缓温室效应;
B. 还原反应室中发生的反应都属于置换反应
C. 上述生产过程中,可参与循环的物质有水和二氧化碳;
D. 由合成气制二甲醚的反应符合绿色化学的特点(“零排放”,即原子利用率为100%);
-
科目: 来源: 题型:
查看答案和解析>>【题目】写出下列反应的化学方程式,并按要求填空。
(1)工业上用一氧化碳和赤铁矿(主要成分是三氧化二铁)在高温下炼铁:__________。
(2)生石灰作为干燥剂: ____________________,该反应属于_________ (选填“放或吸热”)。
(3)用氢氧化钠溶液吸收少量二氧化硫气体:___________________________________。
(4)用稀硫酸除去铁锈:_____________________,反应后所得溶液的颜色为_________色。
(5)硫酸铵固体和氢氧化钙固体混合研磨:___________,该反应的基本反应类型是_______。
(6)生成沉淀的中和反应:_________________________________,恰好完全反应后液体的导电性比反应前的______ (选填“增强”、“减弱”或“不变”)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】工业上炼铁炼钢和轧制钢材的主要流程如图.
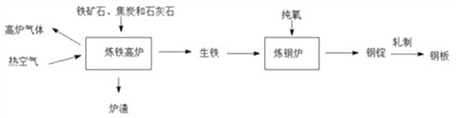
已知生铁的含碳量为 2%--4.3%,钢的含碳量为 0.03%--2%。
(1)反应:①Fe2O3+3CO
 2Fe+3CO2 ,②3C + 2Fe2O3
2Fe+3CO2 ,②3C + 2Fe2O3  4Fe + 3CO2↑。属于置换反应的是_________ ,用于高炉炼铁的原理是 _________(填序号)
4Fe + 3CO2↑。属于置换反应的是_________ ,用于高炉炼铁的原理是 _________(填序号)(2)生铁属于 _________ (填“纯净物”或“混合物”),其熔点比纯铁 _________(填“高”或“低”),铁是由 _________ 构成的物质(填“分子”、“原子”或“离子”)。
(3)炉渣中含有硅酸钙(CaSiO3),其中硅元素的化合价是 _________ 。
(4)将钢锭轧成钢板,属于_________(填“物理变化”或“化学变化”) 。
(5)钢铁制品可能会生锈,写出用稀硫酸除锈反应的化学方程式 _____________________ 。
(6)请用一个化学方程式证明铁的活泼性大于铜 __________________________________ 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某同学对CaH2的制备和性质进行探究。
【阅读资料】①用H2与钙加热制得CaH2 ②钙遇水立即发生剧烈反应生成一种碱和一种气体 ③CaH2要密封保存,遇水反应也生成一种碱和一种气体
【CaH2的制备】设计的制取装置如图所示.
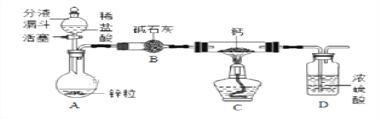
(1)装置B的作用是____________________________;
(2)制备CaH2实验结束后,取少量产物,小心加入水中,观察有气泡产生,在溶液中滴入石蕊试液后显__________色。该同学据此判断:实验中确有氢化钙生成,其他同学提出结论不一定正确,原因是________________________。
【CaH2的性质探究】取少量上述制得的CaH2 样品加入到足量的碳酸钠溶液中,产生大量气泡,过滤,得到滤渣和滤液。经检验滤渣的成分是碳酸钙。该同学进行了如下的探究。
(3)点燃产生的气体,火焰淡蓝色;将燃烧产物通入澄清石灰水中,无现象。则该气体为_________(写化学式)。
(4)对滤液中溶质的成分做出如下猜测并进行实验:
猜想一:NaOH猜想二:NaOH、Ca(OH)2 猜想三:NaOH、Na2CO3 猜想四:NaOH、Na2CO3、Ca(OH)2
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因___________________
【实验验证】
实验
现象
结论
实验一:取滤液,向其中滴入少量 Na2CO3溶液
____________
猜想二不成立
实验二:另取滤液,向其中加入足量稀盐酸
________________
猜想三成立
【定量分析】
取制得的CaH2样品1g(杂质为未反应完的Ca)加入到足量的Na2CO3溶液中,充分反应后,过滤、洗涤、干燥称得CaCO3质量为2.4g,则该样品中CaH2的质量分数为__________(写出计算过程).
-
科目: 来源: 题型:
查看答案和解析>>【题目】小华与朋友聚餐时,对火锅燃料“固体酒精”产生了好奇,于是他与同学对其成分进行如下探究。
【提出问题】固体酒精是固态酒精吗?
【查阅资料一】酒精,学名乙醇,化学式C2H5OH,熔点为-114℃,易挥发,能与水以任意比例互溶。
【交流讨论】小华认为固体酒精不是固态的酒精,他判断的理由是_________,写出酒精完全燃烧的化学方程式________________________________。
【发现问题】小华观察发现,固体酒精完全燃烧后会残留少量白色固体。
【再提问题】燃烧后残留的白色固体是什么?
【查阅资料二】固体酒精是酒精、氢氧化钠和凝固剂按一定的质量比混合制成,该凝固剂在空气中能完全燃烧生成二氧化碳和水。
【作出猜想】猜想一:氢氧化钠;猜想二:碳酸钠;猜想三:__________。你认为猜想中含有碳酸钠的理由是:____________________。(用化学方程式表示)
【实验探究】
步骤
实验操作
实验现象
结论
(1)
将白色固体溶于足量水中
白色固体全部溶解
固体可溶于水
(2)
取(1)所得少量溶液,加入过量的BaCl2溶液
________
白色固体中肯定有Na2CO3
(3)
取(2)所得少量上层清液,加入______________溶液
有蓝色沉淀生成
白色固体中肯定有________
【反思交流】实验中,加入过量氯化钡溶液的目的是____________________________。
如果实验中发现氯化钡溶液不够,可选用下列试剂代替也能达到实验目的是____________。
A.Ca(OH)2溶液 B.Ba(NO3)2溶液 C.稀盐酸 D.CaCl2溶液
-
科目: 来源: 题型:
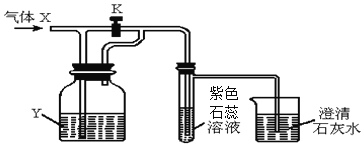
查看答案和解析>>【题目】如图是一套检验气体性质的实验装置,向装置中持续通入气体X,若打开活塞K,只观察到紫色石蕊变红;若关闭活塞K,可观察到紫色石蕊试液变红,澄清石灰水变浑浊。据此判断气体X和洗瓶内的液体Y可能是( )
A
B
C
D
X
二氧化碳
氯化氢
二氧化碳
氯化氢
Y(足量)
水
碳酸钠溶液
氢氧化钠溶液
氢氧化钠溶液
A. A B. B C. C D. D
相关试题

