【题目】实验室用68g过氧化氢溶液和2g二氧化锰制取氧气,实验的相关数据如图。
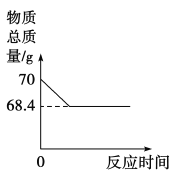
请回答:
(1)二氧化锰作为催化剂在化学反应前后本身的______都没有发生变化;
(2)反应生成氧气的质量为________g。
(3)参加反应过氧化氢溶液的质量分数是____________?
参考答案:
【答案】 质量和化学性质 1.6 5%
【解析】本题考查了催化剂的特点和溶质质量分数与化学方程式相结合的计算。反应过程中质量的减少是因为生成了氧气,所以可以求算氧气的质量,根据氧气的质量和对应的化学方程式求算过氧化氢的质量。
(1)催化剂是在化学反应中能改变化学反应的速率,而本身的质量和化学性质不变的物质,二氧化锰作为催化剂在化学反应前后本身的质量和化学性质都没有发生变化;
(2)根据质量守恒,反应产生氧气的质量=70g-68.4g=1.6g;
(3)设:产生1.6g氧气需要H2O2的质量为x
2H2O2![]() 2H2O+O2↑
2H2O+O2↑
68 32
x 1.6g
![]() x=3.4g
x=3.4g
过氧化氢溶液的溶质质量分数=![]() ×100%=5%。
×100%=5%。
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是甲、乙两种固体物质在水中的溶解度曲线。下列说法正确的是
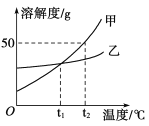
A. t1℃时,甲、乙两种物质的饱和溶液中溶质的质量分数相等
B. 由t2℃降温到t1℃,甲饱和溶液比乙饱和溶液析出晶体的质量多
C. t2℃时,将40g甲物质加入50g水中,充分溶解后溶液的质量为90g
D. t2℃时,用甲、乙配制等质量的饱和溶液,甲所需要水的质量比乙多
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是实验室制取并验证某种气体化学性质的有关装置,据此回答下列问题:
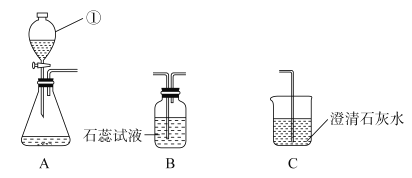
(1)仪器①的名称是_________;
(2)组装好装置A后,必须首先_________。
(3)若A与C连接,C中澄清的石灰水变浑浊,则实验室制取该气体的化学方程式是__________,用_________法收集该气体。
(4)若A与B连接,则B中紫色石蕊试液变_______色。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化学学习小组的同学对一瓶敞口放置氢氧化钙固体的化学成分产生了兴趣,他们根据自己所学知识进行如下探究:
[提出问题]该瓶药品的化学成分是什么?
[查阅资料](1)氢氧化钙能与空气中的二氧化碳反应而变质。
(2)氢氧化钙的溶解度曲线如图:
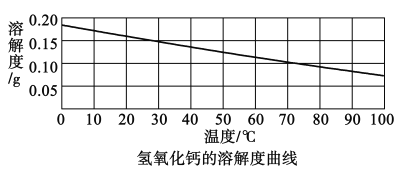
[猜想假设]猜想一:Ca(OH)2
猜想二:__________
猜想三:CaCO3
[实验验证]
实验操作
实验现象
实验结论
(1)取1g样品放入盛有50g水的烧杯中,充分搅拌后,静置
烧杯底部有较多固体未溶解
样品中含有CaCO3
(2)取实验(1)中上层清液少许于试管中,再向试管中滴加2~3滴无色酚酞试液
_____________
样品中含有Ca(OH)2
[得出结论]甲同学认为猜想二正确。
[反思交流]
(1)乙同学认为甲同学的结论不合理,他认为猜想_____也可能正确,原因是______。
(2)丙同学认为要想验证猜想二正确,还需做如下实验:取实验(1)中未溶解固体于试管中,向试管中滴加适量稀盐酸,如有_______,则猜想二正确。
[拓展提升]要想验证反应后物质的成分,除需验证有生成物以外,还应考虑反应物是否________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】向盛有20g10%氢氧化钠溶液的烧杯中逐滴滴入7.3%的稀盐酸,下列是关于溶液总质量或溶液pH随盐酸质量变化的关系图(Q点表示恰好完全反应)。其中正确的是
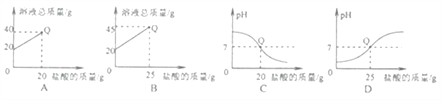
A. A B. B C. C D. D
-
科目: 来源: 题型:
查看答案和解析>>【题目】丁酸乙酯是无色有菠萝香味的液体,其密度为0.87g/cm3,难溶于水,可与油类互溶。现取11.6g丁酸乙酯在氧气中完全燃烧,只产生26.4gCO2和10.8gH2O。
(1)含有丁酸乙酯的物品应远离火源。若丁酸乙酯燃烧,____ (填“能”或不能”)用水来灭火。
(2)丁酸乙酯可与油类互溶,这种性质属于______性质。
(3)丁酸乙酯中碳元素和氢元素的质量比为______。
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是铁、盐酸、氢氧化钙、硫酸铜和氯化镁五种物质的反应与转化关系,“—”表示两种物质之间能发生化学反应,“→”表示在一定条件下的物质转化。
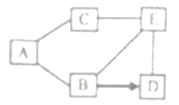
(1)A物质是________(填化学式)。
(2)C与E反应的基本类型是________。
(3)从物质反应规律分析,在单质、氧化物、酸、碱和盐中,能与B反应生成D的物质有________(填序号)。
①2类 ②3类 ③4类 ④5类
相关试题

