【题目】在用稀盐酸和氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如图所示.
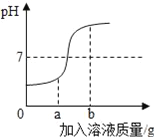
(1)该反应的化学方程式为:__.该反应属于_________反应(填基本反应类型)。
(2)该实验操作是将__滴加到另一种溶液中.
(3)当加入溶液的质量为ag时,所得溶液中的溶质为(写化学式)__.
(4)当加入溶液的质量为bg时,向所得溶液中滴加酚酞溶液,溶液呈__色.
参考答案:
【答案】NaOH+HCl=NaCl+H2O 复分解反应 氢氧化钠 HCl和NaCl 红
【解析】
(1)氢氧化钠与盐酸反应生成氯化钠和水,故化学方程式写为NaOH+HCl=NaCl+H2O;
氢氧化钠与盐酸反应生成氯化钠和水是两种化合物交换成分生成另外两种化合物,基本反应类型属于复分解反应,故填复分解反应。
(2)由图可知,随着溶液的加入,溶液的pH逐渐增大,可以判断实验是将氢氧化钠溶液滴加到稀盐酸中,故填氢氧化钠。
(3)由图可知,当加入溶液的质量为ag时,溶液呈酸性,表明溶液中有盐酸剩余,所以溶液中的溶质应该有剩余的盐酸和反应生成的氯化钠,化学式分别是HCl和NaCl,故填HCl和NaCl。
(4)由图可知,当加入溶液的质量为bg时,溶液呈碱性,向所得溶液中滴加酚酞溶液,碱性溶液使酚酞变红,故填红。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据如图所示的溶解度曲线,下列叙述正确的是
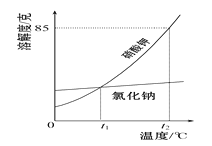
A. 硝酸钾的溶解度比氯化钠大
B. t1 ℃时,氯化钠和硝酸钾的溶解度相等
C. t2 ℃时,85克硝酸钾溶于50克水中得到135g饱和溶液
D. t1 ℃硝酸钾的饱和溶液温度升高到t2 ℃,溶液质量分数增大
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图表示化学反应中溶液的颜色变化。下列叙述错误的是
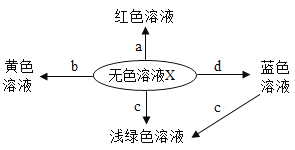
A. 若X是稀硫酸,a可能是紫色石蕊试液 B. 若X是稀硫酸,b可能是氧化物
C. 若X是稀盐酸,c不可能是单质 D. 若X是稀盐酸,d不可能是单质
-
科目: 来源: 题型:
查看答案和解析>>【题目】铁是自然界里分布最广的金属元素之一,在地壳中的质量约占5%左右。铁矿石的种类很多,重要的有磁铁矿石(主要成分是Fe3O4)、赤铁矿石(主要成分是Fe2O3)等。
(1)写出用赤铁矿石炼铁的化学反应式: _____________;
(2)细铁丝在氧气中燃烧,有关化学方程式为_________________;现象为___________。
(3)最近科学家冶炼出了纯度高达99.9999%的铁,你估计它不会具有的性质是________
A.硬度比生铁低 B.在潮湿的空气中放置不易生锈
C.能与硫酸铜反应 D.能与稀盐酸反应
-
科目: 来源: 题型:
查看答案和解析>>【题目】用正确的化学用语填空
(1)2H________;(2)地壳中含量最多的金属元素是_________;
(3)硫酸根离子___________ ;(4)氧化铁中铁元素的化合价为+3价 ___________ 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图所示A、B、C、D、E是五种粒子的结构示意图,根据图示提供的信息,回答相关问题;
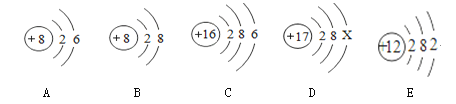
①A、B、C、D、E五种粒子中,属于同种元素的粒子是 ______ ;
②D中X的值可能是 ______ ;
③E在化学反应中易 ______ 最外层电子(填“得到”或“失去”);
④写出D和E两种微粒组成化合物的化学式 ______ 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室用溶质质量分数为10%氢氧化钠溶液进行水的电解实验。
配制溶质质量分数为10%氢氧化钠溶液100g。
(1)所需的氢氧化钠质量______g;需要水的质量__________,体积为________mL(水的密度为1g/cm3)。
(2)称量时,氢氧化钠固体应放于天平_____(填“左”或“右”)盘的烧杯内;量取所需要的水,应选择的量筒的规格是_______mL(选填“10”、“100”或“250”)。
(3)配制的操作如下图,正确操作顺序为________(填字母);
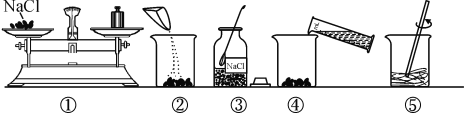
A.③①②④⑤ B.①③④②⑤ C.③①④②⑤ D.①④③②⑤
(4)下列错误操作可能导致溶液溶质质量分数偏大的是______ (填序号)。
①操作中砝码和食盐放置颠倒 ②食盐中混有少量不溶性杂质 ③量取水时俯视量筒读数 ④装瓶时有部分溶液洒落到瓶外 ⑤溶解食盐的烧杯内壁有水
相关试题

