【题目】根据下列装置图,回答有关问题.


①写出仪器名称:a .
②用化学方程式表示实验室用石灰石和稀盐酸制取CO2的原理是 .取用块状石灰石的仪器是 (填编号). 上述可制CO2的实验装置是 (填编号).使用装置C的优点是 .
参考答案:
【答案】①锥形瓶 ②CaCO3+2HCl→CaCl2+ H2O+ CO2↑ Ⅲ A、B、C 随用随开,随关随停
【解析】
试题分析:①常见仪器的识记:锥形瓶
②石灰石和稀盐酸制取CO2的原理是:CaCO3+2HCl→CaCl2+ H2O+ CO2↑;实验室取用块状石灰石的仪器是镊子,选Ⅲ;气体发生装置的选择依据:反应物的状态和反应条件,制CO2属于固液常温型,所以实验装置是A、B、C都可以;使用装置C的优点是:可以通过控制活塞的开关,达到控制装置内的压强发生改变,从而控制反应随用随开,随关随停
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质的用途既利用了物质的物理性质,又利用了物质的化学性质的是
A.用干冰作制冷剂 B.用二氧化碳作灭火剂
C.医疗上用氧气抢救病人 D.用氢气填充气球
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列说法正确的是
A.将带火星的木条伸入集气瓶中,用来检验氧气是否收满
B.石蜡燃烧的过程中一定发生物理变化
C.用燃烧的方法除去密闭容器中空气里的氧气得到较纯净的氮气,可选用硫粉
D.催化剂增大了反应速率,但不能改变生成物的质量
-
科目: 来源: 题型:
查看答案和解析>>【题目】某兴趣小组欲探究Fe、Cu、Ag、R四种金属的活动性顺序(R为未知金属),进行了如下实验:

①图1所示,将金属丝同时插入烧杯中.乙中可观察到的现象是铁丝表面产生 .
②反应一段时间后,把烧杯中铁丝替换为R继续实验,如图2所示.若甲中出现气泡,乙中无明显现象,则此时烧杯乙中的溶质是 ,可得出Fe、Cu、Ag、R的活动性顺序由强到弱为 .
③根据整个实验观察得到的现象,可以推测甲烧杯中X溶液可能是 .
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是某密闭容器中物质变化过程的微观示意图:
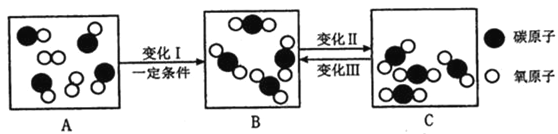
(1)A、B、C中表示混合物的是________.
(2)上述变化I、Ⅱ和Ⅲ中,厲于化学变化的是________,该化学变化中一定不变的粒子是________(填粒子名称).
(3)A图中“
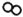 ”表示构成氧气的粒子,氧气的化学性质比较活泼,铁可以在纯净的氧气中燃烧,其燃烧的现象为________,若实验室采用分解过氧化氢的方法制取氧气,其化学方程式为________。
”表示构成氧气的粒子,氧气的化学性质比较活泼,铁可以在纯净的氧气中燃烧,其燃烧的现象为________,若实验室采用分解过氧化氢的方法制取氧气,其化学方程式为________。 -
科目: 来源: 题型:
查看答案和解析>>【题目】如图A~D是四种粒子的结构示意图,E是铈元素在元素周期表中的信息:
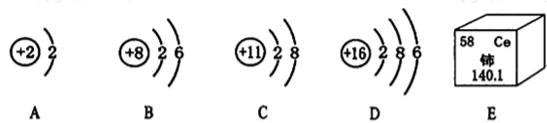
(1)在A~D中,化学性质相似的原子是_________(填字母);
(2)在A~D中,位于同一周期的元素是_________(填字母);
(3)在A~D中,具有相对稳定结构的粒子是_________(填化学符号);
(4)铈的相对原子质量为_________.
-
科目: 来源: 题型:
查看答案和解析>>【题目】叠氮化钠(NaN3)被广泛应用于汽车安全气囊,某化学小组同学对其进行下列研究.
【査阅资料】
①NaN3受撞击会生成Na、N2
②NaN3遇盐酸、H2SO4溶液无气体生成
③碱石灰是CaO和NaOH的混合物
④NaN3的制备方法是:将金属钠与液态氨反应制得NaNH2,再将NaNH2与N2O反应可生成NaN3、NaOH和NH3
【问题探究】
(1)汽车受撞击后,30毫秒内引发NaN3迅速分解,该反应的化学方程式为___________;
(2)工业级NaN3中常含有少量的Na2CO3,其原因是___________(用化学方程式表示);
(3)为测定某工业级NaN3样品中Na2CO3的质量分数,小组同学设计了如图实验装罝:

①小明同学认为通过测定装置I中反应前后B的质量差,再通过相应计算,就可测定Na2CO3的质量分数,小组同学通过讨论认为不可行,其理由可能是___________(答出一种即可)
②小明同学在大家讨论的基础上,又设计了装罝Ⅱ,请分析:装置Ⅱ中A的作用是___________.若无装置C,对测定结果造成的影响是 (填“偏大”、“偏小”或“无影响”).装置E的作用是___________.
③根据装置Ⅱ,小组同学设计的实验步骤有:
a.称量装置D
b.称量样品,检査装置气密性
c.打开弹簧夹,鼓入空气
d.关闭弹簧夹,打开分液漏斗的活塞和玻璃塞,注入足量的稀琉酸,关闭活塞和玻璃塞.
其正确的顺序为___________(填字母序号,可重复)
④计算碳酸钠的质量分数时,至少需要测定___________个数据.(填数字)
相关试题

