【题目】实验室常用加热氯酸钾和二氧化锰混合物的方法制取氧气,写出反应的文字或符号表达式: 。
小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂。
【完成实验】按下表进行分析:测定分解温度(分解温度越低,催化效果越好)。
实验编号 | 实验药品 | 分解温度(℃) |
① | 氯酸钾 | 580 |
② | 氯酸钾、二氧化锰(质量比1:1) | 未测 |
③ | 氯酸钾、氧化铜(质量比l:1) | 370 |
④ | 氯酸钾、氧化铁(质量比1:1) | 390 |
【分析数据、得出结论】
(1)由实验_____________与实验④对比,证明猜想合理。
(2)已知实验所用的三种物质中,催化效果最好的是二氧化锰,则实验②的分解温度 370(填“>”、“=”或“<”)。
【反思】
(1)若要证明氧化铁是该反应的催化剂,还要验证它在化学反应前后质量和 不变;
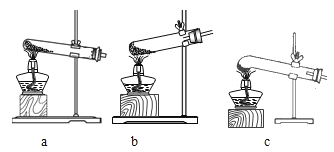
(2)已知氯酸钾的熔点为356℃,结合上表数据,你认为加热氯酸钾和氧化铁的混合物制氧气最适宜的装置是 (填字母)
(3)同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证
参考答案:
【答案】KClO3 ![]() KCl + O2
KCl + O2
[分析数据、得出结论]
(1)① (2)<
[反思]
(1)化学性质 (2)c
(3)将氯酸钾与不同颗粒大小的同种催化剂按质量比1:1混合,加热,分别测定分解温度。
【解析】
试题分析:加热氯酸钾生成的是氯化钾和氧气:KClO3![]() KCl + O2;
KCl + O2;
[分析数据、得出结论]
(1)由实验①和实验④对比可知,加入氧化铁后分解氯酸钾的温度更低了,说明猜想合理;
(2)二氧化锰的催化效果最好,即分解温度最低,那么实验②的分解温度<370;
[反思](1)催化剂具有“一变二不变”的特点,即能改变物质的反应速率,但自身的质量和化学性质不变,故要证明氧化铁是该反应的催化剂,还要验证它在化学反应前后质量和化学中不变;
(2)氯酸钾是固体,为防止试管破裂,那么试管口要略向下倾斜;由因为氯酸钾的熔点为356℃,故用c装置;
(3)要探究颗粒大小比催化效果的影响,那么要采用控制变量法来探究,即可将氯酸钾与不同颗粒大小的同种催化剂按质量比1:1混合,加热,分别测定分解温度。
-
科目: 来源: 题型:
查看答案和解析>>【题目】河水净化的主要步骤如下图所示.请根据图示回答下列问题:

(1)步骤Ⅰ过滤操作过程中用到的玻璃仪器有漏斗、玻璃棒和 ,其中玻璃棒的作用是 。
(2)步骤Ⅱ中的物质X是 。(填物质名称)
(3)步骤Ⅲ中加入液氯会影响水质,现在使用一种新型净水剂铁酸钠,化学式为Na3FeO4,其中铁元素的化合价为 。
(4)通常经过上述步骤获得的“净化的水”仍是硬水,生活中可降低水的硬度的方法是 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列各组物质用稀硫酸不能完全区分开的是
A.铝片、铁片、银片
B.镁粉、氧化铜粉、木炭粉
C.Na2CO3溶液、NaCl溶液、BaCl2溶液
D.NaOH溶液、Ba(OH)2溶液、KOH溶液
-
科目: 来源: 题型:
查看答案和解析>>【题目】新发布的《环境空气质量标准》中增加了PM2.5监测指标。PM2.5是指大气中直径小于或等于2.5微米的颗粒物,对人体健康影响很大,主要来源之一是化石燃料的燃烧。下列措施能减少PM2.5污染的是
A.鼓励开私家车出行 B.鼓励使用太阳能热水器
C.鼓励用煤火力发电 D.鼓励用液化石油气作燃料
-
科目: 来源: 题型:
查看答案和解析>>【题目】氧气是一种化学性质比较活泼的气体,它可以和许多物质发生反应。
(1)下图甲、乙、丙分别是木炭、硫粉和细铁丝在空气中和氧气中的反应。

①分别写出甲图(木炭燃烧)和乙(硫粉燃烧)在氧气中燃烧的文字表达式:
甲: ;乙: ;
②硫在氧气中燃烧的现象是:发出 火焰,生成有刺激性气味的气体并放出大量的热。
③、上述集气瓶中发生的三个反应的相同点是 (多选,填序号)。
A.生成物都是气体
B.都是氧化反应
C.生成物都只有一种物质
D.都需要点燃
E.反应时需要快速伸到瓶底
F.都属于分解反应
(2)下图是同学们构建的关于氧气的部分知识网络,请你由图回答
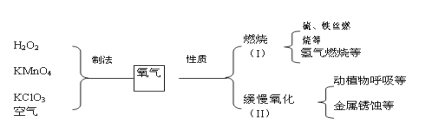
①燃烧前丙瓶内的铁丝前,通常要将铁丝表面打磨、绕成螺旋状并插入一根燃着火柴梗用于 铁丝。
②下列变化中不属于缓慢氧化的是( )
A.食物腐败 B.钢铁生锈 C.牛奶变酸 D.燃放烟花
③用 制取氧气的途径发生的是物理变化。
-
科目: 来源: 题型:
查看答案和解析>>【题目】有A、B、C、D、E、F六种物质,暗紫色的固体A受热会产生一种是带火星木条复燃的气体B,黑色固体C在B中燃烧,发出白光,生成使澄清石灰水变浑浊的气体D,银白色金属E在B中剧烈燃烧,火星四射,生成黑色固体F。
(1)写出各物质的名称或符号:A ,B ,D
(2)写出E在B中燃烧的文字或符号表达式 ;
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究.
已知:在空气中,温度超过40℃,白磷(化学符号为P)就可以燃烧,与氧气反应生成五氧化二磷。
如图是“空气中氧气体积分数测定”实验的改进装置.主要操作是:在实际容积为200mL的集气瓶里,先装进50mL的水,再按图连好仪器,按下热的玻璃棒,白磷立即被点燃.
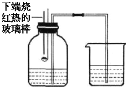
(1)请写出白磷与氧气反应的文字或符号表达式
(2)白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是 ;若实验非常成功,最终集气瓶中水的体积约为 mL.
(3)集气瓶里预先装进的50mL水,在实验过程中起到的作用是 (填序号)
a.加快集气瓶冷却
b.液封导气管末端以防气体逸出
c.缓冲集气瓶内气压的骤然升高.
(4)下列对该实验的认识中正确的是_____________________.
A.白磷燃烧产生大量白色烟雾
B.燃烧匙中的白磷可以换成细铁丝
C.该实验可以说明氮气难溶于水
D.白磷的量不足会导致进入集气瓶中水的体积小于1/5.
(5)该实验的结论是
相关试题

