【题目】空气和水是重要的自然资源。
(1)下列物质不属于空气污染物的是_____,能形成硫酸型酸雨的是______。
A.CO2 B.SO2 C.NOX D.CO
(2)下列能溶于水形成溶液的是______,溶于水pH>7的是______。
A.食用油 B.面粉 C.蔗糖 D.纯碱
(3)如图是实验室电解水实验的装置图,a试管中产生的气体为_____,水中加入少量氢氧化钠的目的是_______。
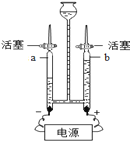
(4)生活中,常用____鉴别硬水和软水。
(5)水常用于灭火,其灭火主要原理是______。
参考答案:
【答案】 A B CD D H2 增强水的导电性 肥皂水 降低温度至可燃物着火点以下
【解析】(1)属于空气污染物的是粉尘、二氧化硫、氮氧化合物等,各选项中只有二氧化碳不属于空气污染物。其中二氧化硫、氮氧化合物溶于水,与水反应形成酸,形成酸雨,能形成硫酸型酸雨的是二氧化硫;
(2)A、食用油不溶于水,与水混合形成的是乳浊液,不均一、不稳定;
B、面粉不易溶于水,与水混合形成的是悬浊液,不均一、不稳定;
C、蔗糖易溶于水,形成均一、稳定的混合物,但是其水溶液显中性,pH小于7;
D、纯碱易溶于水,形成均一、稳定的混合物,其水溶液显碱性,pH大于7;
(3)a试管中产生的气体多,与电源负极相连,为氢气;
电解水实验中在水中加入少量氢氧化钠的目的是增强水的导电性;
(4)向水中加入肥皂水时,如果产生的泡沫较多,是软水,如果产生大量浮渣,是硬水,因此利用肥皂水可以区分硬水和软水;
(5)水常用于灭火,其灭火原理是降温至着火点以下。
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学用语是学习化学的重要工具。
(1)用化学符号表示
①两个硝酸根离子__②五个氨分子__
③三个铝原子__④两个亚铁离子____
(2)请从①活性炭 ②聚乙烯 ③熟石灰 ④氧气 中选择适当物质,用其序号填空:
①可用于改良酸性土壤的是____ ;②可用于急救病人的是____;
③能吸附水中色素和异味的是____ ;④可做食品包装袋的是____。
(3)写出下列反应的化学方程式:
①稀盐酸除铁锈________②实验室用过氧化氢制氧气_____
③镁条在氧气中燃烧_______④曾青得铁化为铜_____
-
科目: 来源: 题型:
查看答案和解析>>【题目】3月22日是"世界水日"。下列有关水的叙述正确的是( )
A. 随意丢弃废电池易造成水土重金属污染
B. 经常饮用蒸馏水对身体有益
C. 水中Ca2+、Mg2+增多导致水体富营养化
D. 大量使用农药、化肥不会污染水
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学与生活密切相关。
Ⅰ.小明妈妈准备露营的食物。
(1)下列食物中富含糖类的是______(填序号)。
A. 青菜 B. 鱼肉 C. 牛奶 D. 大米
(2)牛奶中还含有维持人体正常生理功能所必需的磷、硒、钙、钠、镁、铁、锌、铜、锰、钾等元素,其中能够防止人体骨质疏松的元素是 ____(填元素符号)。
Ⅱ.小明一家与朋友们决定使用“共享汽车”出行。
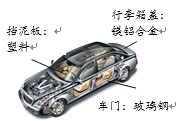
(1)①“共享汽车”中属于金属材料的是____(填材料名称,下同),属于合成材料的是____,属于复合材料的是____。
②将镁铝合金与铝片相互刻画,在铝片表面留下明显划痕,说明镁铝合金的硬度____铝的硬度(填“大于”或“小于”)。
(2)使用“共享汽车”出行出行的好处有______(填序号)
A.降低出行成本 B.减少汽车尾气排放 C.节约能源 D.降低交通压力
(3)“共享汽车”使用天然气作为燃料。“天然气水合物”即为“可燃冰”,它是在海底的高压、低温条件下形成的,外观像冰。1体积“可燃冰”可贮载100~200体积的天然气。下面关于“可燃冰”的叙述不正确的是______(填序号)
A.“可燃冰”有可能成为人类未来的重要能源 B.“可燃冰”是一种比较洁净的能源
C.“可燃冰”提供了水可能变成油的例证 D.“可燃冰”的主要可燃成分是甲烷
-
科目: 来源: 题型:
查看答案和解析>>【题目】果糖大量存在于水果中,其分子的化学式为C6H12O6 ,下列说法不正确的是( )
A.果糖由碳、氢、氧元素组成
B.果糖由果糖分子构成
C.果糖中碳、氢、氧元素质量比1:2:1
D.1个果糖分子有6个碳原子、12个氢原子、6个氧原子构成
-
科目: 来源: 题型:
查看答案和解析>>【题目】工业废料石膏(CaSO42H2O)可以“变废为宝”,用于生产氧化钙、硫酸钾、电石(化学名称为碳化钙)等。某研究性学习小组展开了如下系列研究。
一、高纯CaO的制备
【资料一】
Ⅰ.石膏(CaSO42H2O)与碳粉高温煅烧生成氧化钙和几种气态非金属氧化物。
Ⅱ.SO2能使品红溶液褪色,也能使澄清石灰水变浑浊。
甲同学用如图1装置制备CaO并验证石膏与焦炭高温反应的其他产物。
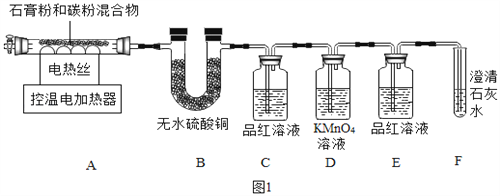
实验过程中发现:B中无水硫酸铜变蓝;C中产生__现象证明有SO2生成;装置__中无明显变化和装置F中__现象证明有CO2生成。写出石膏与碳粉在高温条件下反应的化学方程式:____。
二、硫酸钾和电石的制备
乙同学模拟生产化肥硫酸钾和电石的流程如图2:
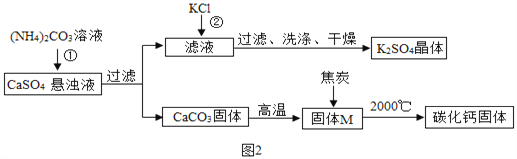
【资料二】CaO与C在高温下反应生成碳化钙(化学式为CaCx)和CO。
(1)反应①的化学方程式为___。证明固体M中不含CaCO3的方法是____(写出实验的方法、现象)。
(2)反应②的化学方程式为(NH4)2SO4+2KCl═K2SO4↓+2NH4Cl,该反应能析出K2SO4晶体的原因是__。
三、假设上述流程中制得的碳化钙(化学式为CaCx)固体中只含杂质CaO,乙小组同学为测定CaCx中x的值进行如下实验。
【资料三】CaCx在空气中灼烧生成CaO和CO2。
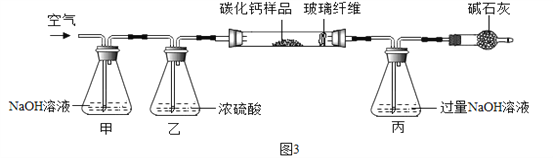
步骤一:称取3.76g样品于图3所示石英管中(测定装置图如图3,夹持及加热装置省略),反应前缓缓通入空气,高温灼烧石英管中的样品至反应完全后继续缓缓通入空气,测得丙溶液的质量比反应前增重了4.4g。(玻璃纤维可防止固体粉末进入导管)
步骤二:将石英管内剩余固体全部转移到水中,加入足量碳酸钠溶液,经搅拌、过滤、洗涤、干燥等操作得到碳酸钙固体6克。试回答下列问题:
(1)装置甲的作用是__。反应完全后继续缓缓通入空气的目的是__。
(2)根据步骤一、二计算该样品中钙、碳、氧的质量比为___,
计算确定CaCx的化学式(请写出计算过程)______________。
(3)若碳酸钙未能完全干燥,则会导致CaCX中的x的值____(填“偏大”、“偏小”、“无影响”)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列依据实验目的所设计的实验方案中,正确的是( )
选项
实验目的
实验方案
A
除去NaCl溶液中的Na2CO3
加适量稀硫酸
B
除去CaO中的CaCO3
加水溶解,过滤
C
除去CO2中的HCl气体
将混合气体通入NaOH溶液
D
除去KNO3溶液中的KCl
加适量的AgNO3溶液,过滤
A. A B. B C. C D. D
相关试题

