【题目】某化学兴趣小组在实验室配制一定溶质质量分数的稀盐酸,并用其测定某氢氧化钠溶液的溶质的质量分数。
实验一:37%的浓盐酸(密度为1.19g/mL)、氢氧化钠溶液、蒸馏水、量筒、细口瓶等
实验步骤:
(1)计算:配制74g质量分数为10%的稀盐酸,需要37%的浓盐酸的体积为 mL(精确到0.1mL,下同);需要蒸馏水的体积为 mL(水的密度为1.0g/mL)。

(2)量取:用量筒分别量取相应的浓盐酸和蒸馏水。
(3) 。
(4)装瓶并贴上标签。
实验二:用上述配制的稀盐酸加入到20g某氢氧化钠溶液中,溶液pH的变化情况如右图所示。试计算该氢氧化钠溶液中溶质的质量分数。 (在答题卡上写出计算过程)
参考答案:
【答案】实验步骤:(1)16.8 54.0 (3) 混和均匀 (4)20%
【解析】
试题分析:配制74g质量分数为10%的稀盐酸,需要37%的浓盐酸的体积为X,则74克×10%=X×1.19g/mL×37%,解得X=16.8ml,需要蒸馏水的体积为74mL-16.8ml×1.19g/mL=54ml。量取:用量筒分别量取相应的浓盐酸和蒸馏水,然后混合均匀即成为要配制的溶液。
解:设参加反应的氢氧化钠溶液中溶质的质量为x。
NaOH + HCl = NaCl + H2O
0 36.5
x 36.5 g×10%
40:36.5= x:36.5 g×10%
x = 4g
氢氧化钠溶液中溶质的质量分数为4g/20g×100%=20%
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图是甲、乙两位同学一起在实验室进行的氢氧化钠与盐酸中和反应的实验。
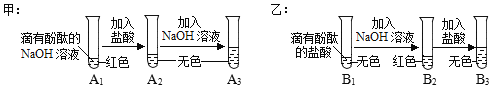
(说明:图中A1、A2、A3、B1、B2、B3均为溶液编号)
根据上图实验,请你与甲、乙同学一起完成下列探究:
探究环节
甲同学的探究
乙同学的探究
提出问题
A3溶液为什么不变红?
B3溶液中溶质成分是什么?(酚酞不计)
作出猜想
实验过程中,酚酞变质了。
猜想一:NaCl 猜想二:NaCl、HCl
实验验证
(1)取少量A3溶液于另一试管中,向其中滴加NaOH溶液,溶液变红,说明甲同学的猜想 (填“成立”或“不成立”)。
(2)你认为,在常温下A2溶液测出的pH应 (填“>”、“=”或“<”)7。取少量B3溶液加入盛有少量铁粉的试管中,观察到有无色气泡产生,固体逐渐减少,溶液由无色变为 。据此,你认为乙同学的猜想 (填“一”或“二”)成立。
交流反思
(1)甲、乙同学的实验中,反应均涉及到的化学方程式是 。
(2)A3溶液未变红,你认为原因是A2溶液中 较多,加入的NaOH溶液未将其完全中和。
(3)甲、乙同学经过实验对比探究,一致认为做化学实验时应注意药品用量的控制。 -
科目: 来源: 题型:
查看答案和解析>>【题目】擦玻璃时,人们时常向玻璃“哈气”,再擦会使玻璃擦得更干净。这说明与空气相比,人体呼出气体中含有较多的
A、CO2 B、 N2 C、H2O D、O2
-
科目: 来源: 题型:
查看答案和解析>>【题目】从分子的角度分析并解释下列事实,说法不正确的是( )
事实
解释
A
碘酒是混合物
由不同分子构成
B
八月桂花香
分子在不停运动
C
气体受热膨胀
温度升高,分子自身体积增大
D
碘受热升华
分子间间隔增大
A. A B. B C. C D. D
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列各选项与下图所示曲线相符的是

选项
横坐标
纵坐标
A
向一定量稀硫酸中加入锌粉的质量
溶液中氢元素的质量
B
向一定量的氢氧化钠和碳酸钠混合溶液中加入稀盐酸的质量
产生气体的质量
C
向一定量的澄清石灰水中加入碳酸钠溶液的质量
生成沉淀的质量
D
在一定温度下,向一定量的不饱和硝酸钾溶液中加入硝酸钾固体的质量
溶液中溶质的质量分数
A. A B. B C. C D. D
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图所示的四个图像,能正确反映对应变化关系的是

A. 水的电解
B. 木炭在密闭的容器内燃烧
C. 加热一定量的高锰酸钾制氧气
D. 等质量的氯酸钾在有无二氧化锰条件下加热
-
科目: 来源: 题型:
查看答案和解析>>【题目】在某无色溶液中,能大量共存的是( )
A. Na+,Fe2+,NO3﹣Cl﹣ B. Na+,K+,NO3﹣,CO32﹣
C. Ba2+,K+,SO42﹣Cl﹣ D. H+,K+,OH﹣,SO42﹣
相关试题

