【题目】请结合下列实验常用装置,回答有关问题:
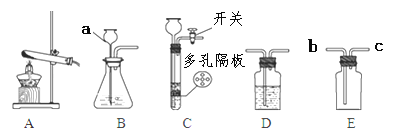
(1)写出有关标号仪器的名称a
(2)实验室制取CO2的方程式为 ,若要获得干燥的二氧化碳,还应选用D装置,并在该装置中盛放 (填写试剂名称)。如果用E装置收集该气体,则气体从 端进入(填“b”或“c”)。
(3)实验室若用块状固体和液体无需加热制取气体,可将B装置改进为C装置(多孔隔板用来放块状固体),其改进后的优点是 。
(4)工业上以氨气为原料制备硝酸的过程(见图1)如下:
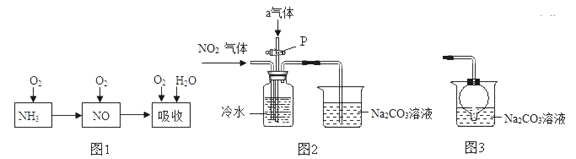
某课外小组认真分析了工业制取硝酸的流程及反应原理,设计了如图2的实验装置制备硝酸,试回答下列相关问题:
①完成图1工业上用氨气制取NO的化学方程式:4NH3+5O2═4NO+6 ;然后产生的NO被氧气氧化成NO2;NO2和水反应生成硝酸和NO。
②连接好图2装置后,首先进行的操作是 。
③图2中通入的气体a是 ,其目的是 。
④盛有Na2CO3溶液的烧杯作为尾气处理装置有点缺陷,某兴趣小组把图2右边装置改进成如图3的装置,这样改进的优点是 。
参考答案:
【答案】(1)长颈漏斗(2)CaCO3+2HCl=CaCl2+H2O+CO2↑ 浓硫酸 、 b
(3)控制反应的发生与停止(4)①H2O;②检查装置的气密性。
③氧气、提高NO2的转化率。④防止倒吸或者充分吸收有害气体 。
【解析】试题分析:(2)实验室制取CO2常用碳酸钙和稀盐酸即方程式 CaCO3+2HCl=CaCl2+H2O+CO2↑,用浓硫酸干燥;CO2的密度比空气大,应从b进入。(3)控制反应的发生与停止
(4)依据质量守恒定律为① H2O ; ②连接好图2装置后,首先进行的操作是检查装置的气密性。
③图2中通入的气体a是氧气,其目的是提高NO2的转化率;④改进的优点是防止倒吸或者充分吸收有害气体
-
科目: 来源: 题型:
查看答案和解析>>【题目】【2016年山西省】世界上物质多种多样,下列物质属于氧化物的是( )
A.葡萄糖 B.液氧 C.氯酸钾 D.一氧化碳
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室有一瓶长期放置的氢氧化钠固体,某兴趣小组同学欲对该固体变质情况进行探究。
Ⅰ 固体的成分分析
【提出问题】该瓶氢氧化钠固体是否变质,变质情况如何?
【查阅资料】
①氢氧化钠在空气中容易变质但不会转化为NaHCO3;
②CaCl2溶液的pH=7,碳酸钠溶液的pH7
③CaCl2+Na2CO3═CaCO3↓+2NaCl
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
④碱石灰是CaO和NaOH的混合物
【提出猜想】
猜想Ⅰ:固体未变质
猜想Ⅱ:固体全部变质
猜想Ⅲ:固体部分变质
【原因分析】氢氧化钠在空气中变质的原因是___________(用化学方程式表示)。
【进行实验】小聪同学取少量样品于烧杯中,用足量水溶解,再向溶液中滴入几滴酚酞试液,溶液变红,由此他得出猜想Ⅰ正确,但其他同学很快予以否定,否定的理由是____,为了进一步得出结论,组内其他三位同学分别取小聪实验后的溶液于试管中,进行如下表所示实验。
同学
小红
小美
小伍
实验操作
加入适量氢氧化钙溶液
加入过量氯化钙溶液
加入过量稀硫酸
【实验结论】小红、小美的实验中都观察到有白色沉淀生成且溶液仍是红色,于是他们都得出猜想Ⅲ正确。
【反思评价】(一)老师指出,仅凭小红的实验操作和现象无法确定猜想Ⅲ正确,理由是_____________________。
(二)根据小美的结论推测小伍实验现象是__________________。
Ⅱ 固体中各成分含量
【提出问题】如何测定变质的氢氧化钠固体中碳酸钠的质量分数?
【进行实验】化学小组同学设计了如下实验装置。

①小明同学认为通过测定装置 I中反应前后B的质量差,再通过相应计算,就可测定Na2CO3的纯度,小组内同学通过讨论认为不可以,其理由可能是_______;
②小刚同学在大家讨论的基础上,设计了装置II。请分析:装置II中A的作用_______;若无装置C,对测定结果造成的影响是_______(填“偏大”、“偏小”或“无影响”);
【实验结论】称取10g样品于圆底烧瓶中,实验结束后,测得装置D增重2.2g,请你计算出样品中Na2CO3质量分数。(写出计算过程)____
【反思评价】①联想到空气中有CO2,所以实验室中的氢氧化钠应_____保存。
②若将上述5g氢氧化钠固体全部溶解在45g水中,得到的溶液中氢氧化钠质量分数_______10%(填“大于”、“小于”或“等于”)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学用语是学习化学的重要工具,请用化学符号来表示:
氧化铝 2个二氧化碳分子 3个铁离子
水中氧元素显﹣2价 碳酸根离子
-
科目: 来源: 题型:
查看答案和解析>>【题目】【2016年广东省广州市 】下列事实中,属于物质化学性质的是( )
A.普通玻璃属于易碎品 B.二氧化碳能使澄清石灰水变浑浊
C.金刚石硬度大 D.盛有水和植物油的试管振荡得到乳状浑浊液体
-
科目: 来源: 题型:
查看答案和解析>>【题目】【2016年湖北省黄石市】下列过程属于化学变化的是
A.碘升华 B.铝放置于空气中,表面生成一层致密的薄膜
C.风能发电 D.蒸发蔗糖水溶液得到蔗糖晶体
-
科目: 来源: 题型:
查看答案和解析>>【题目】【2016年广东省 】 根据日常经验和你所学的化学知识,判断下列变化不属于化学变化的是( )
A.酿制甜酒 B.煤炭燃烧 C.瓷器破碎 D.钢铁生锈
相关试题

