【题目】铁制零件在电镀前必须先用稀盐酸除去表面的锈迹,在除锈时会有少量气泡产生,写出有关反应的化学方程式: ,___________________。
参考答案:
【答案】Fe2O3+6HCl==2FeCl3+3H2O;Fe+2HCl==FeCl2+H2↑
【解析】
试题分析:书写化学方程式的依据是质量守恒定律,书写步骤是:一写二配三标四查。
铁锈的主要成分是氧化铁,氧化铁与稀盐酸反应生成氧化铁和水;铁与稀盐酸反应生成的是氯化亚铁和氢气。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列对物质性质的描述中,属于化学性质的是
A.浓盐酸的挥发性 B.活性炭的吸附性
C.浓硫酸的脱水性 D.氢氧化钠易潮解
-
科目: 来源: 题型:
查看答案和解析>>【题目】浓硫酸具有 性,所以可以做某些气体的干燥剂,浓硫酸露置在空气中一段时间后:质量变 浓度变 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某发电厂烟气处理的新工艺:CH4十2NO2=N2+X+2H2O,则X的化学式为
A.CO B.CO2 C.O2 D.C
-
科目: 来源: 题型:
查看答案和解析>>【题目】(11分)医用氯化钙可用于生产补钙、抗过敏和消炎等药物。以工业碳酸钙为原料(含量为97.5%,含有少量Na+、Al3+、Fe3+等杂质)生产医药级二水合氯化钙的主要流程如下:
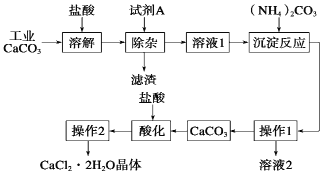
(1)除杂操作时加入试剂A,调节溶液的pH为8.0~8.5,以除去溶液中少量的Al3+、Fe3+。试剂A是Ca(OH)2,还可以选择 。
a.NaOH b.NH3 c.Na2CO3
(2)请指出下列操作的名称:操作1 ;操作2蒸发浓缩、 ;操作1中所用的玻璃仪器有漏斗、玻璃棒、 。
(3)酸化操作是加入过量盐酸,调节溶液的pH为4.0,目的之一是为了将少量的 转化为CaCl2。
(4)写出加入碳酸铵所发生的反应的方程式: +(NH4)2CO3=CaCO3↓+2NH4Cl
写出溶液2的一种用途 。
(5)测定样制得品中Cl-含量的方法是:称1.5g样品,溶解,滴加过量的 AgNO3 溶液,过滤、洗涤、干燥,称得沉淀质量为2.87g,证明沉淀洗净的标准是:取最后一次洗涤的滤液,滴加 试剂,若 现象,则已经洗净。
(6)计算上述样品中CaCl2·2H2O的质量分数为: 。若用上述方法测定的样品中CaCl2·2H2O的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有: 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(13分)某兴趣小组为了探究铁粉与水蒸气反应的产物,做了下面实验。
资料:在不同温度下,铁粉与水蒸气反应的产物不同。
Fe +H2O
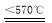 FeO+H2 3Fe + 4H2O
FeO+H2 3Fe + 4H2O Fe3O4 + 4H2
Fe3O4 + 4H2实验一:某兴趣小组用下图所示装置,使铁粉与过量水蒸气充分反应并检验固体产物的组成。

铁粉与水蒸气的反应装置
(1)实验过程中,应先点燃 (选填“酒精灯”或“酒精喷灯”);目的是 ,装置中石棉绒的作用是 。
(2)若在实验中的某段时间内生成H20.04g,则这段时间内参加反应的铁粉质量至少是 g。
实验二:铁粉完全反应后,兴趣小组对硬质玻璃管中生成的FeO和Fe3O4的质量进行测定,实验流程如下图。

(1)实验前如何检查装置A的气密性关闭止水夹K,从长颈漏斗向试管内加水,至长颈漏斗中管内的 液面高于管外液面,静置一段时间,若液面高度差 ,则气密性良好。
(2)装置A中发生的反应方程式 。
(3)为了安全,在点燃酒精灯之前,在F装置出口b处必须 。
(4)装置C中所放试剂为 ,则装置B的作用是 。
(5)干燥管E右边又连接干燥管F的目的是 。
若无干燥管F,测得Fe3O4的质量将 (填“偏大”、“偏小”或“无影响”)。
(6)若FeO和Fe3O4混合物的质量为15.2g,反应完全后干燥管E的质量增加了4.5g,则完全反应后D装置中固体的质量为 g;混合物中Fe3O4的质量为 g。
-
科目: 来源: 题型:
查看答案和解析>>【题目】将二氧化碳通入紫色石蕊试液中,将其溶液加热,冷却后再加入一定量的活性炭、振荡.在这个过程中,液体颜色变化的顺序是
A.紫→红→紫→无 B.紫→红→蓝→无 C.紫→蓝→红→无 D.紫→红→蓝→紫
相关试题

