【题目】(1)化学家道尔顿认为原子是—个简单的、不可分割的实心球体。你认为该观点____(选填“正确”或“不正确”)。
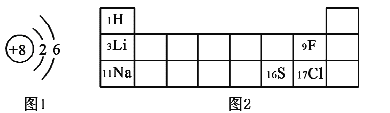
(2)图1表示的粒子名称是_______,
(3)图2是元素周期表的一部分,氯原子的最外层电子数为_______,
(4)16号元素的原子得到电子形成相对稳定结构的离子,该离子与Na+形成化合物的化学式是_______。
参考答案:
【答案】 不正确 氧原子 7 Na2S
【解析】原子是由位于中心的原子核和核外电子构成,电子的质量很小,原子的质量主要集中在原子核上,原子核只占原子体积的几千分之一在原子结构示意图中,小圆圈表示原子核,圆圈内的数字为质子数;弧线表示电子层,弧线上的数字为该层上的电子数。同一原子中,质子数=核外电子数=核电荷数,所以该微粒是氧原子;在元素周期表中电子层数等于周期数,所以氯原子的最外层电子数为3;16号元素为硫元素,得电子时显-2价,化合物的化学式书写:显正价的元素其符号写在左边,显负价的写在右边,化合价的绝对值交叉约减,得化学式右下角的数字,数字为1时不写;所以钠与硫形成化合物的化学式为Na2S;
-
科目: 来源: 题型:
查看答案和解析>>【题目】【2015年福建省厦门市】新装修房室内存在甲醛(CH2O)、苯(C6H6)等有害物质。下列叙述正确的是( )
A.甲醛分子中含有水分子 B.甲醛中碳元素质量分数为40%
C.苯中碳元素与氢元素的质量比为1:1 D.甲醛和苯都属于无机化合物
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列叙述正确的是
A.给玻璃仪器加热时,无需预热,直接加热
B.蒸发时,应该等溶液完全蒸干时停止加热
C.吸液时,应该先将胶头滴管伸入液体中,然后挤出空气,吸取液体
D.洗净的玻璃仪器水膜均匀,既不聚成滴,也不成股流下
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究。
【提出问题】金属与盐酸反应剧烈程度受哪些因素的影响?
【查阅资料】盐酸是由氯化氢和水组成,盐酸的浓度是指氯化氢在盐酸中所占的质量分数。
【作出猜想】a.可能与金属本身的性质有关;b.可能与盐酸的浓度有关。
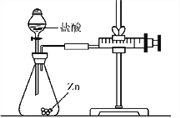
【设计探究】实验所用金属均已用砂纸打磨。
实验(1):为探究猜想a,常温下,小组同学分别在两支试管中放入相同形状、质量相等的锌片和铁片,然后分别加入质量相等、浓度相等的稀盐酸,观察到放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡。请写出放锌片的试
管中发生反应的化学方程式:____。从实验现象可初步判断:金属活动性Zn____Fe(填“<”“=”或“>”)。
【得出结论1】金属与盐酸发生反应的剧烈程度与金属本身性质有关。
实验(2):为探究猜想b,小组同学设计如图的装置进行实验,其中注射器的作用是____________________。
【实验记录】实验数据如下表:
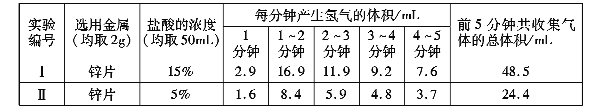
【得出结论2】金属与盐酸发生反应的剧烈程度与盐酸的浓度有关,其关系是________________。
【反思评价】根据表中实验Ⅱ数据分析,请描述锌与盐酸发生反应快慢的变化情况并解释原因_______________________。通过以上探究,你认为金属与盐酸反应的剧烈程度可能还受哪些因素的影响?____________________(写一条即可)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据图示回答问题。

(1)仪器①的名称是____;
(2)实验室制取二氧化碳,反应的化学方程式是____,应选用的发生和收集装置是____(填字母序号);
(3)实验室常用A装置加热氯酸钾和二氧化锰的混合物制取氧气,反应的化学方程式是____,可以用E装置收集氧气的原因是____。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下述实验现象正确的是
A.铁丝在空气中燃烧,火星四射
B.加热“铜绿”,绿色固体逐渐变为白色
C.木炭燃烧,发出耀眼的强光
D.蜡烛在氧气中燃烧,发出白光
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列说法错误的是
A.空气中含量最多的物质——氮气
B.地壳中含量最多的金属元素——铝
C.相对分子质量最小的物质——氢气
D.含氧量最高的氧化物——水
相关试题

