【题目】下图是a、b、c三种物质(均不含结晶水)的溶解度曲线。

①t1℃时物质的溶解度a b(填“>”或“<”或“=”);
②t2℃时将28g a物质加入到50g水中充分溶解,所得溶液的质量为 g,其中溶质与溶剂的质量比为 ;
③t1℃时,欲将c物质在m点对应的溶液变为p点的溶液,可采用的方法是 (写一种即可);
④t2℃时,将等质量的a、b、c三种物质的饱和溶液分别降温到t1℃时,所得溶液中的各项关系符合b>a>c的是 (填序号)。
Ⅰ.溶质质量 Ⅱ.溶剂质量 Ⅲ.溶液质量 Ⅳ.溶质的质量分数
⑤欲配置100g质量分数为15%的a物质的溶液,所需a物质 g,所需蒸馏水的体积为 mL,可选择的量筒规格为 mL(填50或100),溶解时玻璃棒的作用是 。
参考答案:
【答案】①<②75;1:2③加溶质或(恒温)蒸发溶剂
④Ⅰ、Ⅳ⑤15;85;100;加速溶解。
【解析】
试题分析:①由图可知t1℃时a在b的下方; ②t2℃时a的溶解度为50g,那么50g水最多溶解25ga物质,因此只能形成75g的溶液 ;m(溶质):m(溶剂)=25g:50g=1:2 ③由图即为t1℃时a的不饱和溶液变为饱和溶液;④t2℃时,将等质量的a、b、c三种物质的饱和溶液分别降温到t1℃时,ab的溶解度降低,溶质析出减少,c的溶解度升高,溶质不变,因此溶质质量b>a>c,Ⅰ符合;溶剂都不变,Ⅱ不符合;ab有溶质析出溶液质量减小,而c不会,因此溶液质量c>b>a,Ⅲ不符合;Ⅳ 由Ⅰ及溶剂质量不变可得Ⅳ符合⑤ m(a) = 100g × 15% = 15g ;v(H2O) = (100g-15g) ÷ 1g/ml = 85ml;遵循一次量取和精确的原则选100ml的;加速溶解。
-
科目: 来源: 题型:
查看答案和解析>>【题目】为探究氧化铜与木炭反应产生气体的成分,进行如下实验。(B装置内药品足量)

①加热装置A,刚开始B中导管口冒出的气泡成分是 ,当持续加热至固体质量不再减少,A中试管内的现象是 ,反应的化学方程式为 ;B中石灰水的作用 ;
②最终装置C与装置A中观察到的现象相同,说明碳与氧化铜反应还生成了 气体。装置C内反应的化学方程式 ;
③E处的作用是 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列各组离子在水中能大量共存的是
A.Na+、Fe3+、OH﹣、Cl﹣ B.H+、Na+、HCO3﹣、Cl﹣
C.Na+、K+、NO3﹣、Cl﹣ D.H+、K+、OH﹣、Cl﹣
-
科目: 来源: 题型:
查看答案和解析>>【题目】除去下列各组物质中的杂质,所选用的试剂及操作方法均错误的是
选项
物质
杂质
选用试剂
操作方法
A
CO2
HCl(气)
AgNO3溶液和浓硫酸
先通过硝酸银溶液,再通过浓硫酸
B
CaCl2溶液
HCl(盐酸)
过量CaCO3
过滤
C
木炭粉
CuO粉末
足量的稀硫酸
溶解过滤,洗涤晾干
D
Zn粉
FeCl2粉末
加足量的水
溶解、过滤
-
科目: 来源: 题型:
查看答案和解析>>【题目】水是我们熟悉的物质。右图是电解水实验的示意图。

①电极上的现象是 ;b管内生成的气体是 ;
检验a管内产生气体的方法是 。
②电解水发生化学反应的微观示意图如下:

从示意图中可获得的正确信息是 (填写编号)。
A.水由2个氢原子和1个氧原子构成
B.反应前后元素种类不变
C.化学变化的实质是原子的重新组合
D.反应前后分子的种类没变
E.该化学反应中,生成气体的体积比是2∶1
F.水是由氢气和氧气组成
③电解水的化学方程式为 。
④水体污染的来源主要有工业污染、农业污染和生活污水的排放等,请列举一种预防水体污染的具体做法 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下图所示实验,请回答相关问题:
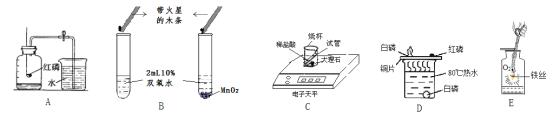
① 图A中若红磷用量不足,测得空气中氧气的体积分数将 ,红磷燃烧的化学方程式为 ;
② 图B中实验运用了 的研究方法,二氧化锰在反应前后 均不改变,
右边试管发生反应的化学方程式为 ;
③ 图C中反应后天平示数减少,有人说该反应不符合质量守恒定律。你的观点是 ;
④ 图D中铜片上的白磷燃烧了,热水里的白磷没有燃烧,说明燃烧条件之一是 。
⑤ 图E中铁丝在氧气中燃烧的现象是 ,反应的化学方程式 ;该实验瓶底放少量水或铺一层细砂的目的是 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列每组中的固体物质,只用水做试剂,不能将其鉴别出来的是
A.氢氧化钠、氯化钠 B.氧化铜、铁粉
C.高锰酸钾、碘 D.氧化钙、氢氧化钙
相关试题

