【题目】某金属冶炼厂的管道烟泥中含有某些单质,其中Cu约占10.3%、Zn约占5.0%、S约占1.2%。现欲回收铜和锌,并对硫进行环保处理,主要步骤如下图所示:
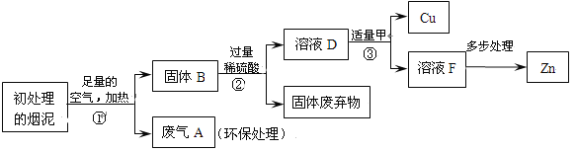
已知:加热的条件下,Zn、Cu都可以与氧气反应生成相应的金属氧化物。
(1)步骤①产生的废气A中,一定含有的有害气体是 。
(2)步骤③中反应的化学方程式是 , 。
(3)下列说法正确的是 。
a.②、③中的操作均包含过滤
b.溶液D和溶液F中ZnSO4的质量相等
c.溶液D中ZnSO4的质量大于CuSO4的质量
d.若步骤①中空气不足量,不会导致锌的回收率降低
参考答案:
【答案】(1)二氧化硫(或SO2)(2)Zn+H2SO4=ZnSO4+H2↑ Zn+CuSO4=Cu+ ZnSO4(3)ad
【解析】
试题分析:步骤①产生的废气A中,一定含有的有害气体是 二氧化硫,因为含有硫元素。步骤③中反应的化学方程式是Zn+H2SO4=ZnSO4+H2↑ Zn+CuSO4=Cu+ ZnSO4。说法正确的是:②、③中的操作均包含过滤,因为得到固体和液体的分离,若步骤①中空气不足量,不会导致锌的回收率降低,因为锌还会和酸发生反应,从而进入溶液。
-
科目: 来源: 题型:
查看答案和解析>>【题目】 图中的物质均是初中化学常见物质,其中A是常见的无色液体,F是大理石的主要成分,甲是生活里常用的燃料。根据它们之间的转化关系(有些反应条件、反应物、生成物已省略)。回答下列问题:

(1)D→E的化学方程式是:________;
(2)F→D的化学方程式是___________,该反应的基本类型
-
科目: 来源: 题型:
查看答案和解析>>【题目】金属材料在工农业生产、日常 生活中有着广泛应用。请根据所学知识填空:
(1)铝制品不易锈蚀的原因是铝与氧气作用,在表面形成了致密的保护膜,这种保护膜的化学成分用化学式表示为 。
(2)回收利用废金属是解决废金属造成资源浪费和不同程度的环境污染的方法之一。某化工厂处理回收含铜废料的生产流程与部分操作如下:
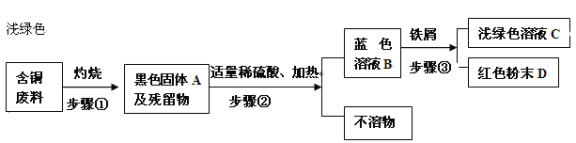
(注:步骤①得到的残留物不溶于水和稀硫酸)
①黑色固体A的化学式是 ;
②写出步骤③反应的化学方程式 ;
③通常在步骤③必须加入略过量的“铁屑”,原因是 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】瘦肉精被认为是肉制品业的“三聚氰胺”,属食品行业的违禁药品,瘦肉精的化学式为C12H19ON2Cl3。则下列有关瘦肉精的说法正确的是( )
A.瘦肉精由五种元素组成 B.一个瘦肉精分子中含有一个氮分子
C.瘦肉精由37个原子构成 D.瘦肉精中碳元素与氧元素的质量比为12∶1
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图分别是有关二氧化碳制取、干燥,收集和性质检验的装置图。请回答下列问题:
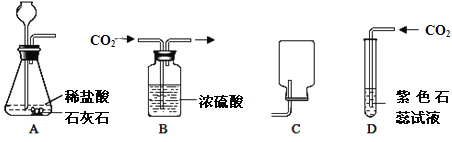
(1)四幅图中错误的是 (填字母序号)。
(2)请写出装置A中反应的化学方程式为
(3)如果实验室用装置A制取氧气,其反应的化学方程式为 。
(4)用B装置干燥二氧化碳时,利用了浓硫酸的 性。
(5)用D装置验证二氧化碳的性质时,反应现象是 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】碳和碳的氧化物是自然界庞大的家族。回答下列问题:
(1)金刚石硬而石墨软,是由于 不同。
(2)由于人类消耗化石燃料的增加和森林的乱乱砍滥伐,使空气中的CO2的含量上从而导致 增强,全球气候变暖。
(3)科学家正在研究将空气中过多的CO2与氢气在催化剂和加热条件下反应,转化为甲烷和水,这个反应的化学方程式是 。
(4)碳的两种氧化物可以互相转化。写出CO2转化为CO的化学方程式: 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化工厂排出的废液中含有一定量的AgNO3。化学兴趣小组同学收集了一些该化工厂排出的废液,准备将其中的银以单质的形式进行回收。他们进行了如下的实验活动
【设计方案】
①加入比银活动性强的金属单质;②除去金属混合物中的杂质。
【小组讨论】
①选择加入的金属。甲同学认为:向废液定中加入过量的铜粉,则得到银和铜的金属混合物;乙同学认为:向废液中加入过量的铁粉,则得到银和铁的金属混合物。
你认为 (填“甲”或“乙”)同学的方案更合理,原因是 ;
②除去银粉中混有的金属。向上述所得的金属混合物中加入的试剂是 ,反应的化学方程式为 。
【进行实验】进行实验:实验过程图示如下

操作a是 ,滤液B中溶质的化学式是 ;
【产品验证】
请你设计一种简单的化学实验检验得到的银粉中是否含铁粉: 。
相关试题

