【题目】(4分)化学是在原子、分子、离子水平上研究物质及其变化的科学。
(1)一定条件下,甲和乙反应生成丙和丁(四种物质均由分子构成),反应前后微观示意图如下。下列说法正确的是 (填序号)。
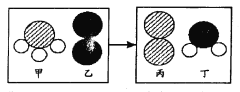
A.反应前后共有4种原子
B.该反应有单质生成
C.反应前后元素化合价都不变
D.化学变化中分子和原子均可再分
E.该化学反应中,甲、丁两种分子的个数比是2:3
(2)胃酸过多须服用抗酸药。下表为两种抗酸药的有效成分及其构成微粒:
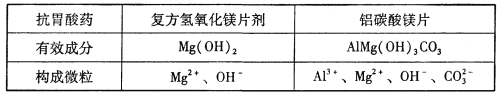
由于抗酸药有效成分不同,起抗酸作用(即消耗胃液中盐酸)的微粒也有差异。
①![]() 起抗酸作用的微粒是 (填微粒符号,下同);
起抗酸作用的微粒是 (填微粒符号,下同);
②铝碳酸镁与盐酸的反应为:![]() 。
。
则铝碳酸镁起抗酸作用的两种微粒是 、 。
参考答案:
【答案】(1)BE;
(2)①OH-- ②OH-- CO32-
【解析】
试题分析:(1)根据微观示意图可知,A.反应前后共有3种原子;B.该反应有单质生成是正确的叙述;C.反应前后有一种元素的化合价没有变,两种元素的化合价变化;D.化学变化中分子可再分,而原子不可分;E.该化学反应中,甲、丁两种分子的个数比是2:3,根据质量守恒定律可知是正确的叙述;(2)根据胃酸的成分为盐酸,质量胃酸过多的药物实际上是与盐酸中的氢离子反应的微粒,故①抗酸作用的微粒是OH--②铝碳酸镁起抗酸作用的两种微粒是OH-- CO32-。
-
科目: 来源: 题型:
查看答案和解析>>【题目】丁二酮(C4H6O2)可用作糖果增香剂。下列关于丁二酮的说法正确的是
A.丁二酮中含有氧分子
B.丁二酮中碳元素的质量分数最大
C.丁二酮中碳氢氧元素质量比为4:6:2
D.丁二酮中含有4个氢原子、6个氢原子和2个氧原子
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是一盏废旧台灯,某实验小组的同学利用它进行观察分析并完成相关实验.
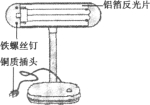
(1)小明发现台灯的铁螺丝钉表面已经锈蚀,原因是铁与空气中的________等发生了化学反应.
(2)小红发现铝箔反光片呈银白色,无锈迹,原因是铝表面有一层致密的氧化膜,生成该氧化膜的化学方程式为________.
(3)铁、铝、铜的金属活动性由强到弱的顺序为________.为了验证三者的金属活动性顺序,小志从实验室领来氯化铝溶液、硫酸铜溶液,并利用台灯提供的一种金属进行实验,即达到了实验目的.实验中发生反应的化学方程式为________.
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列做法不利于减轻环境污染的是
A.燃料脱硫以减少酸雨的产生
B.随意丢弃废旧电池
C.农药化肥的合理施用
D.开发利用清洁能源
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列有关pH试纸的使用方法或结论正确的是
A.直接将pH试纸浸入待测液中
B.用湿润的pH试纸测定稀氢氧化钠溶液的pH
C.用干燥的pH试纸测定稀盐酸的pH
D.用广泛pH试纸测得某溶液的pH为3.5
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质属于混合物的是
A.氧气 B.清新的空气 C.氯酸钾 D.金刚石
-
科目: 来源: 题型:
查看答案和解析>>【题目】(9分)镁及其化合物在生产、生活中应用广泛。
(1)从海水中提取金属镁,可按下图流程进行:

①下列说法正确的是 (填字母)。
A.步骤Ⅰ通过一步反应即可实现
B.步骤Ⅱ、Ⅲ、Ⅳ的目的是从海水中提纯氯化镁
C.步骤Ⅴ中化学能转化为电能
D.该流程涉及的基本反应类型有4种
②该流程中采取的一种降低成本且减少污染的措施是 。
(2)某化学兴趣小组对某种碱式碳酸镁晶体的组成进行探究。
【查阅资料】①碱式碳酸镁晶体可以表示为xMgCO3yMg(OH)2zH2O;②Mg(OH)2、MgCO3受热均能分解生成对应的氧化物;③碱石灰是固体氢氧化钠和生石灰等物质的混合物。
【设计实验】该小组同学设计了下图所示的实验装置,假设每步反应和吸收均进行完全。

【进行实验】取23.3g碱式碳酸镁晶体进行实验,步骤如下:
①连接好装置并检查气密性。
②装入药品,打开活塞K,通入一段时间空气。
③分别称量装置C、D的质量(数据见下表)。
装置C的质量
装置D的质量
步骤③
292.4g
198.2g
步骤⑥
296.9g
207.0g
④关闭活塞K,点燃酒精灯,使碱式碳酸镁晶体完全分解。
⑤停止加热,同时打开活塞K,通入空气至恢复到室温。
⑥再次分别称量装置C、D的质量(数据见右表)。
【实验分析】
①装置A的作用为 ,装置D的作用为 。
②反应后,装置B中的剩余固体是 ,质量为 g。
③该碱式碳酸镁晶体[xMgCO3yMg(OH)2zH2O]中,x︰y︰z = (写最简整数比)。
相关试题

