【题目】(10分)科学家设想利用太阳能加热器“捕捉CO2”、“释放CO2”,实现碳循环(如图所示)。
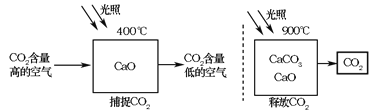
某化学小组的同学对此非常感兴趣,在老师的指导下,设计如下装置探究上述设想的反应原理是否可行。

(1)能证明装置A“释放CO2”的现象是 ;
(2)装置B在实验结束撤掉酒精喷灯时的作用是 ;
(3)上述反应结束后,小组同学对D中固体的成分进行探究,以证明是否“捕捉”到CO2。
【猜想与假设】
D中的固体可能为:I.只有氧化钙;Ⅱ.氧化钙与碳酸钙;Ⅲ.只有碳酸钙
【进行实验】
①甲同学从D中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物。甲同学据此认为试管中的固体为碳酸钙,即猜想Ⅲ成立。乙同学认为上述实验不足以证明猜想Ⅲ成立,其理由是 。
②乙同学从D中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热;继续向试管中加入几滴稀盐酸,没有发现气泡产生。乙同学据此认为试管中的固体只有氧化钙,即猜想I成立。丙同学认为乙的实验不足以证明猜想I成立,理由是 。
③丙同学认为利用感觉温度变化的方法判断是否有氧化钙不可靠,他用水、酚酞试液和
稀盐酸证明了猜想Ⅱ成立,请完成他的实验报告。
实验步骤 | 实验现象 | 实验结论 |
猜想Ⅱ成立 |
(4)通过以上探究,小组同学认为科学家的设想在反应原理上是可行的。该设想的优点
有 (填字母序号)。
A.原料易得 B.充分利用太阳能 C.释放出的CO2可作为资源加以利用
参考答案:
【答案】(1)C中的澄清的石灰水变浑浊
(2)防止装置C中的石灰水被吸入热试管中而使试管炸裂。
(3)①因氧化钙可与水反应生成氢氧化钙,微溶于水,也会形成白色不溶物
②加入少量的稀盐酸,会先和溶液中的氢氧化钙反应。无法说明一定不含碳酸钙。
③
实验步骤 | 实验现象 | 实验结论 |
取少量固体于试管中,加入水振荡,滴加几滴酚酞试液 向试管中加入足量的稀盐酸 | 溶液变红 有气泡产生 |
(4)ABC
【解析】
试题分析:(1)A中释放出的二氧化碳气体会进入装置C中,且会使澄清的石灰水变浑浊。所以当观察到C中的澄清的石灰水变浑浊,即可说明A中产生了二氧化碳。
(2)在实验结束撤掉酒精喷灯后,装置A中的温度会下降,其中的气压会降低。如没有装置B,则会吸入装置C中的石灰水而形成倒吸现象,而致试管炸裂。所以装置B的作用是防止装置C中的石灰水被吸入热试管中而使试管炸裂。
(3)①因氧化钙可与水反应生成氢氧化钙,氢氧化钙微溶于水,未完全溶解也会形成白色不溶物。所以也可能是氢氧化钙。
②加入水后,感觉试管壁发热可说明固体中含氧化钙。同时氧化钙能与水反应生成氢氧化钙。再加入少量的稀盐酸,会先和溶液中的氢氧化钙反应。无法说明一定不含碳酸钙。
③猜想Ⅱ为固体成分为氧化钙和碳酸钙。氧化钙可与水反应生成氢氧化钙,氢氧化钙的溶液呈碱性,可使酚酞试液变红。碳酸钙可与盐酸反应生成二氧化碳气体。所以可设计实验为:
实验步骤 | 实验现象 | 实验结论 |
取少量固体于试管中,加入水振荡,滴加几滴酚酞试液 向试管中加入足量的稀盐酸 | 溶液变红 有气泡产生 |
(4)该设想中所用的原料为碳酸钙,易得;充分利用了太阳能为反应的进行提供能量;可制得纯净的二氧化碳作为资源利用。所以应选ABC
-
科目: 来源: 题型:
查看答案和解析>>【题目】消防使用风力灭火机可以喷出类似十二级台风的气流将火吹灭,它灭火原理是( )
A. 隔绝空气 B. 吹走可燃物 C. 降温到着火点以下 D. 降低可燃物着火点
-
科目: 来源: 题型:
查看答案和解析>>【题目】在“创新实验装置”的竞赛中,某化学兴趣小组设计了如图所示的装置(夹持仪器已略去),引起同学们的兴趣.如图是四位同学对实验中的部分现象进行的预测,预测正确的是
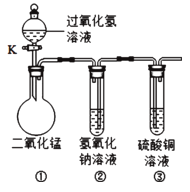
A. 打开活塞K,装置①中会有气泡冒出,黑色固体消失
B. 打开活塞K,装置②中会看到液面上升,产生蓝色沉淀
C. 打开活塞K,装置②中会有气泡冒出
D. 打开活塞K,装置③中会有液体流入,产生蓝色沉淀
-
科目: 来源: 题型:
查看答案和解析>>【题目】郝颖同学在化学课上提出,可用澄清石灰水来检验人呼出的气体是否是二氧化碳气体,就这一过程而言,属于科学探究环节中的
A.建立假设 B.收集证据 C.设计实验 D.做出结论
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列工艺制作过程中包含了化学变化的是 ( )
A.用纸剪窗花 B.泥土烧成瓷器
C.冰块制成冰雕 D.木板制成飞机模型
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室部分仪器或装置如图所示,请回答下列问题。
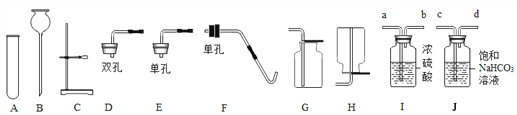
⑴装置B的名称为_________,实验室常用石灰石和稀盐酸制取二氧化碳气体,发生装置可选择图中的________(填仪器字母)进行组装。用高锰酸钾制取氧气,除了图中已有仪器外,还需补充的仪器是_________,反应的化学方程式为________________________。
⑵采用上述方法制取的二氧化碳中常含有氯化氢气体和水蒸气,为获得纯净、干燥的二氧化碳气体,可选用如图所示的I装置和J装置进行除杂和干燥,导管口连接的正确顺序是:气体→__________→G,除去HCl时发生反应的方程式为__________________________。
⑶某同学选用F装置收集二氧化碳,并用燃着的小木条放在瓶口验证二氧化碳是否收集满,结果发现火焰不灭,出现上述情况的原因可能是___________。(写出其中一条)
-
科目: 来源: 题型:
查看答案和解析>>【题目】工业上采用氨碱法生产纯碱,主要流程如下图,请据图回答相关问题。

⑴氨碱法生产所得产品为纯碱,向纯碱水溶液中滴入无色酚酞试液显________色。
⑵从步骤①提取粗盐常用___________(填“蒸发结晶”或“降温结晶”)方法。
⑶从酸碱反应的角度分析,步骤④中通入氨气的作用是____________________。
⑷步骤⑤所得的碳酸氢钠在生产和生活中有许多重要用途,请写出它的一种用途______。
⑸步骤⑥中发生反应的化学方程式为______________,该反应类型属于________反应。
⑹工业产品中往往含有一些杂质,用“氨碱法”制得的纯碱含有少量氯化钠。为了测定该产品中碳酸钠的纯度,进行以下实验:取16.5g纯碱样品放入烧杯中,将烧杯放在电子天平上,再把150g稀盐酸(足量)加入样品中,观察读数变化如下表所示:
时间/s
0
5
10
15
读数/g
215.2
211.4
208.6
208.6
请你据此分析计算:
①实验中产生二氧化碳的质量为____________;
②该产品中碳酸钠的质量分数_______(写出计算过程,结果精确到0.1%)
相关试题

