【题目】铁是目前世界年产量最多的金属。如图所示,甲图是实验室一氧化碳还原氧化铁实验装置图:

回答下列问题:
(1)甲中硬质玻璃管中观察到的现象是_____________,写出玻璃管中的化学反应方程式_____________,该反应中,还原剂是 __________ ,发生还原反应的是___________________。
乙试管中的现象是________________,反应方程式______________________。
(2)实验前,先检查装置的_________;先检验气体的____________________。
实验开始时,先通入一氧化碳,后点酒精喷灯,目的是_____________;
实验结束时,先灭酒精喷灯,继续通一氧化碳,直到玻璃管冷却,目的是________ ;
(3)丙中导管末端加一点燃的酒精灯的目的是________,反应方程式是__________。
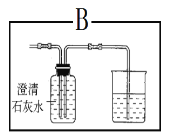
(4)若将上图A部分换成B部分,下列说法正确的是:

①收集多余的CO ②检验CO2并吸收反应生成的CO2 上述说法中正确的___________
A.只有① B.只有② C.是①和②
(5)工业炼铁的设备是________,冶炼得到的产品是_____________
(6)空气通过进风口与原料中的焦炭充分反应,其化学方程式为____________________
(7)由(6)中产生的气体与炽热的焦炭会继续反应,其化学方程式为_______________
参考答案:
【答案】红色粉末变黑3CO+Fe2O3 ![]() 2Fe+3CO2COFe2O3澄清石灰水变浑浊CO2 + Ca(OH)2====CaCO3 ↓ + H2O气密性纯度排出空气, 防止爆炸防止铁再次被氧化点燃有毒的CO,防止污染空气2CO+O2
2Fe+3CO2COFe2O3澄清石灰水变浑浊CO2 + Ca(OH)2====CaCO3 ↓ + H2O气密性纯度排出空气, 防止爆炸防止铁再次被氧化点燃有毒的CO,防止污染空气2CO+O2![]() 2CO2C高炉生铁C+O2
2CO2C高炉生铁C+O2![]() CO2CO2+C
CO2CO2+C![]() 2CO
2CO
【解析】
(1)一氧化碳和氧化铁反应生成铁和二氧化碳,甲中硬质玻璃管中观察到的现象是红色粉末变黑,玻璃管中的化学反应方程式3CO+Fe2O3 ![]() 2Fe+3CO2,反应中得氧的物质是还原剂,失氧的物质是氧化剂,该反应中还原剂是一氧化碳,氧化铁发生的是还原反应;二氧化碳和氢氧化钙反应生成碳酸钙沉淀,乙试管中的现象是澄清石灰水变浑浊,反应方程式CO2 + Ca(OH)2====CaCO3↓+ H2O;
2Fe+3CO2,反应中得氧的物质是还原剂,失氧的物质是氧化剂,该反应中还原剂是一氧化碳,氧化铁发生的是还原反应;二氧化碳和氢氧化钙反应生成碳酸钙沉淀,乙试管中的现象是澄清石灰水变浑浊,反应方程式CO2 + Ca(OH)2====CaCO3↓+ H2O;
(2)实验前,先检查装置的气密性;加热或点燃可燃性气体前都要检验气体的纯度,防止发生爆炸;实验开始时,先通入一氧化碳,后点酒精喷灯,目的是排尽装置内的空气,防止加热时发生爆炸;实验结束时,先灭酒精喷灯,继续通一氧化碳,直到玻璃管冷却,目的是防止生成的高温的铁再被氧化;
(3)丙中导管末端加一点燃的酒精灯的目的是点燃尾气中的一氧化碳,使一氧化碳转化成二氧化碳,反应方程式是2CO+O2![]() 2CO2;
2CO2;
(4)若将上图A部分换成B部分,通过二氧化碳与氢氧化钙反应生成碳酸钙沉淀,能检验CO 2,同时一氧化碳进入广口瓶,随气体增多压强增大,将液体压入烧杯中而达到收集一氧化碳的目的,故选C;
(5)工业炼铁的设备是高炉,冶炼得到的产品是含有少量杂质的生铁;
(6)空气通过进风口与原料中的焦炭充分反应生成二氧化碳,其化学方程式为C+O2![]() CO2;
CO2;
(7)二氧化碳高温下能与焦炭反应生成一氧化碳,其化学方程式为CO2+C![]() 2CO。
2CO。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下列化合物与单质相互转化的关系(如下图), 请写出化学式:
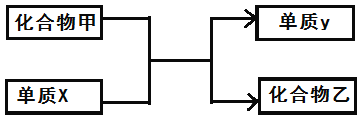
(1)若乙的溶液为浅绿色,y是红色固体,则x是________________;
(2)在常温下若乙是气体,则x是________________;
(3)若常温下乙为无色液体,则x为______________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】金属钛被称为铁和铝之后崛起的“第三金属”,钛的硬度大、熔点高、常温下耐酸碱、耐腐蚀,是航海、化工、医疗上不可缺少的材料.钛铁矿(主要成分FeTiO3(钛酸亚铁),是工业上冶炼金属钛的主要原料,制备金属钛的一种工艺流程如图所示(部分产物略)。
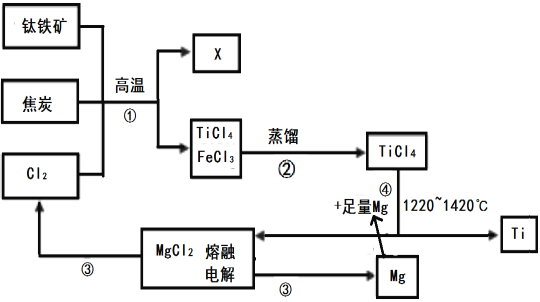
(1) FeTiO3 (钛酸亚铁)中Ti元素的化合价为_____________;
(2)步骤(1)中生成的可燃性气体氧化物X为______________ (写出物质的化学式)。
(3)步骤(4)中在高温下与足量Mg反应生成金属Ti,此反应的化学方程式为_________________ ,该反应说明Mg与Ti的金属活动性强弱关系为:Mg______Ti (填“>”、“<”或“=”)。
(4)用上述冶炼方法得到的金属钛中会混有少量金属单质是____________(填化学式)。
(5)绿色化学提倡物料循环,以上流程中,可用于循环的物质除Cl2、Mg之外,还有_______________(填化学式) 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】为了测定某黄铜(铜锌合金)样品中铜的质量分数(不考虑黄铜中的其他杂质),现将30g稀盐酸分三次加入到10g黄铜样品粉末中,每次充分反应后,测定生成气体的质量数据见下表:
第一次
第二次
第三次
加入稀盐酸的质量/g
10
10
10
生成氢气的质量/g
0.08
m
0.04
试求:
(1)m=______________;
(2)此黄铜样品中铜的质量分数________;
(3)请画出随着稀盐酸的加入,生成氢气的质量关系图__________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】分别写出下列物质发生化学变化的文字表达式:
(1)实验室加热高锰酸钾制氧气____________________________
(2)铁丝在氧气中燃烧 ____________________
(3)红磷燃烧 _____________________________________
-
科目: 来源: 题型:
查看答案和解析>>【题目】以下是研究实验室制取氧气的装置图,请按要求回答下列问题.
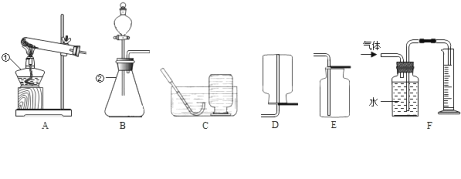
(1)写出图中标号仪器的名称:① ___________;②_______________。
(2)用排水法收集氧气的理由______________________________;
用向上排空法收集氧气的理由是_______________________________。
(3)实验室用氯酸钾制取氧气,应选用的发生装置是_________,(填字母序号,下同),该化学反应的文字表达式为______________________,若要收集一瓶干燥的氧气,应选择的收集装置是____________ 。
(4)实验室用H2O2溶液和MnO2混合制氧气,其中MnO2起___________作用,该化学反应文字表达式为__________________。同学们利用B和F装置,通过排水量来测定生成氧气的体积,反应结束后,发现量筒内收集到的水的体积总是比理论值偏大(水的体积测量准确),其主要原因是______________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某同学设计了测定空气中氧气含量的实验,实验装置如图。该同学的实验步骤如下:
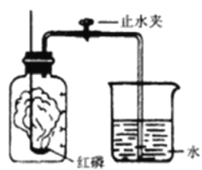
①将图中的集气瓶分为5等份,并作好标记。
②在带橡皮塞和导管的燃烧匙内装入足量的红磷,将导管上的止水夹夹紧,在酒精灯上点燃红磷,并立即伸入集气瓶内,塞紧橡皮塞。
③充分反应后,待集气瓶冷却至室温,打开止水夹。
请回答下列问题:
(1)该实验中红磷需稍过量,目的是__________________________________。
(2)步骤②集气瓶中的现象是_______________________________;步骤③中打开止水夹后观察到的现象是_________________________________ ,由此可得出氧气约占空气体积的__________。
(3)该实验可推论出氮气_________(填“易”或“难”)溶于水和其化学性质___________(填“活泼”或“不活泼”)的结论。
相关试题

