【题目】小明同学取14%的硫酸溶液70g于烧杯中,然后向烧杯中慢慢加入10g氧化铜粉末并不断搅拌,测得烧杯中溶液的质量与加入氧化铜粉末的质量关系如图所示。
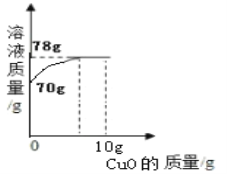
求:
(1)完全反应时共消耗氧化铜的质量为 g;
(2)配制14%的硫酸溶液70g,需要98%的硫酸溶液 g;
(3)反应后所得溶液中溶质的质量分数为多少?(写出计算过程,最后结果保留到小数点后1位)
参考答案:
【答案】(1)8
(2)10
(3)解:设生成硫酸铜的质量为x。
CuO + H2SO4 = CuSO4+H2O
80 98 160
8g x
80/8g = 160/ x
x = 16g
反应所得溶液中溶质的质量分数= 16g÷78g×100% =20.5%
答: 反应所得溶液中溶质的质量分数为20.5%。
【解析】根据质量守恒定律知(1)完全反应时共消耗氧化铜的质量为78g-70g=8g. (2)配制14%的硫酸溶液70g,需要98%的硫酸溶液质量为x
70g×14%=98%×x,x=10g.
(3)反应后所得溶液中溶质的质量分数为
解:设生成硫酸铜的质量为x。
CuO + H2SO4=CuSO4+H2O
80 160
8g x
![]() =
=![]() ,x=16g.
,x=16g.
反应后所得溶液中溶质的质量分数为![]() ×100%=20.5%.
×100%=20.5%.
答∶(1)完全反应时共消耗氧化铜的质量为8g.
(2)配制14%的硫酸溶液70g,需要98%的硫酸溶液是10g.
⑶反应所得溶液中溶质的质量分数为20.5%。
点睛∶本题主要考查质量守恒定律的应用和根据化学方程式进行计算。
-
科目: 来源: 题型:
查看答案和解析>>【题目】常温下,一些食物的近似pH如下,其中显碱性的是
A. 柠檬汁(2.1~2.8) B. 菠萝汁(3.3~5.2)
C. 牛奶(6.3~6.6) D. 鸡蛋清(7.6~8.0)
-
科目: 来源: 题型:
查看答案和解析>>【题目】当汽车油箱泄露时,采取的应急措施首先是
A. 亮灯查找泄露源 B. 打开车窗,严禁一切火种
C. 洒水吸收汽油 D. 报警说明情况
-
科目: 来源: 题型:
查看答案和解析>>【题目】将下列固体分别放入水中,溶液温度明显降低的是
A. 硝酸铵 B. 生石灰 C. 烧碱 D. 食盐
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质属于纯净物的是
A、洁净的空气 B、自来水 C、冰水混合物 D、澄清的石灰水
-
科目: 来源: 题型:
查看答案和解析>>【题目】空气、水都是重要的自然资源。
(1)敞口放置在空气中的饼干会变软,说明空气中含有___________。
(2)空气污染指数与空气质量的关系是_________________。为减少空气污染,工业上将含有SO2的尾气用________(填“酸性”“碱性”“中性”)液体处理后再排放。
(3)为了减缓大气中的CO2含量的增加,以下建议中不可行的是___________(填序号)。
A.禁止使用煤、石油、天然气等矿物燃料
B.开发太阳能、水能、风能、地热等新能源
C.大量植树造林,禁止乱砍乱伐
(4)雷阵雨过后,空气特别清新,原因之一是空气中少量氧气(O2 )转化为臭氧(O3),表示为3O2
 2O3 。下列说法中正确的是_______。
2O3 。下列说法中正确的是_______。A.O2与O3的相对分子质量相等 B.该反应属于物理变化
C.等质量的 O2与O3所含原子数相等 D.O2 与O3是同一种物质
(5)下列净化水的方法中,净化程度最高的是_______。
A.蒸馏 B.吸附 C.沉淀 D.过滤
(6)对水的净化与软化说法正确的是________。
A.它们的原理相同
B.水的净化和软化都能使水变为纯净水
C.水的净化只是过滤
D.水的软化是降低水中Ca2+、Mg2+的浓度
-
科目: 来源: 题型:
查看答案和解析>>【题目】在宏观、微观和符号之间建立联系是学习化学的特点。
(1)现有下列四种粒子:①Mg2+ ②H2SO4 ③C60 ④CO32-
其中能表示化合物的是____(填序号),由①和④两种粒子构成的化合物属于_________(填“氧化物”、“酸”、“碱”或“盐”)。
(2)氢氧化铝可治疗胃酸过多。请完成反应方程式Al(OH)3+3HCl=_________+3H2O,该反应属于___________反应(填基本反应类型)。
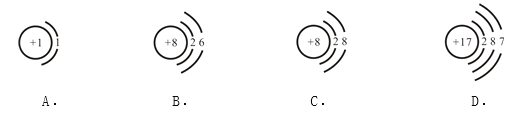
(3)下面示意图表示的粒子中,属于阴离子的是_____(填序号),与该阴离子属于同种元素的是_____。
(4)在一定条件下,A、B两种物质反应可生成C、D(A、B、C、D均由分子构成)。反应前后的微观示意图如下所示。下列说法正确的是_________。
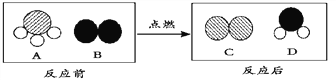
A.该反应中共有4种原子 B.该反应中有单质生成
C.该反应中元素化合价都不变 D.化学变化中分子和原子均可再分
相关试题

