【题目】某化学兴趣小组在探究稀盐酸的化学性质时,做了如图一所示的三个实验。
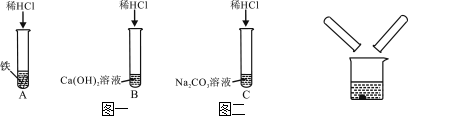
(1)A试管中的反应现象是 。
(2)C试管中反应的化学方程式是 。
(3)实验结束后,小组同学将B、C两支试管中的废液同时倒入一个洁净的烧杯中(如图二所示),观察到先有气泡产生,后有白色沉淀生成。同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究。
【提出猜想】
甲同学猜想:有NaCl
乙同学猜想:有NaCl、CaCl2
丙同学猜想:有NaCl、CaCl2、 HCl
你的猜想:有 。
【交流讨论】
你认为 同学的猜想一定不正确,理由是 。
【设计实验】请设计实验证明你的猜想正确。
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,向其中滴加 。 | _________________。 | 我的猜想成立 |
【反思与总结】判断反应后溶液中溶质的成分,除要考虑生成物外,还需考虑 。
参考答案:
【答案】(1)铁片表面有气泡产生,溶液由无色逐渐变为浅绿色(2)Na2CO3 + 2HCl===2NaCl + H2O + CO2↑
(3)你的猜想:NaCl、Na2CO3 丙 理由是:白色沉淀是CaCO3,能与盐酸反应,二者不能共存(表述合理即可)
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,向其中滴加 无色酚酞试液 。 | 溶液变红 | 我的猜想成立 |
(或滴加紫色石蕊试液,实验现象为紫色石蕊试液变蓝;滴加稀盐酸等稀酸,实验现象为产生气泡;滴加CaCl2溶液、BaCl2溶液、Ca(NO3)2溶液、Ba(NO3)2溶液、Ca(OH)2溶液、Ba(OH)2溶液,实验现象为产生白色沉淀等合理即可,但要注意所加试剂与实验现象相对应。)
反应物是否有剩余 (表述合理即可)
【解析】
试题分析:根据金属活动性顺序可知(1)A中的现象为铁片表面有气泡产生,溶液由无色逐渐变为浅绿色;(2)C试管中反应的化学方程式是Na2CO3 + 2HCl===2NaCl + H2O + CO2↑;(3)有实验现象可知,B盐酸剩余,C为碳酸钠剩余;二者混合后,一定没有盐酸,根据反应程度,故猜想为NaCl、Na2CO3【交流讨论】白色沉淀是CaCO3,能与盐酸反应,二者不能共存,故丙同学的不正确;【设计实验】根据结论可知含有氯化钠和碳酸钠,根据碳酸钠的性质进行操作取少量滤液于试管中,向其中滴加 无色酚酞试液,溶液变红色即可证明。
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲、乙两种物质的溶解度曲线如图。

(1)10℃时,甲物质的溶解度 (选填“大于”、“小于”或“等于”)乙物质的溶解度。
(2)40℃时,把40g甲物质放入100g水中,所得的是 (选填“饱和”或“不饱和”)溶液。
(3)20℃时,甲物质溶液中溶质的质量分数不可能为 。
A.20% B.25% C.26.5% D.30%
-
科目: 来源: 题型:
查看答案和解析>>【题目】钙是维持人体正常功能所必须的元素,有时需要服用补钙满足人体需求.如图分别为两种补钙剂说明书的一部分.

请根据图示中的信息回答下列问题:
(1)钙是人体必须的常量元素,每日要摄取足量的钙,才能避免 (填字母序号);
A.佝偻病或骨质疏松 B.贫血症 C.甲状腺肿大
(2)葡萄糖酸钙(C12H22O14Ca)的化学式量是 ;
(3)碳酸钙(化学式为CaCO3)中钙元素的质量分数为 ;
(4)每片金钙尔奇中含碳酸钙的质量为 mg;
(5)按照金钙尔奇说明书每日的补钙量,若该服用葡萄糖酸钙片,一日3次,一次应服用 片.
-
科目: 来源: 题型:
查看答案和解析>>【题目】“低碳经济”已成为经济发展的重要模式,实现“低碳经济”的一种策略是节能。下列制备氧气的方法最节能的是
A. 通电电解水生成氢气和氧气 B. 加热氯酸钾和二氧化锰制取氧气
C. 双氧水和二氧化锰制取氧气 D. 加热高锰酸钾制取氧气
-
科目: 来源: 题型:
查看答案和解析>>【题目】葡萄糖酸亚铁是治疗缺铁性贫血的一种药品,它的化学式为C12H22FeO14,
求:①葡萄糖酸亚铁的相对分子质量为 ;
②该物质中铁元素的质量分数为 ;
③若某病人要补充2.8g铁元素,医生开给病人 g葡萄糖酸亚铁。
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室取用一定量的液体药品,可以用 量出体积。量液体体积时,必须放 ,视线要跟容器内液体的 处保持水平,然后再读出液体的体积数。
-
科目: 来源: 题型:
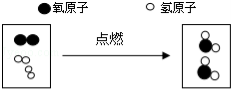
查看答案和解析>>【题目】如图是某化学反应的微观示意图(表示氧原子,表示氢原子)
(1)该反应的化学方程式为 ;
(2)以上变化的基本反应类型是 ;
(3)结合如图,从原子、分子的角度分析,在化学反应过程中, 可分,而 不能再分.
相关试题

