【题目】下图为“хх”钙片商品标签图,请根据标签的有关信息完成下列各题。

(1)主要成分碳酸钙由__________种元素组成。
(2)碳酸钙中各元素的原子个数比为__________。
(3)每片钙片中至少含钙元素的质量为__________g。
(4)小花同学为测定其中碳酸钙的含量标注是否属实,她取出10片钙片,研碎后放入小烧杯中,再加入50g稀盐酸,在T0至T3时间段,测得反应剩余物的质量变化如下:
①生成的二氧化碳的质量是__________?
②通过计算判断该钙片中碳酸钙的含量标注是否属实__________。
时 间 | T0 | T1 | T2 | T3 |
反应剩余物质量(g) | 70 | 65 | 63.4 | 63.4 |
参考答案:
【答案】 三 Ca∶C∶O=1∶1∶3 0.6g 6.6g 钙片中碳酸钙的含量标注属实
【解析】本题考查了根据化学式和化学方程式计算,根据表格中数据得到生成的二氧化碳质量是关键。。
(1)由碳酸钙的化学式可知,它是由碳、氢、氧三种元素组成的;
(2)碳酸钙中各元素的原子个数比Ca∶C∶O=1∶1∶3;
(3)每片钙片中至少含钙元素的质量为:1.5g×![]() ×100%=0.6g;
×100%=0.6g;
(4)①根据质量守恒定律,生成的二氧化碳的质量为:70-63.4=6.6g;
②解:设10片样品中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
X 6.6g
![]() =
=![]() x=15g;
x=15g;
每片含碳酸钙的质量为: ![]() =1.5g,钙片中碳酸钙的含量标注属实。
=1.5g,钙片中碳酸钙的含量标注属实。
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室部分装置如下图所示,请回答下列问题。

(1)实验室可以用如下方法制备一些常见的气体,请用图1中字母编号填写下表空白。
制气方法
制取的气体
发生装置
收集装置
①加热高锰酸钾
O2
A
_____或F
②大理石和稀盐酸混合
CO2
C
_____
③加热二氧化锰和浓盐酸
Cl2
_______
D
﹙2﹚用装置A制取O2时,装入药品前应进行的实验操作是_________;选用F装置收集O2时,下列实验操作不正确的是 ________________(填序号)。
①点燃酒精灯前,将集气瓶注满水,用玻璃片盖住瓶口,倒立在盛水的水槽中;
②加热时,当看到有气泡从导管口冒出,立即将导管口移入集气瓶口收集气体;
③集满气体后,在水里用玻璃片盖住瓶口,再将集气瓶移出水槽,正放在桌上;
﹙3﹚用上述方法②制取CO2时发生反应的化学方程式为____________________;若用图2的装置检验CO2气体,则气体应从___(填“a”或“b”)端通入。
(4)用上述方法③制取并收集到的Cl2不够纯净,含有的杂质气体中除了少量空气和水蒸气外,还有_(填化学式)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】铁粉与硫酸铜溶液反应,除了有红色固体生成外,还有一种无色无味的气体产生。为确定气体的成分,进行下列实验探究。
【猜想与假设】:依据____可知气体可能是SO2、O2、H2中的一种或几种。
【查阅资料】:
①SO2能使酸性高锰酸钾溶液褪色。
②O2+4KI+4HCl=2I2+4KCl+2H2O,淀粉遇I2变蓝。
③H2、CO等气体能将氧化铜还原成铜。
【实验验证】:
(1)将气体通入酸性高锰酸钾溶液中,无现象,则该气体中 无SO2。小明同学认为没有必要做这个实验,只要根据“无色无味的气体”就可推导出该气体一定不是SO2,他的依据是_________________________。
(2)用下列所示实验检验氢气和氧气:
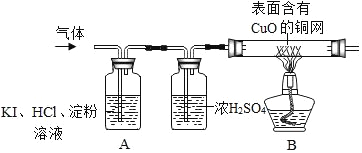
A中观察到_____ ,证明无O2; B中观察到_____ ,证明该气体是H2。
【实验反思】:(1)大家认为丙同学在加热之前,应对气体先________________以确保安全。
(2)由上述实验可知,硫酸铜溶液显 ______性(填“酸”或“碱”或“中”)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】今年三鹿问题奶粉事件使许多婴幼儿产生不良影响,长期摄入三聚氰胺会造成生殖、泌尿系统的损害,造成膀胱、肾部结石,并可进一步诱发膀胱癌。由于食品和饲料工业蛋白质含量测试方法的缺陷,三聚氰胺也常被不法商人用作食品添加剂,以提升食品检测中的蛋白质含量指标。已知三聚氰胺的化学式为C3H6N6,试计算:
(1)三聚氰胺的相对分子质量_____
(2)三聚氰胺由_____种元素组成,其中碳、氢、氮元素的质量比是_____
(3)三聚氰胺中300g的三聚氰胺中氮元素的质量为____________
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列实验符合下图所示变化趋势的是( )

选项
实验
横坐标
纵坐标
A
向一定量氢氧化钠
溶液中滴加稀硫酸
稀硫酸的质量
水的质量
B
加热一定量氯酸钾固体
反应时间
剩余固体中
氧元素的质量
C
向一定量饱和硝酸钾溶液中加水
加水的质量
溶质的质量分数
D
向一定量镁粉中加入稀盐酸
稀盐酸的质量
镁元素的质量
A. A B. B C. C D. D
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是X、Y、Z三种固体物质的溶解度曲线图,下列说法正确的是(____)
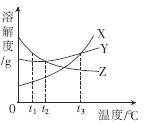
A.t1℃时,将X、Y、Z的饱和溶液都升温到t3℃,溶液仍然饱和的是Y、Z的溶液
B.t2℃时,Y和Z的溶液的溶质质量分数相等
C.t3℃时,将X、Y、Z的饱和溶液都降温到t1℃,溶液中溶质质量分数由大到小的顺序为Y> Z> X
D.在t1℃时,X的饱和溶液质量为230 g,蒸干后得到30 g的X固体(不含结晶水),则t1℃时X的溶解度为________
-
科目: 来源: 题型:
查看答案和解析>>【题目】在老师的帮助下,同学们制作了“叶脉书签”。制作中需用到10%的氢氧化钠溶液200 g,
下图是配制该溶液的实验操作。

下列操作步骤正确的是(_____)
A.操作①中,需称量氢氧化钠固体20 g
B.操作②中,玻璃棒的作用是搅拌防止液体溅出
C.视线如图③所示(其他操作正确),会造成所配制溶液的溶质质量分数偏大
D.实验结束后,处理废液的方法是____
相关试题

