【题目】实验室有碳酸钾和碳酸钙的固体混合物75g,使之与500g质量分数为14.6%的盐酸充分反应,将反应后的溶液蒸干得到82.7g固体。则原混合物中金属元素的质量分数为
A. 44% B. 50% C. 55% D. 68%
参考答案:
【答案】A
【解析】碳酸钾、碳酸钙与稀盐酸反应的化学方程式分别为CaCO3+2HCl═CaCl2+H2O+CO2↑、K2CO3+2HCl═2KCl+H2O+CO2↑,由上述化学方程式可知,碳酸钾、碳酸钙与盐酸完全反应后,可看成碳酸根离子被两个氯离子取代,两个氯离子的相对原子质量的和是71,碳酸根的相对原子质量的和是60,差是11,即完全反应后质量增加了11份质量.实际反应后固体质量增加了82.7g-75g=7.7g,设原混合物中含碳酸根的质量为x,则60:11=x:7.7g,x=42g;则所含金属元素质量为75g-42g=33g,原混合物中金属元素的质量分数为![]() ×100%=44%。
×100%=44%。
-
科目: 来源: 题型:
查看答案和解析>>【题目】用化学用语表示:
(1)锌元素_________;(2)2个铵根离子________;
(3)二氧化硅 ______;(4)人体缺少_____元素,会导致甲状腺疾病。
-
科目: 来源: 题型:
查看答案和解析>>【题目】为了节能减排,科学家发明了一种以某种镁硅酸盐矿石[主要成分Mg3Si2O5(OH)4]为原料的新型绿色水泥。全球镁硅酸盐储量丰富,新型绿色水泥不必担心原材料,推广潜力很大。新型绿色水泥与传统水泥对比如图。
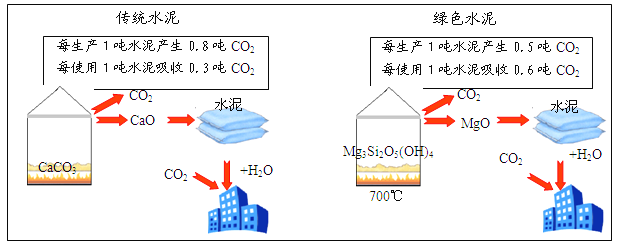
(1)传统水泥和绿色水泥的生产过程分别涉及以下反应:
CaCO3 高温CaO+ CO2↑ Mg3Si2O5(OH)4高温3MgO + 2SiO2 + 2H2O↑
以上两个反应都属于 (填写基本反应类型)。
(2)与传统水泥相比,每生产和使用1吨绿色水泥能够减少排放 吨二氧化碳。
(3)传统水泥生产中,高温煅烧某种石灰石50吨,可产生二氧化碳多少吨?已知该石灰石中碳酸钙含量为80%,杂质不反应。
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是

A. 将100g10%的甲溶液稀释到4%需加入150g水
B. t1℃时,将25g丙溶解到50g水中能得到饱和溶液
C. t2℃时,甲、乙溶液中溶质的质量分数一定相等
D. 分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得到的三种溶液中溶质的质量分数大小关系是乙>甲>丙
-
科目: 来源: 题型:
查看答案和解析>>【题目】在密闭容器中有甲、乙、丙、丁四种物质,在一定的条件下充分反应,测得反应前后各物质的质量分数如图所示,下列说法正确的是

A. 丁一定是化合物
B. 丙一定是这个反应的催化剂
C. 该反应一定是分解反应
D. 该反应可能是碳酸钙的分解
-
科目: 来源: 题型:
查看答案和解析>>【题目】碳单质多种多样,但化学性质相似,常温下具有 性;寒冬,人们常常烧炭取暖,这是利用了碳单质的 性;专家提醒,这种传统的取暖方式潜藏着巨大的危险,需要打开门窗,保持通风,因为过程中产生的一氧化碳能与血红蛋白结合,具有 性。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列图像不能正确反映对应变化关系的是( )
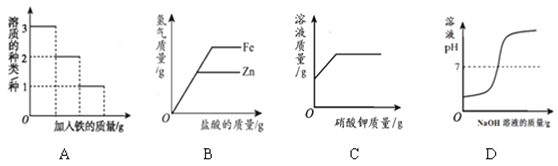
A.在一定量AgNO3和Zn(NO3)2的混合溶液中加入铁粉
B.向等质量的锌粉和铁粉中,分别加入相同质量分数的稀盐酸
C. 常温下,向硝酸钾的不饱和溶液中加入硝酸钾晶体
D.向一定量的稀盐酸中加入过量的NaOH溶液
相关试题

