【题目】有一瓶气体,可能是 CO、 CO2 、 H2O 、 H2 中的一种或几种组成。为了分析该气体的成分,取适量该气体进行实验,实验方案设计如下:
(提示:Ⅰ.浓硫酸具有吸水性,能干燥某些气体;Ⅱ.假设每一步都吸收完全;Ⅲ.氢气还原氧化铜得到铜和水)。
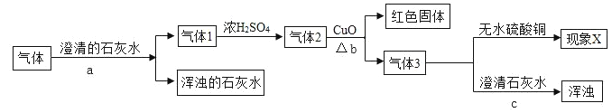
①上述可能存在的气体中,易与血红蛋白结合的气体是________。
②通过步骤 a 能确定一定含有的气体是_______。
③实验中如没有用浓 H2SO4 干燥气体 1,对气体检验______(选填“有”或“无”)影响。
④若现象 X 为“无水硫酸铜变蓝色”,结论是气体中__________;若现象 X 为“无水硫酸铜不变色”,结论是气体中_________。
⑤b 中一定发生的反应方程式是________________。
⑥该实验不能确定是否含有 H2O 蒸汽,改进的实验方案是_________________。
参考答案:
【答案】CO CO2 有 一定含有 H2 一定不含 H2 CO+CuO ![]() Cu+CO 2 在操作 a 前先通入装有无水 CuSO4 的装置
Cu+CO 2 在操作 a 前先通入装有无水 CuSO4 的装置
【解析】
(1)CO易与血红蛋白结合,导致中毒死亡;
(2) 步骤 a为气体通入澄清石灰水,石灰水变浑浊,故混合气体中一定含有CO2;
(3) 实验中如没有用浓 H2SO4 干燥气体 1,将会无法证明H2O是混合气体中的,还是气体3反应生成的,故对气体检验有影响;
(4) 若现象 X 为“无水硫酸铜变蓝色”,证明氢气与氧化铜的反应发生了,故该气体中一定含有H2;
若现象 X 为“无水硫酸铜不变色”,证明氢气与氧化铜的反应没发生,故该气体中一定不含H2;
(5)因为气体3中通入澄清石灰水,石灰水变浑浊,所以,一氧化碳与氧化铜的反应发生了,化学方程式为CO+CuO ![]() Cu+CO 2
Cu+CO 2
(6)该实验因为混合气体首先通入澄清石灰水,所以,不能确定是否含有 H2O 蒸汽,改进方案为在操作 a 前先通入装有无水 CuSO4 的装置
-
科目: 来源: 题型:
查看答案和解析>>【题目】R 是硝酸钾或氯化铵中的一种。硝酸钾或氯化铵的溶解度曲线如图 1 所示,进行如图 2 所示实验。
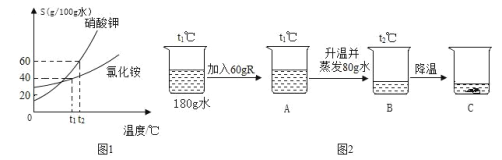
① t1 ℃时,氯化铵的溶解度为_________。
② A 烧杯中溶液的溶质质量分数为_________。
③根据以上信息可推出 R 是_______(写名称或化学式均可)。
④关于图 2 中烧杯内的物质,以下几种说法正确的是_____。
a.A、B、C 中,只有 C 中上层清液是饱和溶液
b.若使 C 中的固体溶解,可采用加水或升温的方法
c.A 和 B 的溶液中,溶质质量相等
d.A 的溶液中溶质质量分数一定比 C 的上层清液中溶质质量分数小
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据图 1 实验装置回答问题。

①A 实验中仪器 a 的名称是________。
②A 实验中连接玻璃管和橡皮管的操作,先把玻璃管口_______,然后稍稍用力,即可把玻璃管插入橡皮管内;该反应的化学方程式______________________,该反应类型是_______;排水法收集氧气后,用玻璃片_______(选填“磨砂”或“光滑”)的一面盖住集气瓶口。
③上述三个实验中,水对实验仪器起到安全保护作用的是_______(填字母)。
④C 实验中的实验现象是__________,该反应的化学方程式是____________;该实验中细铁丝成螺旋状的原因是________________。
⑤B 实验中,发生反应的化学方程式是_________;B 实验过程中广口瓶内压强变化曲线如图 2:CD 段气压变化的原因是__________。
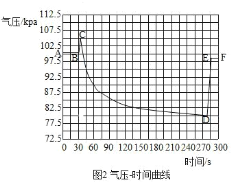
实验前广口瓶内空气体积为 V,烧杯中水的体积为V1 ;实验后烧杯中剩余水的体积为V2 。计算空气中氧气体积分数的表达式为________(用 V、V1 、V2 表示)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】牙膏中的摩擦剂碳酸钙可以用石灰石来制备,设计实验方案如下图。
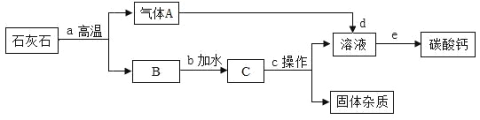
①写出步骤 a、b 中反应的化学方程式___________、_____________。
②c 操作用到的玻璃仪器有玻璃棒、烧杯、_______。
③c 操作得到的溶液中溶质的化学式为____________,其中原子团的名称是_______。
④该实验方案中____步骤(选填“a”、“b”、“c”、“d”、“e”)体现了“绿色化学”理念。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图是二氧化碳的实验室制备与性质实验,请回答相关问题。

①写出图中 m 的仪器名称:______________。
②用装置 A 制备二氧化碳,关闭 K2 和 K3 ,打开 K1 ,若用装置 E 所示的医用塑料袋排空气法收集 CO2 ,则E 装置_____(填“a”或“b”)端与 B 装置相连。
③现有 50g 含碳酸钙 20%的大理石样品,与足量的稀盐酸反应,能产生多少摩尔二氧化碳气体?_____(根据化学方程式列式计算)。
④打开 K2 、关闭 K1 和 K3 ,用于检验制取的二氧化碳性质。
若装置 C 中是紫色石蕊试剂,可观察到_______(填现象),证明二氧化碳与水发生了反应,反应的化学方程式为____________________;若装置 C 中试剂是澄清石灰水,则可看到的现象是___________,该反应的化学方程式是________________________。
⑤打开 K3 、关闭 K1 和 K2 ,观察到的实验现象是________,此实验说明二氧化碳具有的性质是__________。
⑥为了验证二氧化碳能与氢氧化钠溶液发生化学反应,设计实验,装置如下图:
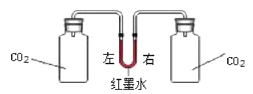
A B
A、B 瓶中装有等体积的二氧化碳气体,装置气密性良好,实验开始前红墨水左右两端液面相平。实验时同时向 A、B 瓶中分别加入等体积的氢氧化钠溶液和蒸馏水,塞紧瓶塞、震荡、平放,实验结束红墨水液面呈现________,证明二氧化碳与氢氧化钠溶液反应,发生反应的化学方程式是______。
-
科目: 来源: 题型:
查看答案和解析>>【题目】规范实验操作是实验成功的保证。你认为以下操作正确的是
A. 加热液体
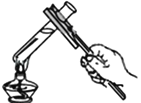 B. 检验装置气密性
B. 检验装置气密性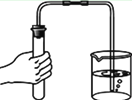
C. 氧气验满
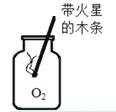 D. 滴加液体
D. 滴加液体
-
科目: 来源: 题型:
查看答案和解析>>【题目】2019年为“国际化学元素周期表年”。在元素周期表中硒元素的某些信息如图所示,下列说法不正确的是
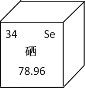
A. 硒原子中的质子数为34 B. 硒的原子序数是34
C. 硒的相对原子质量为78.96 g D. 硒属于非金属元素
相关试题

