【题目】请结合下列实验常用装置,回答有关问题。
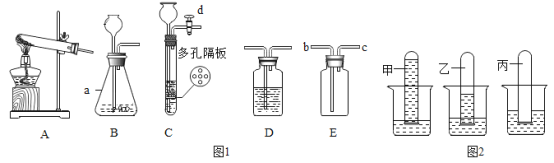
(1)写出图中标有字母仪器名称:a_____________
(2)若用B装置制取氧气,反应的方程式____________________________________
(3)若要制取氢气在B中装有锌粒,那么长颈漏斗中应加入___(填写试剂名称)反应的化学方程式是__果用E置收集该气体,气体从____(填“b或“c”)进入。
(4)实验室如用块状固体和液体无需加热制取难溶性气体,将B置改进为C装置 (多孔隔板用来放块状固体),其优点是____________
(5)某同学从图中选用适当装置成功的制备二氧化碳,该反应发生的化学反应的化学方程式为;_______为了进一步验证产生的气体是二氧化碳该同学将气体通入E装置中,则装置中应加入的试剂为 ________(填主要成分的化学式);发生化学反应的化学方程式为___________
(6)把甲、乙、丙三种气体的试管倒插在盛有水的烧杯中,一段时间后 , 观察到图2所示的现象。下列分析正确的是___(填字母代号 )
A. 甲、乙、丙气体都易溶于水 B.乙气体比甲气体更易溶于水
C. 不可用排空气法收集甲气体 D.可以采用排水集气法收集丙气体
参考答案:
【答案】锥形瓶 2H2O2![]() 2H2O+ O2↑ 稀硫酸 Zn + H2SO4 = ZnSO4 + H2↑ c 可以控制反应的发生和停止 CaCO3+2HCl=CaCl2+H2O+CO2↑ Ca(OH)2 CO2 +Ca(OH)2 =CaCO3↓+ H2O D
2H2O+ O2↑ 稀硫酸 Zn + H2SO4 = ZnSO4 + H2↑ c 可以控制反应的发生和停止 CaCO3+2HCl=CaCl2+H2O+CO2↑ Ca(OH)2 CO2 +Ca(OH)2 =CaCO3↓+ H2O D
【解析】
(1)标有字母a仪器名称为:锥形瓶;
(2)若用B装置制取氧气,反应物状态可以是固体与液体,不需加热,选用的药品是过氧化氢和二氧化锰,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,反应的化学方程式为:2H2O2![]() 2H2O+ O2↑;
2H2O+ O2↑;
(3)实验室是用锌粒和稀硫酸在常温下反应制氢气的,液体从长颈漏斗加入,该实验中长颈漏斗中应加入稀硫酸;反应的化学方程式为:Zn + H2SO4 = ZnSO4 + H2↑;氢气的密度比空气的密度小。如果用E装置收集该气体,则气体从c(短)管进入;
(4)在装置C中,固体药品物放在多孔隔板上,液体药品从长颈漏斗中加入。关闭开关时,试管中的气体增多,压强增大,把液体压入长颈漏斗,固体和液体分离,反应停止,打开开关时,气体导出,试管中的气体减少,压强减小,液体和固体混合,反应进行。实验室常用装置C代替装置B制取气体,装置C的优点是可以随时控制反应的发生与停止;
(5)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳能使澄清石灰水变浑浊,二氧化碳一般用澄清的石灰水检验,把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳,装置中应加入的试剂为Ca(OH)2;氢氧化钙与二氧化碳反应生成碳酸钙和水,反应的化学方程式为:CO2 +Ca(OH)2 =CaCO3↓+ H2O;
(6)观察图示可以看出:甲、乙试管倒插在盛有水的烧杯中,一段时间后,均有液体进入,说明这两种气体均能溶于水,而甲中进入的水比乙多,说明甲比乙更易溶于水,丙试管中几乎无液体进入,说明不溶于水,故可以采用排水集气法收集丙气体;由于不知甲能否与空气中成分反应,无法判断是否能用排空气法收集,故选D。
-
科目: 来源: 题型:
查看答案和解析>>【题目】用相应的化学用语回答;
(1)一个氢原子_________(2)三个碳酸根离子_________(3)标出二氧化碳中碳元素的化合价__(4)氧化铁的化学式_______
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图中A、B、C、D是四种粒子的结构示意图。
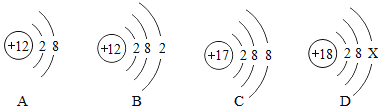
请回答下列问题:
(1)图中A、B、C、D属于_______种元素的粒子;
(2)A、B、C、D四种粒子中,不具备稳定结构的是_________(填序号);
(3)D中x=________;
(4)A与C形成化合物的化学式是___________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】A.C.D.E.各代表木炭、氧气、二氧化碳、一氧化碳、氧化铜中的一种,一定条件下,相连环物质间能发生反应(如图),其中A是能使澄清石灰水变浑浊的气体,C具有助燃性,则:
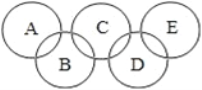
(1)下列物质的化学式分别是:A_____;E_____;
(2)写出其中的两个化学方程式:_________________________ __________________
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化学兴趣小组对某铜锌合金样品进行探究实验。称取样品10.0克,再用100.0克稀硫酸溶液逐滴滴入,实验情况如图所示。求:
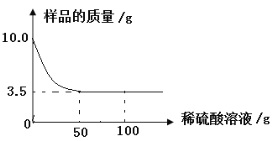
(1)铜锌合金汇中,Zn的质量分数是 。
(2)所用稀硫酸溶液中溶质的质量分数是多少?
-
科目: 来源: 题型:
查看答案和解析>>【题目】碘-131 是指相对原子质量为 131 的碘原子。下图是碘元素某些信息,不正确的是( )
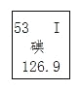
A. 图中的碘元素的原子相对原子质量为 126.9 克
B. 碘元素的原子的核电荷数为 53
C. 碘-131 的核内中子数为 78
D. 碘元素的原子的核外电子数为 53
-
科目: 来源: 题型:
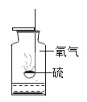
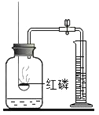
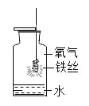
查看答案和解析>>【题目】下列实验指定容器中的水,其解释没有体现水的主要作用的是( )
实验
A
B
C
D
装置
解释
集气瓶中的水:吸 收放出的热量
量筒中的水:通过水 的体积变化得出 O2 的体积
集气瓶中的水:冷 却溅落熔融物,防 止集气瓶炸裂
集气瓶中的水:水 先将集气瓶内的空 气排净
A. A B. B C. C D. D
相关试题

