【题目】为测定某CuSO4溶液的溶质质量分数,化学小组的同学取CuSO4溶液100g,向其中滴加某一定质量分数的NaOH溶液,至不再产生沉淀为止,过滤,得到滤液175.1g和滤渣4.9g。请计算:
(1) 滤液中溶质的质量分数;
(2) NaOH溶液中溶质的质量分数。(写出计算过程)
参考答案:
【答案】(1) 4.1% (2) 5%
【解析】硫酸铜与氢氧化钠反应生成氢氧化铜沉淀和硫酸钠:CuSO4 + 2NaOH == Cu(OH)2↓+Na2SO4。向其中滴加某一定质量分数的NaOH溶液,至不再产生沉淀为止,过滤滤液是硫酸钠溶液,滤渣是沉淀氢氧化铜。利用化学方程式,根据反应的质量比即可计算出硫酸钠和氢氧化钠的质量。
解:设滤液中溶质硫酸钠的质量为x,氢氧化钠溶液中溶质的质量为y;
CuSO4 + 2NaOH == Cu(OH)2↓+Na2SO4
80 98 142
Y 4.9g x
![]() x=7.1g
x=7.1g
![]() y=4g
y=4g
滤液中溶质的质量分数=![]() 4.1%
4.1%
根据质量守恒定律化学反应前后物质的总质量不变,设加入的氢氧化钠溶液的质量为z,那么:100g+z=175.1g+4.9g ,z=80g
NaOH溶液中溶质的质量分数=![]() 5%
5%
答:略
-
科目: 来源: 题型:
查看答案和解析>>【题目】小明同学在理化实验考查中抽到的考题是“探究某种盐的性质”,他按照实验流程将一定质量未知白色固体溶于水配成溶液,再用贴有标号的3支试管分别取适量上述溶液,按照如图所示的方法进行试验。(氯化钙溶液呈中性)

实验现象:①溶液变红 ②_____________ ③产生白色沉淀
请你帮小明将实验现象补充完整。根据以上现象,小明得出结论:白色固体为碳酸钠。
考试结束后,小明和小伙伴们讨论结果,发现了两个问题,他们就这两个问题请教老师,并在老师的指导下继续进行了探究实验。
问题一:白色固体一定是碳酸钠吗?
小华认为有可能是碳酸钾,小红认为还有可能是碳酸钙,小明认为小红的说法一定不对,理由是_________________。
小明设计了方案定量研究:称取样品5.3g,加入足量的稀盐酸,产生气体的质量为2.2g。请你推断,该白色固体应为__________。

问题二:碳酸钠溶液为什么能使酚酞试液变红?
【提出问题】酚酞试液变红究竟与溶液中哪种微粒有关呢?
【进行实验】同学们取了三份酚酞试液进行如图实验:
(1) 实验1的目的是为了说明水分子不能使酚酞变红;
(2) 实验2的目的是为了说明___________________;
(3) 小明同学认为实验1没必要做,你认为小明的理由是_________;
(4) 实验3滴入碳酸钠溶液,振荡,酚酞试液变红,向变红后的溶液中再滴加过量的氯化钙溶液,振荡,观察到______________的现象。
【得出结论】酚酞试液变红与溶液中的__________(填离子符号)有关。
【实验反思】若将步骤(4)中的氯化钙溶液换成石灰水,能否得出同样的结论?_____(填“能”或“不能”),原因是________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质由分子构成的是
A. C60 B. 汞
C. 铁 D. 硫酸铜
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质中属于氧化物的是
A.臭氧O3 B.冰 C.碳酸钙 D.食盐水
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲、乙两种物质的溶解度曲线如图所示。下列叙述正确的是
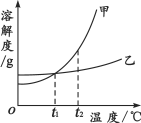
A.将甲的溶液从t2℃降到t1℃,其溶质的质量分数一定减小
B.t2℃时,甲、乙的饱和溶液各100 g,其溶质的质量一定相等
C.当温度高于0℃而低于t1℃时,乙的溶解度比甲的溶解度大
D.t2℃时,蒸发溶剂可使乙的饱和溶液析出晶体后变为不饱和溶液
-
科目: 来源: 题型:
查看答案和解析>>【题目】地壳中含量最多的金属元素是
A. 硅 B. 铁
C. 铝 D. 钙
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列处理事故的方法正确的是
A. 家用电器着火时,立即用水扑灭 B. 室内起火时,立即打开门窗通风
C. 炒菜时油锅着火,立即浇水灭火 D. 扑灭森林火灾时,设置隔离带
相关试题

