【题目】(7分)使用密度小、强度大的镁合金能减轻汽车自重,从而减少汽油消耗和废气排放。
![]() (1)镁元素在自然界中是以(填“单质”或“化合物”)形式存在。
(1)镁元素在自然界中是以(填“单质”或“化合物”)形式存在。
(2)工业制镁的一种原理是2MgO+Si+2CaO ====== 2Mg↑+Ca2SiO4,抽走容器中的空气对反应有促进作用,且能防止空气中的物质与Mg反应使产品混有 (填化学式)。
(3)制镁的原料MgO可从海水中获得。小华利用镁与盐酸反应后的废液,模拟从海水中获取MgO的过程,实验如下:
步骤1:向上述废液中,边搅拌边分批加入CaO,至MgCl2完全沉淀为止,过滤得Mg(OH)2固体。共消耗8.4g CaO。
步骤2:将Mg(OH)2固体加热分解为MgO和水,所得MgO的质量为4.0g 。
①步骤2中Mg(OH)2分解的化学方程式为 。
②通过所得MgO的质量计算上述废液中含MgCl2的质量m=g。
③分析实验数据,可知步骤Ⅰ中反生的化学反应有:
CaO+H2O==Ca(OH)2;Ca(OH)2+MgCl2==CaCl2+Mg(OH)2↓; 。
参考答案:
【答案】(1)化合物;(2)氧化镁、氮化镁或者碳; (3)①Mg(OH)2△MgO+ H2O; ②9.5 ; ③CaO+2HCl==CaCl2+ H2O。
【解析】
试题分析: (1)镁的化学性质比较活泼,镁元素在自然界中主要以化合物形式存在;(2)镁能与空气中的氧气、氮气和二氧化碳反应,使镁产品中混有氧化镁、氮化镁和碳;(3)①Mg(OH)2属于不溶性碱,受热分解能生成氧化镁和水,Mg(OH)2△MgO+ H2O;②已知氢氧化镁分解所得MgO的质量,利用镁元素质量守恒可以计算上述废液中含MgCl2的质量:镁元素质量=4.0g×![]() ×100%=2.4g ,故氯化镁的质量为2.4g÷
×100%=2.4g ,故氯化镁的质量为2.4g÷![]() ×100%=9.5g;③由生成氯化镁9.5g 再结合CaO+H2O==Ca(OH)2,Ca(OH)2+MgCl2==CaCl2+Mg(OH)2↓,可以求得所用的氧化钙质量为5.6g,而题给质量为8.4g,故氧化钙还与其他物质发生了化学反应:氧化钙是金属氧化物,能与废液中的盐酸反应生成氯化钙和水, CaO+2HCl==CaCl2+ H2O。
×100%=9.5g;③由生成氯化镁9.5g 再结合CaO+H2O==Ca(OH)2,Ca(OH)2+MgCl2==CaCl2+Mg(OH)2↓,可以求得所用的氧化钙质量为5.6g,而题给质量为8.4g,故氧化钙还与其他物质发生了化学反应:氧化钙是金属氧化物,能与废液中的盐酸反应生成氯化钙和水, CaO+2HCl==CaCl2+ H2O。
-
科目: 来源: 题型:
查看答案和解析>>【题目】今年的6月5日是世界第45个“世界环境日”,我国今年的主题是“改善环境质量,推动绿色发展”.下列做法不符合这一主题的是
A. 推广使用节能灯和太阳能路灯
B. 实行垃圾分类和回收
C. 减少使用农家肥,大量使用化肥和农药
D. 出行方式尽量采用步行、骑自行车或乘公交车
-
科目: 来源: 题型:
查看答案和解析>>【题目】现有Na2S、Na2SO3组成的混合物,经测定其中硫元素的质量分数为32%,则该混合物中钠元素的质量分数为
A. 46% B. 48% C. 50% D. 52%
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列变化中,属于化学变化的是
A. 冰雪融化 B. 粮食酿酒 C. 橙子榨汁 D. 品红扩散
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列关于“不一定”的说法中,不正确的是
A. 含氧化合物不一定是氧化物
B. 由分子构成的纯净物不一定只含一种分子
C. 氧化反应不一定是化合反应
D. 质子数相等的粒子不一定是同种元素
-
科目: 来源: 题型:
查看答案和解析>>【题目】(10分)实验室部分装置如图所示,请回答下列问题。
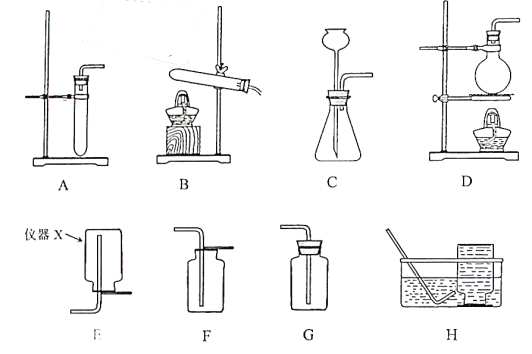
(1)仪器X的名称是 。
(2)实验室用CaCO3和稀盐酸制备CO2的化学方程式为 ,若需制备22g CO2,不计实验损耗,至少需要消耗 g CaCO3。
(3)①用大理石和稀盐酸制取CO2时,能作为发生装置的是 、 (填字母,下同)。
②若要制备多瓶CO2,并在制取过程中便于补充稀盐酸,发生装置应选择 ,收集装置应选择 。
(4)实验室通过加热亚硝酸钠和氯化铵的混合溶液制取并收集N2时,应选择 与
组合而成的装置。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(10分)组成相似的盐具有一些相似的化学性质。
(1)①Cu(NO3)2溶液和CuSO4溶液都含有大量 (填离子符号)。
②向Cu(NO3)2溶液中加入NaOH溶液,充分振荡。反应的化学方程式为 。
③向CuSO4溶液中加入过量的锌片,充分反应后,可看到的现象是 ,下图表示该反应前后溶液中存在的主要离子,请写出每种图形代表的离子(填离子符号)

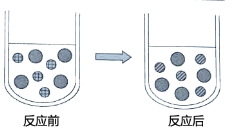
(2)除上述实验外,在溶液中与Cu(NO3)2和CuSO4均能反应的物质还有 、
(任举二例,填化学式,下同)
(3)在溶液中能与CuSO4反应而不与Cu(NO3)2反应的物质有 (任举一例)。
相关试题

