【题目】下图是实验室配制一定溶质质量分数的NaCl溶液的流程图。
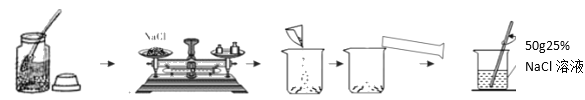
请回答:
(1)应称量________gNaCl,需加水________mL。
(2)若称量NaCl固体时指针向右偏转,则应_____直到天平平衡。
(3)取上述溶液20g加入蒸馏水,稀释到_______g,可得到5%的NaCl溶液。
参考答案:
【答案】12.5 37.5 继续向左盘添加氯化钠 80
【解析】
(1)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得水的质量。
(2)使用托盘天平称量药品时应遵循“左物右码”,指针偏右,说明药品质量小于砝码质量,据此进行分析解答。
(3)根据溶液稀释前后溶质的质量不变,进行分析解答。
(1)溶质质量=溶液质量×溶质的质量分数,配制10%的氯化钠溶液50g,需氯化钠的质量=50g×25%=12.5g;溶剂质量=溶液质量-溶质质量,则所需水的质量=50g-12.5g=37.5g(合37.5mL)。
(2)在称量氯化钠固体的过程中,步骤应该是:先调好砝码和游码,然后向左边托盘添加固体物质;若发现指针向右偏转,说明固体物质药品的质量小于砝码的质量,故应继续向左盘添加氯化钠,直至天平平衡。
(3)设要加水的质量为x,根据溶液稀释前后溶质的质量不变,
则20g×25%=(20g+x)×5%
x=80g
故取上述溶液20g加水稀释到20g+80g=100g。
答案:
(1)12.5; 37.5;
(2)继续向左盘添加氯化钠;
(3)100
-
科目: 来源: 题型:
查看答案和解析>>【题目】某校化学研究性学习小组探究气体制取的实验原理与方法.
(1)甲同学将课本的基础知识进行整理如图,请你帮助他完成相关内容.

制取气体
所需要品
装置连接顺序
反应的化学方程式
二氧化碳(干燥)
大理石和稀盐酸
______________
______________________________
(2)乙同学设计的实验装置(如图),既可用于制取气体,又可用于验证物质性质.当打开K1、关闭K2时,利用I、Ⅱ装置可直接进行的实验是______________(填序号).

①大理石与稀盐酸反应制取二氧化碳
②锌与稀硫酸反应制取氢气
(3)丙同学认为在不改变I、Ⅱ、Ⅲ装置的仪器及
位置的前提下,该装置可用于过氧化钠(Na2O2)与水反应制取氧气,另一产物为氢氧化钠,则该反应的化学方程式为:______________________________;她的改进措施是_______________________________________________________.
(4)丁同学打开K2、关闭K1,利用I、Ⅲ装置来验证生成的二氧化碳中含有水蒸气,此时C中盛放的物质是_______________,可以观察到的现象是________________________________________.
(5)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应)作如下回收处理:
①通过以下四步实验操作回收二氧化锰.正确操作的先后顺序是____________(填写选项序号).
a.烘干b.溶解c.过滤d.洗涤
②用所得氯化钾晶体配制50g质量分数为5%的氯化钾溶液,需要氯化钾的质量为_______g.
③过滤、蒸发时都需用到的仪器是__________(填序号).
A.酒精灯B.烧杯C.玻璃棒D.漏斗E.量筒
(6)小明用6.5g可能含有铜、铝、铁、镁中的一种或几种金属杂质的锌粉,跟足量的稀盐酸完全反应时,生成0.2g氢气,则此锌粉中一定含有的金属杂质是________________.
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化学反应的微观示意图如下。
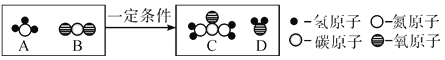
请回答:
(1)C 为尿素[CO(NH 2 ) 2 ],农业上常用作____(填“氮”“磷”或“钾”)肥
(2)上图所示物质中属于氧化物的是____ (填字母序号)
(3)该反应的化学方程式是______。
-
科目: 来源: 题型:
查看答案和解析>>【题目】右图是包含物质A、B、C、D和盐酸卡片的“化学拼图”,相邻两张卡片所标的物质(或其溶液)间能发生反应。
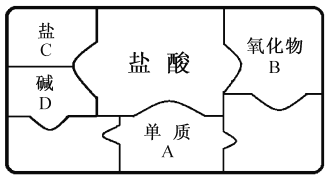
(1)A不可能是______(填标号)。
a.Mg b.Fe c.Ag d.Zn
(2)若B为铁锈的主要成分Fe2O3,B与盐酸反应的化学方程式为______。
(3)若C为碳酸钠
①C与D的反应属于______(填基本反应类型)。
②D与盐酸反应的化学方程式为______(写一个)。
③将二氧化碳通入C溶液,可化合生成碳酸氢钠( NaHCO3),该反应的反应物有______种。
-
科目: 来源: 题型:
查看答案和解析>>【题目】A~F是碳单质、氧化铜、二氧化碳、稀硫酸、氢氧化钠和碳酸钠六种物质中的某一种,A、B都是黑色固体,E属于盐,它们之间的相互关系如图所示(实连线“—”表示物质间能反应,虚连线“ ”表示物质间不能反应)。请回答下列问题:
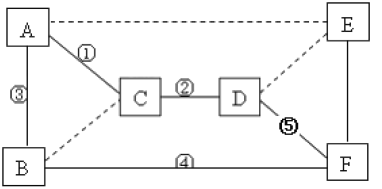
(1)C的化学式是__________。
(2)B与F反应的化学方程式为________。
(3)E与F反应的化学方程式为_______。
(4)上图关系中________(从①~⑤中选填序号)的反应属于中和反应。
(5)在上图中,三个虚线连接中存在转化关系的有(填物质化学式):____→___;___→____。
-
科目: 来源: 题型:
查看答案和解析>>【题目】粗盐中含有MgCl2、CaCl2等杂质,工业提纯粗盐的工艺流程如下图所示:
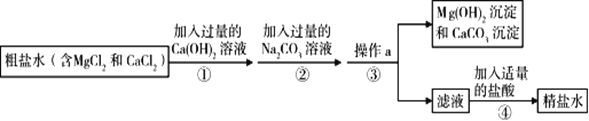
(1)Ca(OH)2俗称:____,其溶液的pH____7(选填“>”“<”或“=”)。①反应的化学方程式为_____。
(2)步骤②操作a的名称是___。步骤④加入适量盐酸的目的是除去滤液中的___和___(填化学式)。
(3)若步骤①和步骤②的顺序颠倒,则最后所得的精盐水中还含有____。
(4)将精盐水制成食盐晶体的方法是___。
-
科目: 来源: 题型:
查看答案和解析>>【题目】小明、小芳二位同学为探究稀硫酸的化学性质,做了如下实验:
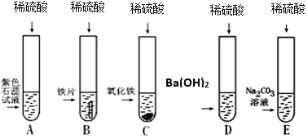
(1)试管A中的现象是____,反应后试管B中一定有的阳离子是____(写离子符号)。
(2)试管C中反应的化学方程式为_____。
(3)试管D中反应的化学方程式为____。
小芳同学把反应后D、E试管中的废液倒入一个洁净的烧杯中,过滤,得到白色沉淀和无色滤液,她决定对白色沉淀的成分进行探究。
(查阅资料)硫酸钡不溶于酸。
(作出猜想)I.BaSO4;II.BaCO3;III._____。
(拓展与反思)猜想II不成立,原因是_____。
(实验方案)
实验操作
实验现象与结论
过滤、洗涤白色沉淀备用;向白色沉淀中加入盐酸至过量
①若沉淀全部不溶解;猜想Ⅰ成立;
②若____,且有气泡产生,猜想III成立,其化学反应方程式为____。
相关试题

