【题目】某兴趣小组用下图所示流程制取氧气,并回收提纯氯化钾和二氧化锰。
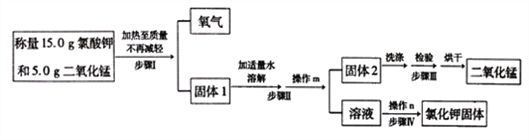
回答下列问题:
(1)固体1中二氧化锰的质量分数_______________25%(填=、<或>)。
(2)在回收提纯的过程中需要控制水的用量,原因有____________(填标号)。
A.提高实验效率 B.保证固体1全部溶解 C.节约能源
(3)步骤Ⅱ中的操作m应选择图中______(填“甲”或“乙”)装置,该操作中玻璃棒的作用是______________________________ 。操作n中,当观察到__________________________时即停止加热。

(4)实验结束后,称得回收到的氯化钾的质量比理论值小,可能的原因是________________________(写一点)
参考答案:
【答案】 > A 甲 引流 大量固体析出时 过滤时有部分药品残留在滤纸上(合理即可)
【解析】(1)由题中信息可知可知,反应前固体混合物中二氧化锰占25%,反应后由于生成氧气,固体1的质量小于原固体质量,而二氧化锰的质量不变,二氧化锰的质量分数大于25%;(2)在回收提纯的过程中需要控制水的用量,原因有如果水的量太少,不能将氯化钾全溶解,若果用量太多,过滤用时太多;(3)步骤Ⅱ中的操作m是将难溶性固体与液体分离,应用过滤操作,应选择图11中甲装置,该操作中玻璃棒的作用是引流。蒸发操作中,当观察到有大量晶体析出时即停止加热。(4)实验结束后,称得回收到的氯化钾的质量比理论值小,可能的原因是有部分氯化钾没有溶解过滤时有部分药品残留在滤纸上(也可能是蒸发结晶时停止加热太早,使氯化钾析出的少)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室内用块状固体碳化钙制取乙炔(C2H2),该反应比二氧化锰催化过氧化氢分解更加激烈,所选发生装置最合适的是( )

A. A B. B C. C D. D
-
科目: 来源: 题型:
查看答案和解析>>【题目】合成纤维具有的特性是( )
①强度高,②弹性好,③耐磨,④透气性好,⑤吸水性好,⑥耐化学腐蚀
A.①②③④ B.④⑤⑥ C.④⑤ D.①②③⑥
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列做法不会对环境造成危害的是( )
A.使用后的塑料袋随意丢弃
B.大量使用化肥农药
C.工业废水、生活污水处理达标后排放
D.废旧电池已无用处,不需要回收
-
科目: 来源: 题型:
查看答案和解析>>【题目】用如图所示装置,在常温下,进行研究氧气性质的实验.

内容步骤
【实验1】研究氧气性质
Ⅰ
烧杯中盛有石灰水,燃烧匙中放入木炭,点燃木炭后,迅速将燃烧匙伸入瓶中,塞紧瓶塞
Ⅱ
推入适量H2O2 溶液
(1)实验1中,推入H2O2溶液后,集气瓶中现象是_______________________________;推入H2O2溶液后,观察到烧杯中的现象是____________________。
(2)推入H2O2溶液后,观察到木炭燃烧得更剧烈,由此得出氧气的性质是_________;木炭熄灭后冷却一段时间,烧杯中的部分溶液流入集气瓶.该实验中,集气瓶内压强的变化过程是__________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下列装置图回答问题:
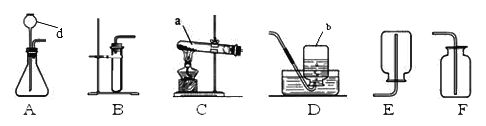
(1)指出仪器的名称: a______________、d______________;
(2)用D装置收集某气体时,如何判断发生装置中水已排尽:_____________;
(3)实验室用氯酸钾和二氧化锰制取并收集干燥的氧气应选用的装置是_________ (填编号)。该反应中二氧化锰的作用是_______________,该反应属于_______反应类型。用B装置制取氧气结束后,分离出二氧化锰的操作是_____________。
(4)氨气是一种无色,有刺激性气味,密度比空气小,极易溶于水的气体,其水溶液称为氨水。实验室用氯化铵和消石灰的固体混合物加热制取氨气,应选择的发生装置是_____,收集装置是__________。
(5)装置A、B都可用于实验室制取氧气。使用装置A制取时,d的下端管口必须_______________,目的是______________________________。使用装置A比用装置B制取气体优点是______________________。有一名同学欲用G装置收集一瓶纯净的氧气,他的操作方法是______________________________。
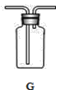
(6)现有一瓶用排水法收集的甲烷气体(图1中的A)。
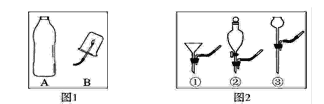
要将A中的气体通入B装置中,应选图2中的______(填序号)“注水装置”最佳。
-
科目: 来源: 题型:
查看答案和解析>>【题目】新药帕拉米韦(化学式为C15H28O4N4)注射液可用于治疗H7N9型禽流感。下列关于帕拉米韦的说法正确的是(相对原子质量:C—12、H—1、O—16、N—14)
A.帕拉米韦的相对分子质量为328 g
B.帕拉米韦是由15个碳原子、28个氢原子、4个氧原子、4个氮原子构成的
C.帕拉米韦是由碳、氢、氧、氮四种元素组成的
D.帕拉米韦中碳元素的质量分数为
 ×100%
×100%
相关试题

