【题目】课外活动小组的同学为确定某硫酸钠和氢氧化钠固体混合物中硫酸钠的含量,他们取10g该固体混合物与98g质量分数为10%的稀硫酸恰好完全反应.求:
(1)原混合物中硫酸钠的质量分数;
(2)反应后所得溶液中溶质的质量分数.
参考答案:
【答案】(1)20% (2)15%
【解析】本题是溶质质量分数与化学方程式相结合的计算,计算中要弄清反应后溶液中溶质的来源。
设参加反应氢氧化钠质量为x,反应生成硫酸钠的质量为y
2NaOH+H2SO4═Na2SO4+2H2O
80 98 142
x 98g×10% y
![]()
x=8g y=14.2g
(1)原混合物中硫酸钠的质量分数=![]() ×100%=20%
×100%=20%
(2)反应后所得溶液中溶质的质量=10g﹣8g+14.2g=16.2g,故反应后溶液的质量分数=![]() ×100%=15%
×100%=15%
答:(1)原混合物中硫酸钠的质量分数为20%;
(2)反应后所得溶液中溶质的质量分数为15%.
-
科目: 来源: 题型:
查看答案和解析>>【题目】科学家在合成超导材料时,偶然制得了在自然界中尚未发现的紫色合成物质BaCuSi2O6,它由______种元素组成,一个分子中有______个原子。写出与该物质相同价态硅元素的氧化物的化学式________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列做法有利于保护环境的是
A. 工厂废气直接排放 B. 废旧电池回收处理
C. 生活污水任意排放 D. 随意丢弃塑料袋
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列对水的叙述正确的是
A. 水的三态变化,能实现水的自身净化和水资源的重新分配
B. 水的三态变化,是由于水分子的体积改变
C. 过滤和吸附能除去水中所有的杂质
D. 水是由氢气和氧气组成
-
科目: 来源: 题型:
查看答案和解析>>【题目】(6分)某化学小组围绕燃烧与灭火的主题开展了相关活动。请你参与完成:
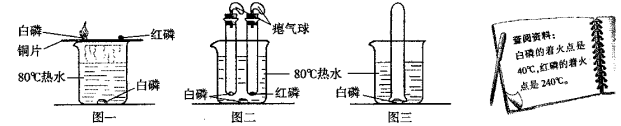
【知识回忆】可燃物燃烧的必备条件是 ;
【交流讨论】(1)改进后的装置(如图二)与图一相比,其优点是 。欲使图二中的红磷着火,可将试管从水中取出并 后才能对试管加热;
(2)将装有某气体的大试管口朝下垂直插入水中,使试管罩住白磷(如图三所示),结果观察到了“水火相容”的奇观,则大试管所装气体可能是 ;
【综合应用】“水火不相容”是指水能灭火,其实水有时也可以“生火”,比如钾遇水会立刻着火,因为钾遇水生成H2和一种碱(化学式为KOH),该反应是 (填“吸热”或“放热”)反应,其反应化学方程式为 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质是由分子构成的是( )
A.二氧化碳 B.金刚石 C.铁 D.氯化钠
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列属于非金属元素的是
A. 钠 B. 镁 C. 铜 D. 硅
相关试题

