【题目】氢气作为新能源有很多优点,制取与储存氢气是氢能源利用领域的研究热点。
I.制氢:铁酸锌(ZnFe2O4)可用于循环分解水制气,其反应可表示为: 6ZnFe2O4![]() 6ZnO+4Fe3O4+O2↑;3ZnO+2Fe3O4+H2O
6ZnO+4Fe3O4+O2↑;3ZnO+2Fe3O4+H2O![]() 3ZnFe2O4+H2↑
3ZnFe2O4+H2↑
(1)ZnFe2O4中Fe的化合价为_______________。
(2)该循环制氢中不断消耗的物质是________(填化学式),得到H2和O2的质量比为__________。
(3)氢气作为新能源的优点有________(任写一点)。该循环法制氢的不足之处是________。
Ⅱ.贮氢:合金Mg2Cu是一种潜在的贮氢材料,高温时在氩气保护下,由一定质量比的Mg、Cu单质熔炼获得。该合金在一定条件下完全吸氢生成氢化物和另一种合金,其化学方程式为: 2Mg2Cu+ 3H2![]() 3MgH2+MgCu2
3MgH2+MgCu2
(4)熔炼制备Mg2Cu合金时,通入氩气的目的是_________________。
(5)氢化物MgH2与水反应生成一种碱,并释放出H2。 其化学反应方程式为________。
(6)11.2g Mg2Cu完全吸氢后所得混合物与过量盐酸反应,放出H2的质量为________g。
参考答案:
【答案】 +3 H2O 1:8 不污染环境、热值大、原料来源丰富 能耗高 起到保护作用,防止金属被氧化 MgH2+2H2O=Mg(OH)2↓+2H2↑ 0.7g
【解析】本题考查了有关元素化合价的计算,氢能源,化学方程式的书写,根据化学方程式的计算。难度较大,仔细审题,找出的用的信息结合已有知识进行分析解答。
(1)ZnFe2O4中锌的化合价为+2价,氧元素的化合价为﹣2,设:Fe的化合价为x,根据化合物中元素化合价的代数和为零,则有(+2)+2x+(﹣2)×4=0,x=+3;
(2)根据化学方程式6ZnFe2O4![]() 6ZnO+4Fe3O4+O2↑;3ZnO+2Fe3O4+H2O
6ZnO+4Fe3O4+O2↑;3ZnO+2Fe3O4+H2O![]() 3ZnFe2O4+H2↑可知,该循环制氢中不断消耗的物质是水,其化学式为H2O,得到H2和O2的质量比为4:32=1:8;
3ZnFe2O4+H2↑可知,该循环制氢中不断消耗的物质是水,其化学式为H2O,得到H2和O2的质量比为4:32=1:8;
(3)氢气作为新能源的优点有不污染环境、热值大、原料来源丰富,该循环法制氢时都是在高温下进行,不足之处是能耗高;
(4)高温时Mg、Cu都能与空气中氧气反应,熔炼制备Mg2Cu合金时,通入氩气可以起到保护作用,防止金属被氧化;
(5)氢化物MgH2与水反应生成一种碱,并释放出H2,根据质量守恒定律可知,生成的碱是氢氧化镁,化学反应方程式为 MgH2+2H2O=Mg(OH)2↓+2H2↑;
(6)11.2g Mg2Cu完全吸氢后所得混合物与过量盐酸反应,其中的氢化镁与水反应生成氢氧化镁和氢气,MgCu2中只有镁与盐酸反应产生氢气。
设:11.2g Mg2Cu完全吸氢后生成氢化镁的质量为x,MgCu2的质量为y。
2Mg2Cu+3H2 ![]() 3MgH2+MgCu2
3MgH2+MgCu2
224 78 152
11.2g x y
![]() x=3.9g
x=3.9g
![]() y=7.6g
y=7.6g
设:3.9g氢化镁与水反应生成氢气的质量为a
MgH2+2H2O=Mg(OH)2↓+2H2↑
26 4
3.9g a
![]() a=0.6g
a=0.6g
7.6gMgCu2含有镁的质量为:7.6g×![]() × 100%=1.2g
× 100%=1.2g
设:1.2g的镁与盐酸反应生成的氢气质量为b
Mg+2HCl═MgCl2+H2↑
24 2
1.2g b
![]() b=0.1g
b=0.1g
生成氢气的质量为:0.6g+0.1g=0.7g。
-
科目: 来源: 题型:
查看答案和解析>>【题目】铜元素有多种氧化物,如CuO、Cu2O.称取14.4g仅含Cu、O两种元素的固体样品、采用如下装置实验(夹持装置省略)。测得实验前后装置B增重4.4g。下列说法正确的是( )
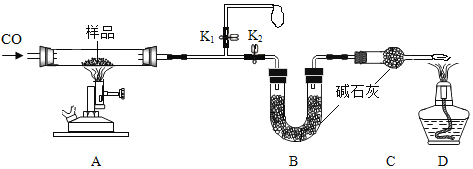
A. 装置B的作用是吸收反应生成的H2O和CO2
B. 实验开始前应先关闭K2,打开K1,让CO通一段时间
C. 根据实验数据进行计算,可以确定该固体为Cu2O
D. 若缺少装置C,则实验所得Cu、O个数比偏高
-
科目: 来源: 题型:
查看答案和解析>>【题目】氧气是我们身边无法离开的物质。某兴趣小组对氧气的研究如下:
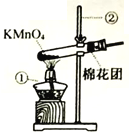
I.氧气的制备:
(1)写出上图中有标号仪器的名称:①___________,②__________。
(2)写出用KMnO4制取O2的化学反应方程式__________________。该装置中棉花团的作用是_________________,图中装置一处明显的错误是______________。
II.氧气的收集:
[实验1]用向上排空气法收集氧气,当放置在集气瓶口带火星木条复燃时停止收集,测定瓶中氧气的含量,重复实验3次。
[实验2]用向上排空气法收集氧气,当放置在集气瓶口带火星木条复燃后,继续收集40秒,测定瓶中氧气的含量,重复实验3次。
[实验3]用排水法收集氧气,测定瓶中氧气的含量,重复实验3次。
实验数据:
实验1
实验2
实验3
氧气的体积分数(%)
79.7
79.6
79.9
88.4
89.0
87.9
90.0
89.8
89.3
氧气的平均体积分数(%)
79.7
88.4
89.7
数据
(3)由实验1、2可知,用向上排空气法收集氧气时,为提高获得的氧气体积分数,可采取的措施是_______________。
(4)不考虑操作因素,实验3获得的氧气体积分数不能达到100%的主要原因是_______。
Ⅲ.铁丝在氧气中燃烧
(5)铁丝在纯净氧气中燃烧的化学反应方程式为________________________。
(6)铁丝燃烧时火星四射,经研究表明产生火星四射现象的原因,可能是同时生成了某种气体,推测该气体是_____________(填化学式)。将燃烧后的黑色固体粉碎后,滴加稀盐酸,若产生气泡,则原因是________________(用化学反应方程式表示)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】空气是宝贵的自然资源,下图是以空气等为原料合成尿素[CO(NH2)2]的流程。请按要求回答相关问题:

(1)空气属于__________(填“纯净物”或“混合物”),X是空气中含量最多的气体,其分子式为________________。
(2)图中分离空气的过程属于________变化(填“物理”或“化学”)。
(3)空气中含有的少量稀有气体的化学性质_________(填“活泼”或“稳定”)。
(4)实验室用大理石和稀盐酸制取二氧化碳的化学反应方程式为_____________;二氧化碳的密度比空气__________(填“大”或“小”)。
(5)①天然气的主要成分是CH4,天然气属于__________再生资源(填“可”或“不可”)。
②点燃CH4之前应__________。 8g CH4完全燃烧消耗32gO2,生成agCO2和18gH2O,则a=__________。
③由CH4在该流程中的作用表明:化学反应中发生物质变化的同时也会伴随有________变化(填“能量”或“原子个数”)。
(6)尿素属于_______(填“氮肥”、“磷肥”或“钾肥”);写出NH3合成尿素的化学反应方程式_____________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某工厂产生的废渣主要成分是含钙的化合物(杂质为Fe2O3)。用该废渣制取CaCl2晶体(CaCl2·xH2O)并进行组成测定,其制取的流程如下图所示:
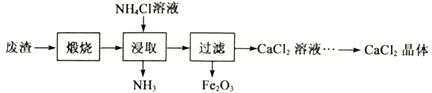
已知:NH4Cl溶液显酸性,且浓度越高酸性越强
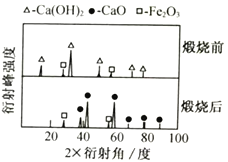
(1)XRD图谱可用于判断某固态物质是否存在。右图为煅烧前后废渣的XRD图谱。写出煅烧时发生的化学反应方程式________________________________。
(2)浸取时需连续搅拌,其目的是_________________;生成的NH3能使湿润的红色石蕊试纸变____________色。
(3)在其它条件相同的情况下,CaCl2的产率随浸取温度的变化如下图所示。则宜选择的浸取温度为____________℃左右。
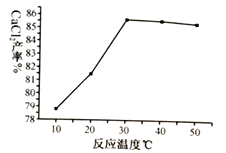
(4)若使用过量浓度较高的NH4Cl溶液,则所得CaCl2溶液中会含有NH4Cl、_______(填化学式)等杂质。
(5)过滤得到的Fe2O3在高温下可与CO反应,写出该反应的化学方程式____________。
(6)测定晶体(CaCl2·xH2O)的组成:
a.称取14.7000g CaCl2晶体于锥形瓶内,加入适量蒸馏水.使其全部溶解。
b.再向其中加入足量的Na2CO3溶液,静置。
C.过滤、洗涤、干燥、称量,得到10.0000g固体。
①通过计算,确定x的值(写出计算过程)。______________________。
②判断步骤b中沉淀完全的方法是:静置,向上层清液中滴加__________,则说明已沉淀完全;若沉淀不完全,则测得的x值比实际值______(填“偏大”、“偏小”或“ 不变”。
-
科目: 来源: 题型:
查看答案和解析>>【题目】为探究物质溶解过程中的能量变化,某同学设计图I所示装置。在盛有水的烧杯中放入一装有饱和硝酸钾溶液的试管,向水中加入足量物质X,搅拌。结合图II硝酸钾溶解度曲线,对硝酸钾溶液变化的推断,合理的是
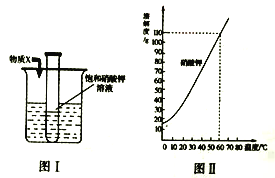
①X为NaCl固体试管中无晶体析出,硝酸钾溶液仍是饱和溶液
②X为NaOH固体,试管中无晶体析出,硝酸钾溶液仍是饱和溶液
③X为NH4NO3晶体,试管中有晶体析出,硝酸钾溶液仍是饱和溶液
④X为浓H2SO4,试管中无晶体析出,硝酸钾溶液为不饱和溶液
A. ①②③ B. ①③④ C. ①②④ D. ②③④
-
科目: 来源: 题型:
查看答案和解析>>【题目】分别向50gFeSO4和CuSO4溶液中,加入一定质量Mg粉恰好完全反应。随Mg粉消耗,Mg粉与帶液中FeSO4、CuSO4的质量变化见图。请读取图象信息并结合金属活动性服序分析,下面说法不合理的是
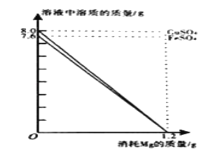
A. 反应前,溶液中溶质质量分数:FeSO4<CuSO4
B. 反应后,两容液底部分别析出的金属是Fe和Cu
C. 反应后,两溶液底部析出金属的质量:Fe<Cu
D. 反应后,若FeSO4和CuSO4对应新溶液的溶质质星分数分别为A、B,则A>B
相关试题

