【题目】四种物质在一定的条件下充分混合反应,测得反应前后各物质的质量分数如图所示。则下列有关说法中不正确的是
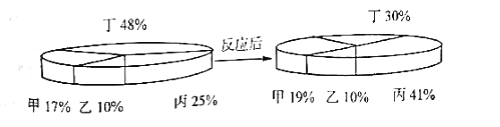
A. 生成的甲、丙两物质的质量比例为1:8 B. 乙一定是这个反应的催化剂
C. 甲可能是单质 D. 参加反应的丁的质量一定等于生成甲和丙的质量之和
参考答案:
【答案】B
【解析】由四种物质反应前后各物质的质量分数可知,反应前后甲的质量分数增加了19%17%=2%,故甲是生成物;乙的质量分数不变,可能作该反应的催化剂,也可能没有参加反应;丁的质量分数减少了48%30%=18%,故丁是反应物;丙的质量分数增加了41%25%)=16%,丙是生成物。A、生成的甲、丙两物质的质量比为(19%17%):(41%25%)=1:8,正确; B、乙的质量分数不变,可能作该反应的催化剂,也可能没有参加反应,错误;C、该反应的反应物为丁,生成物是甲和丙,符合“一分多”的特征,属于分解反应,所以甲可能是单质,正确;D、 该反应的反应物为丁,生成物是甲和丙,根据质量守恒定律,参加反应的丁的质量一定等于生成甲、丙的质量之和,正确。
故选B。
-
科目: 来源: 题型:
查看答案和解析>>【题目】以下是初中化学一些基本实验,请根据实验内容回答下列问题:
(1)利用下图进行粗盐中难溶性杂质去除和配制一定质量分数氯化纳溶液的实验。
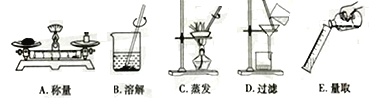
①粗盐中难溶性杂质去除的主要操作顺序是_____________(填字母序号);
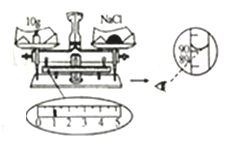
②配制11%的氯化钠溶液100g。如按下图进行称量和量取,其它操作均规范无误,最终导致配制的氯化钠溶液的溶质质量分数______(填“大于”、“小于”或”不能确定”)11%。
(2)下图为某小组探究金属化学性质的两组实验。
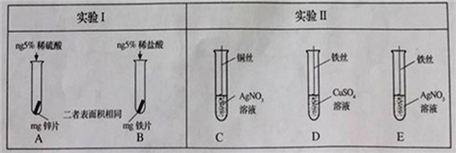
①实验I中以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不够合理,理由是____________________________________;
②写出实验II中C试管内反应的化学方程式____________________________;
③实验II中要验证Cu、Fe、Ag的金属活动性顺序,至少要做的实验是_____(填字母序号)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化学兴趣小组的同学,通过咨询老师准备用亚硫酸钠溶液与浓硫酸反应来制备一定量的SO2(Na2SO3+H2SO4(浓)==Na2SO4+SO2↑+H2O]。老师给他们提供了一瓶亚硫酸钠溶液并告知该瓶溶液放置时间可能较长,不知是否变质。兴趣小组的同学分成甲、乙两小组对该瓶亚硫酸钠溶液成分进行实验探究。
(提出问题)①该瓶溶液中溶质的成分是什么?
②该瓶溶液中亚硫酸钠的质量分数是多少?
(查阅资料)
(1) Na2SO3有较强还原性,在空气中易被氧气氧化:2 Na2SO3+O2==2Na2SO4;
(2) Na2SO3能与酸反应产生SO2气体;
(3)SO32-、SO42-均能与Ba2+反应产生白色沉淀,BaSO3可溶于稀盐酸。
(作出猜想)
猜想1:没有变质,成分是Na2SO3;
猜想2完全变质,成分是Na2SO4;
你认为还可能有的猜想3:_____________________。
(实验探究I)甲、乙两组分别进行实验探究溶液是否变质:
小组
实验操作
现象
结论
甲组
取少量样品于试管中加入过量稀盐酸;
产生气泡
没有变质,还是Na2SO3
乙组
取少量样品于试管中加入氯化钡溶液,再加入足量稀盐酸。
_____
已部分变质
(评价)有同学质疑甲组方案不合理,理由是___________。
(实验探究II)
甲组设计如下实验测定Na2SO3溶液的溶质质量分数。(注:空气中二氧化碳的影响忽略不计)
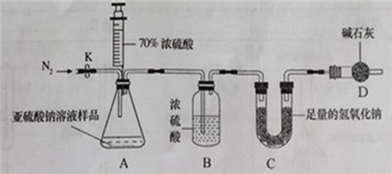
(1)连好装置并检查装置气密性,在锥形瓶中放入126g该样品
(2)实验前称量C装置的质量;
(3)关闭活塞K,用注射器推入浓硫酸至不再产生气泡;
(4)打开活塞K,缓缓鼓入一定量的氮气,关闭活塞K;
(5)再次称量C装置的质量发现比反应前增重6.4g。
由此,计算出该溶液中Na2SO3的质量分数为_____________;
(解释)若没有进行第4步操作,则测得亚硫酸钠溶液的溶质质量分数比实际的____(填”偏小”或”偏大”)。
乙组仍使用第一次实验的原理,进行如下实验测定Na2SO3溶液的溶质质量分数。
第一步:称取试样ag;
第二步:在溶液中加入过量氯化钡溶液和足量稀盐酸;
第三步:过滤、洗涤、烘干沉淀;
第四步:称量沉淀的质量为bg;
第五步:计算溶液中Na2SO3的溶质质量分数=(1-142b/233a)×100%。
试完成下列问题:
(1)加入氯化钡溶液过量的目的是________________;
(2)第三步操作要洗涤沉淀的原因是______________________;
(反思)由此可得出,保存亚硫酸钠时应___________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图是A、B、C 三种物质的溶解度曲线,下列分析正确的是
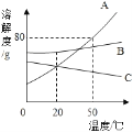
A. 50℃时,把50gA物质放入50g水中能得到100g溶液
B. A中混有少量的B,可用降温结晶法提纯
C. 将C物质的饱和溶液变为不饱和溶液,可采用升高温度或加水的方法
D. 将20℃时A、B、C三种物质的饱和溶液升高到50℃,A溶液中的溶质质量分数最大
-
科目: 来源: 题型:
查看答案和解析>>【题目】金属钯是稀有的贵重金属之一,金属钯制成的首饰不仅有迷人的光彩,而且经得住岁月的磨砺。现有银(Ag)、铂(Pt)、钯(Pd)三种金属制成的戒指,某实验小组利用它们来探究三种金属的活动性。
(1)把钯戒指放入稀硫酸溶液中,戒指完好无损,可推测钯在金属活动性顺序表中位于氢之 (填“前”或“后”)。
(2)如果将钯粉置于盐酸溶液中,边通入氧气边搅拌,钯粉溶解得到二氯化钯(PdCl2)溶液,该反应的化学方程式为 。
(3)如图所示,将银、铂戒指分别放入甲、乙两烧杯中,一段时间后取出,发现只有银戒指表面有明显变化,推测甲烧杯中还可能出现的现象是 。通过该实验判断,银、铂、钯的金属活动性由强到弱顺序为 。

-
科目: 来源: 题型:
查看答案和解析>>【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
(演示实验)将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
(学生板演)该反应的化学方程式 .
(提出问题)实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
(假设猜想)针对疑问,太家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是 .
(实验探究)(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有 .
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,进行如下三个方案的探究.
实验方案
测溶液pH
滴加Na2CO3溶液
滴加BaCl2溶液
实验操作
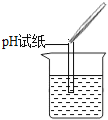
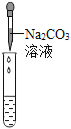
实验现象
试纸变色,对比比色卡,pH<7
有气泡产生
产生白色沉淀
实验结论
溶液中有H2SO4
溶液中有H2SO4
溶液中有H2SO4
(得出结论)通过探究,全班同学一致确定猜想二是正确的.
(评价反思)老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出(实验探究)(2)中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
(1)实验操作中的错误是 .
(2)实验方案中也有一个是错误的,错误的原因是 .
-
科目: 来源: 题型:
查看答案和解析>>【题目】通过一年的化学学习,你已经掌握了一些实验室制取气体的相关规律,以下是老师提供给大家的一些装置,请你回答下列问题:
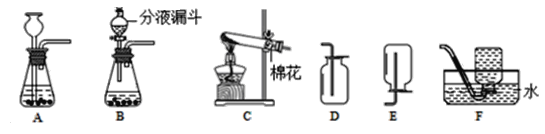
(1)实验室用二氧化锰和过氧化氢溶液制取氧气的化学方程式是________________,若要较好地控制产生氧气的速度,应选用的发生装置是__________(填字母编号)。
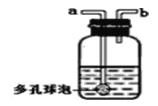
(2)实验室用大理石与稀盐酸制备CO2的化学方程式为_____________, 收集装置最好选择_______(填字母编号)。为了收集干燥的二氧化碳气体,可把气体通过下图的装置中进行干燥再收集。则下图瓶中的溶液是____________(写名称),装置中的多孔球泡的作用是____________。
相关试题

