【题目】我国约在南北朝时就开始冶炼黄铜,黄铜是铜和锌的合金(Cu-Zn),它可用来制造电器零件及日用品。小华利用一瓶稀盐酸和相关的仪器,测定黄铜样品的组成(不考虑黄铜中的其他杂质)。将30mL稀盐酸分三次加入到10g黄铜样品粉末中,每次充分反应后,测定生成氢气的质量,实验数据见下表:
第一次 | 第二次 | 第三次 | |
连续加入盐酸的体积/mL | 10 | 10 | 10 |
生成氢气的质量/g | 0.08 | X | 0.04 |
(1)X=____________;
(2)从上表数据分析,小华用10 g合金粉末总共收集到氢气_______g;
(3)求该合金中铜的质量分数。
参考答案:
【答案】(1)0.08;(2)0.2;(3)35%
【解析】(1)X=0.08;(2)从上表数据分析,小华用10 g合金粉末总共收集到氢气是0.08g+0.08g+0.04g=0.2g;(3)解∶设该合金中锌的质量为xg
Zn→H2
65 2
X 0.2g
![]() =
=![]() ,x=6.5g.
,x=6.5g.
该合金中铜的质量分数∶![]() ×100%=35%.
×100%=35%.
答∶X=0.08;(2)从上表数据分析,小华用10 g合金粉末总共收集到氢气是0.2g;
(3)该合金中铜的质量分数是35%.
点睛∶本题主要考查质量守恒定律的应用以及根据化学方程式进行计算。
-
科目: 来源: 题型:
查看答案和解析>>【题目】亚硝酸钠(NaNO2)外观与食盐很相似,有咸味,误食易中毒。区别它们的一种方法是:隔绝空气加热。没有明显变化的是食盐。能分解放出有刺激性气味气体的是亚硝酸钠。此气体可能是
A.SO2 B.NO2 C.N2 D.NH3
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
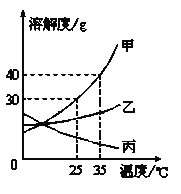
(1)35℃时,这三种物质溶解度由小到大的顺序为______________。
(2)若甲固体中含有少量乙,则提纯甲的方法是_______________。
(3)将25℃时乙的饱和溶液升温到35℃,则其溶液的溶质质量分数___________(填“变大”、“变小”或“不变”)。 25℃时,将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,得到溶液的质量为___________g。
(4)35℃时,分别用等质量的甲、乙、丙配制该温度下的饱和溶液,所得溶液的质量最小的是_________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】在做盐跟盐反应的分组实验时,第一组学生进行BaCl2与Na2CO3溶液的反应,第二组学生进行BaCl2与Na2SO4溶液的反应。实验结束后,两组同学将全部的浊液集中倒进一个废液缸中。浊液中白色沉淀物质是 和 。
化学兴趣小组对浊液进行过滤,探究滤液的成分。
【提出问题】滤液里除了NaCl外,还有什么物质?
【提出猜想】猜想①: ; 猜想②:Na2SO4;
猜想③:Na2CO3; 猜想④:Na2CO3、Na2SO4
【实验探究】

若现象a只有白色沉淀,则猜想 成立;若现象a只有气泡产生,则猜想 可能成立;若现象b产生白色沉淀,然后加稀硝酸沉淀部分溶解,并产生气泡,则猜想 成立,若
沉淀全部不溶解,则猜想 成立。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列实验操作或实验报告中记录的数据正确的是
A. 加热固体物质时试管口应向上倾斜防止固体下滑
B. 用10mL量简量取7.36mLNaOH溶液
C. 用完酒精灯后,必须用灯帽盖灭
D. 用广泛pH试纸测得某溶液pH为5.5
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图为甲乙两物质的溶解度曲线,下列说法正确的是

A.甲的溶解度大于乙的溶解度
B.t1℃时,甲、乙两物质饱和溶液中溶质的质量分数均为15%
C.要使接近饱和的乙溶液转化为饱和溶液,可采用蒸发溶剂的方法
D.t2℃时,将50g甲物质放入100g水中,得到溶液的质量为150g
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学与生产、生活密切相关。下列说法中正确的是
A. 带活性炭口罩防雾覆的原理是利用活性炭的吸附作用
B. 大力推广使用煤的液化、气化技术,能减少二氧化碳的排放
C. 焚烧农田里的秸秆和城市小区路上的落叶可净化环境
D. 胃酸的主要成分是盐酸,胃酸过多的病人可口服少量的氢氧化钠中和
相关试题

