【题目】我国古代将炉甘石(主要成分 ZnCO3)、赤铜(Cu2O)和木炭粉按适当比例混合后加热到约
800℃,得到外观似金子的黄铜(铜和锌的合金)和气体 A。根据流程图回答下列问题:(提示:ZnCO3![]() ZnO+CO2↑)
ZnO+CO2↑)
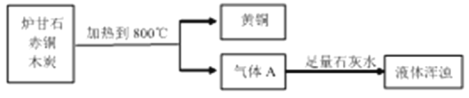
(1)黄铜是铜和锌的合金,生成其中铜的化学方程式为2Cu2O+C![]() 4Cu+CO2↑,请写出生成锌的化学方程式_____;
4Cu+CO2↑,请写出生成锌的化学方程式_____;
(2)黄铜常被称作“假黄金”,区别真假黄金的方法不可行的是___________;
A.看颜色 B.在空气中灼烧 C.放入稀盐酸中 D.放入硝酸锌溶液中
(3)气体 A 中一定含有CO2,还可能含有CO,确定气体 A 中是否含有CO的实验操作 是______。
参考答案:
【答案】2ZnO+C![]() 2Zn+CO2↑ 【答题空2】AD 把气体通过炽热的氧化铜粉末
2Zn+CO2↑ 【答题空2】AD 把气体通过炽热的氧化铜粉末
【解析】
高温条件下,氧化锌和碳反应生成锌和二氧化碳;加热条件下,铜和氧气反应生成氧化铜;
盐酸和锌反应生成氯化锌和氢气;高温条件下,氧化铜和一氧化碳反应生成铜和二氧化碳。
(1)高温条件下,氧化锌和碳反应生成锌和二氧化碳,反应的化学方程式为:2ZnO+C![]() 2Zn+CO2↑;
2Zn+CO2↑;
(2)A、看颜色无法区分黄铜和黄金,这是因为它们的颜色相同;
B、在空气中灼烧时,表面变黑色的是黄铜,无明显现象的是黄金,可以用此法区分黄铜和黄金;
C、放入稀盐酸中时,产生气泡的是黄铜,无明显现象的是黄金,可以用此法区分黄铜和黄金;
D、放入硝酸锌溶液中无法区分黄铜和黄金,这是因为它们都不能和硝酸锌反应;
(3)确定气体A中是否含有CO的实验操作是:把气体通过炽热的氧化铜粉末,如果黑色粉末变红色,说明气体中含有一氧化碳,反之则不含有一氧化碳。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据模拟工业上用一氧化碳还原氧化铁(Fe2O3)炼铁的实验,回答下列问题:
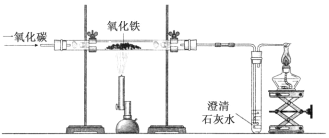
(1)写出一氧化碳还原氧化铁的化学方程式 ____________;
(2)实验过程中,酒精灯的作用是_______;
(3)现有 1000g 含氧化铁 80%的赤铁矿粉,理论上可生成纯铁________________g;
(4)工业炼铁过程中,利用焦炭在高温条件下与二氧化碳反应制取一氧化碳,在这个变化过程 中体现二氧化碳具有 ______性。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据以下课本实验图,回答下列问题:
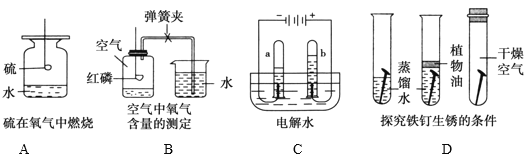
(1)A 实验集气瓶中水的作用是____________________;
(2)B 实验燃烧匙慢慢伸入集气瓶会导致实验结果_______________(选填“偏大”或“偏小”);
(3)C 实验中 a、b 两试管中气体的质量比__________________________;
(4)从 D 实验中可以得到的结论是______________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据所学微观粒子的知识回答下列问题:
(1)将等量的品红分别放入等量的热水和冷水中观察现象,实验目的是探究品红分子运动快慢与_____有关;
(2)在化学变化 X+2O2=CO2+2H2O 中,判断 X 化学式是_____;
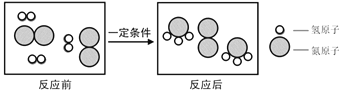
(3)下图是模拟工业制取 NH3 的微观图, 变化过程用化学方程式表示为_____。
-
科目: 来源: 题型:
查看答案和解析>>【题目】“
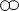 ”和“
”和“ ”代表两种不同的单质分子,它们在一定条件下能发生化学反应,反应前后的微观示意图如下所示,下列说法正确的是 ( )
”代表两种不同的单质分子,它们在一定条件下能发生化学反应,反应前后的微观示意图如下所示,下列说法正确的是 ( )
A. 该反应有2种生成物 B. 每个生成物分子由3个原子构成
C. 该反应是化合反应 D. 参加反应的“
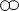 ”和“
”和“ ”分子的个数比是 2︰1
”分子的个数比是 2︰1 -
科目: 来源: 题型:
查看答案和解析>>【题目】通过化学学习我们认识了许多的物质,请回答以下问题
(1)氮气约占空气体积的____________;供给呼吸的气体是__________。
(2)_________、_________和___________是重要的三大化石燃料,大量使用化石燃料会,导致全球变暖。科学家采用高新技术,将二氧化碳和氢气在一定条件下组合,生成一种重要的化工原料乙烯(C2H4)和水,该反应的化学方程式为________________ 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】水是人类生命之源,是宝贵的自然资源。
(1)下列各种水中,属于纯净物的是______ (填字母)。
A.汽水 B. 矿泉水 C.蒸馏水 D. 经过净化处理的自来水
(2)蒸馏水、矿泉水、白醋、酒精都是常见的无色液体,其中白醋具有酸味,酒精具有特殊气味的是酒精,常被称为绿色能源,请写出酒精燃烧的化学方程式 _______________________________ ;在密闭容器中,将少量乙醇置于一定量氧气中燃烧,生成二氧化碳、水蒸气和一种未知物质W。现测得反应前后各物质的质量如下:
物质
乙醇
氧气
二氧化碳
水蒸气
W
反应前质量/g
48
80
0
0
0
反应后质量/g
2
0
44
54
x
根据质量守恒定律,得出表中x的值为_______,另外两种无色液体可用多种方法区分,例如:加入 _____________ ,根据产生泡沫的多少来区分。
相关试题

