【题目】草木灰是植物燃烧后的残余物,草木灰中几乎含有植物体内所有的矿质元素。草木灰的主要成分是碳酸钾,干木柴烧出来的草木灰pH值为12左右且无任何杂质。某化学兴趣小组取来干木柴燃烧后产生的草木灰69g,并向其中加入稀盐酸进行反应。实验过程中的pH图像如图所示,求:
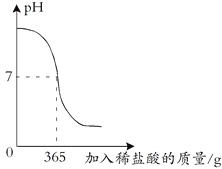
(1)当溶液为中性时,加入稀盐酸的质量为 g。
(2)计算实验所用的稀盐酸的溶质质量分数。
参考答案:
【答案】(1)365;(2)10%
【解析】(1)根据图像得,当溶液为中性时,加入稀盐酸的质量为365g。
(2)设参加反应的HCl的质量为x。
K2CO3 + 2HCl=2KCl + CO2 ↑ + H2O
138 73
69g x
![]()
x=36.5g
实验所用的稀盐酸的质量分数=![]() =10%。
=10%。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质在空气中燃烧现象的叙述错误的是
A.铁丝:火星四射 B.木炭:呈红热状态
C.镁条:耀眼的白光 D.硫粉:淡蓝色火焰
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学知识能帮助我们有效的保障人体健康和人身安全,下列处置不当的是
A.餐桌上酒精着火,立即用湿抹布扑灭
B.油锅着火,立即盖上锅盖
C.用燃着的小木条检查液化石油气是否泄漏
D.身处火灾现场,应用湿毛巾捂住口鼻,保持低姿态逃生
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲烷是最简单的有机物,实验室常用加热无水醋酸钠和碱石灰的固体混合物制取甲烷。在标准状况下,甲烷的密度比空气密度小,难溶于水。某实验小组准备了下列器材进行甲烷的制取和收集实验。

(1)在图A所示的装置中,仪器①的名称是___________。
(2)实验室中制取并收集比较纯净的甲烷可选用下列仪器中的_______和______。(填编号)
(3)请你设计实验,检验生成的气体甲烷中含有氢元素。
实验操作
实验现象
实验结论
______
_____
甲烷中含有氢元素
-
科目: 来源: 题型:
查看答案和解析>>【题目】物质由元素组成,请根据H、C、O、Cl、Ca、Na、Fe七种元素回答下列问题。
(1)某固体可以用于人工降雨,组成该固体的元素为______。
(2)A、B两种物质分别由1种或2种元素组成,进行如下实验。
物质
A
B
滴加的物质
稀盐酸
稀盐酸
现象
生成浅绿色溶液和一种可燃性气体
生成黄色溶液
① A物质的化学式为_______。
② B中滴加稀盐酸,发生反应的化学方程式为______。
(3)如图所示,打开止水夹和胶塞,向放有少量固体C的甲中加入足量D的溶液,塞紧胶塞,观察到甲中有气泡,乙中溶液变浑浊。关闭止水夹,甲中无色液体流入乙中,乙中有气泡产生,浑浊液变为无色溶液。乙中溶液变浑浊反应的化学方程式为______;甲中无色液体流入乙中时所含溶质可能的组成为___。

-
科目: 来源: 题型:
查看答案和解析>>【题目】海水中含有MgCl2和NaCl等多种物质,利用海水提取金属镁的工业流程如图所示:
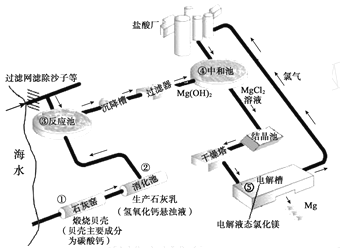
(1)在①~⑤的每个反应装置内都发生了化学反应,发生分解反应的装置有_______(填序号)。
(2)写出装置④内发生反应的化学方程式_______。
(3)MgCl2溶液在进入结晶池之前需先加热浓缩,加热过程中,MgCl2溶液中溶质质量分数会逐渐________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】为了研究反应中压强的变化情况,利用下图进行实验。

(1)检查装置气密性:打开a,关闭b,在A中加入水, ,则装置的气密性良好。用同样原理可以检查装置另一侧的气密性。
(2)在A、B中分别加入澄清石灰水,在集气瓶内放入一定量的大理石,将a、b都打开,用注射器加入足量稀盐酸直至液面浸没下端管口,保持注射器活塞不动。此时,可观察到的现象是 。
(3)关闭b,集气瓶中持续产生气体,A中的现象是 。判断A中是否发生化学反应: (若没有反应,写出理由;若发生反应,写出化学方程式)。
相关试题

