【题目】以下是实验室制取气体的常用仪器,回答下列问题。

(1)标号为a的仪器名称是__________;
(2)用大理石和稀盐酸反应制取CO2,并用排水法收集。
①该反应的化学方程式为__________;
②若要制取两瓶CO2(总质量为4.4g),所用7.3%的盐酸至少__________g;
③组装制取装置时,需选择上图中的a、b、h、i、k、l、m和_________;
④实验室制取下列气体时,可选用制取二氧化碳装置的是_________(填序号)
A 锌粒和稀硫酸制取氢气
B 加热无水醋酸钠与碱石灰固体制取甲烷
C 硫化亚铁与稀硫酸常温反应制取易溶于水的硫化氢气体
(3)实验室用KClO3制取O2:
①若用排水法收集O2,当观察到_________现象时,说明已收集满。
②反应过程中MnO2在固体混合物中质量分数变化情况,正确的是_________(填序号)
A 先逐渐变小,最后不变 B先逐渐变大,最后不变 C 始终不变
【答案】锥形瓶 CaCO3+2HCl=CaCl2+H2O+CO2↑ 100 c C 集气瓶口有大气泡 B
【解析】
(1)标号为a的仪器名称是锥形瓶;
(2)①大理石的主要成分是碳酸钙,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳;故填:CaCO3+2HCl=CaCl2+H2O+CO2↑;
②设:需要7.3%的盐酸的质量至少为x。
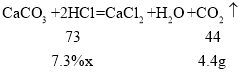
![]() x=100g;
x=100g;
③实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,所以组装制取装置时,需选择上图中的a、b、h、i、k、l、m和c;
④实验室中制取二氧化碳,反应物是固体和液体,不需加热,属于固—液常温型;二氧化碳的密度比空气大,能溶于水,一般采用向上排空气法收集。
A 锌粒和稀硫酸常温反应制取氢气,反应物是固体和液体,不需加热,属于固—液常温型,但氢气的密度比空气小,若用排空气法收集,应采用向下排空气法收集,故A错误;
B加热无水醋酸钠与碱石灰固体制取甲烷反应物是固体,反应条件是加热,属于固体加热型,故B错误;
C硫化亚铁与稀硫酸常温反应制取易溶于水的硫化氢气体,反应物是固体和液体,不需加热,属于固—液常温型;硫化氢的密度比空气大,易溶于水,一般采用向上排空气法收集,故C正确。故选C;
(3)①若用排水法收集O2,当观察到集气瓶口有大气泡向外冒出时,说明已收集满;
②二氧化锰在反应中用作催化剂,在反应前后质量不变,由于氧气的放出,剩余固体的质量不断减小,反应结束后,剩余固体质量不变,反应过程中MnO2在固体混合物中质量分数变化情况,正确的是:先逐渐增大,最后不变。故选B。

