【题目】质量守恒定律的发现,对化学的发展作出了重要贡献。
(1)通过分别称量下列两组试剂在密闭容器内混合前后的总质量,能验证质量守恒定律的是__(填标号)。
a.大理石和稀盐酸 b.NaOH溶液和Na2SO4溶液
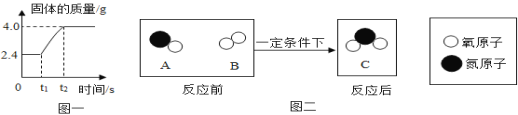
(2)在足量氧气中点燃镁条的实验过程中,固体质量变化如图一。
①从燃烧条件分析,固体质量在t1前没有发生变化的原因是__。
②该反应的化学方程式为__;
③参加反应的氧气质量为__g。
(3)在一定条件下,A和B反应生成C,微观示意图如图二。回答下列问题:
①一个A分子由__个原子构成;
②C分子中元素的质量比N:O=__;
③该反应的化学基本反应类型为__;
④上述反应中一定发生改变的是__(填标号)。
a.元素种类 b.原子种类 c.分子种类
参考答案:
【答案】 a; 温度未达到金属镁的着火点; 2Mg+O2![]() 2MgO; 1.6; 2; 7:16; 化合反应; c
2MgO; 1.6; 2; 7:16; 化合反应; c
【解析】
(1)在验证质量守恒定律时,对于有气体参加或生成的反应,需要在密闭容器内进行,a中大理石和稀盐酸能反应生成氯化钙、水和二氧化碳,可以用来验证,b中氢氧化钠和硫酸钠不会发生化学反应,不能用来验证质量守恒定律;(2)从燃烧条件分析,固体质量在t1前没有发生变化的原因是刚开始温度较低,还没有达到镁条的着火点;发生的反应是镁和氧气在点燃的条件下反应生成氧化镁,反应的化学方程式是2Mg+O2![]() 2MgO;参加反应的氧气的质量,即固体增加的质量,为1.6g;(3)根据微观示意图可知一个A分子由2个原子构成;C分子中元素的质量比N:O=14:32=7:16;该反应是两种物质反应生成一种物质,属于化合反应;上述反应中一定发生改变的是分子的种类,而元素的种类,原子的种类一定不变。
2MgO;参加反应的氧气的质量,即固体增加的质量,为1.6g;(3)根据微观示意图可知一个A分子由2个原子构成;C分子中元素的质量比N:O=14:32=7:16;该反应是两种物质反应生成一种物质,属于化合反应;上述反应中一定发生改变的是分子的种类,而元素的种类,原子的种类一定不变。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化学小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法错误的是( )

A. 该实验是将氢氧化钠溶液滴入稀盐酸中
B. a点所示溶液中,溶质只有NaCl
C. b点表示稀盐酸和氢氧化钠溶液恰好完全反应
D. 向点c所示溶液中滴加紫色石蕊溶液,溶液变蓝色
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验桌上准备了下列仪器和药品。
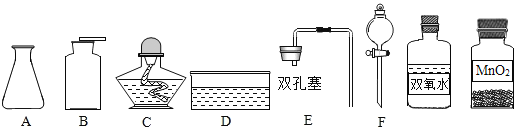
回答下列问题:
(1)标号为C的仪器名称是__。
(2)制取和收集氧气所用的仪器有__(填标号),反应的化学方程式为__。
(3)氧气的验满方法是__。
(4)该气体发生装置,还可以制取其它常见气体。请写出利用该装置制取另一种气体的化学方程式__。
-
科目: 来源: 题型:
查看答案和解析>>【题目】小刚同学在学习化学知识后,知道进入久未开启的菜窖可能造成死亡。于是他和小强一起对自家久未开启的菜窖内的气体成分进行了探究。
(提出问题)菜窖内气体的成分是什么?
(查阅资料)蔬菜在一定条件下发酵生成气体,其成分可能含有CO2、CH4等。
(猜想与假设)小刚认为菜窖内的气体含有CO2和CH4。
(实验探究)他们对菜窖内的气体进行取样按图所示装置进行实验

(1)若装量A中澄清石灰水变浑浊,证明气体样品中含有__;
(2)装置B内发生反应的化学方程式为__;
(3)装置D内浓硫酸的作用是__;
(4)E处观察到干燥冷烧杯内壁有__出现,待火焰熄灭后,把烧杯迅速倒转过来,立刻向烧杯内倒入少量澄清石灰水并振荡,石灰水变浑浊,证明气体样品中含有__。E处气体燃烧的化学方程式为__。
(实验结论)气体样品中含有CO2和CH4,小刚的猜想正确。
(反思与评价)
(5)小强观察上述实验装置发现:装置A和装置C完全相同,他认为可以取消装置C.你是否认同__(填“认同”或“不认同”)理由是__。
(6)根据上述实验探究结果,气体样品中含有CO2,由于二氧化碳__,所以进入久未开启的菜窖前,应向菜窖内通入大量的空气。
-
科目: 来源: 题型:
查看答案和解析>>【题目】阅读科普短文
稀土材料
稀土元素是指元素周期表中ⅢB族的钪(Se)、钇(Y)以及铜系元素。这些元素的氧化物都不溶于水,外形像泥土,而且又稀少,因而人们喜欢称它们为”稀土元素”。稀土元素的化学性质较为活泼,若与其他元素结合,便可组成种类繁多、功能多样、用途广泛的新型材料,且性能会有较大提高,被称作当代的“工业味精”稀土元素的镧(La)、铈(Ce)、镨(Pr)、钕(Nd)。在元素周期表中的位置如图所示。
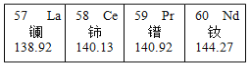
稀土元素的化合物还是生产特种玻璃和陶瓷的重要原料。如将三氧化二铈(Ce2O3)加入玻璃中,可制成低散射、高折射的光学玻璃,用于生产精密的光学器材。
根据短文内容,回答下列问题:
(1)从材料中可得出,稀土元素的化学性质__。
(2)铈元素的质子数是__。
(3)三氧化二铈(Ce2O3)中Ce元素的化合价是__价。
(4)三氧化二铈(Ce2O3)的用途是__。
-
科目: 来源: 题型:
查看答案和解析>>【题目】废旧电池可回收再利用,避免对环境造成污染。如图是普通干电池的结构示意图。回答下列问题:
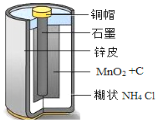
(1)回收大量铜帽,经过净化处理,可制成导线。说明铜具有__性。
(2)回收的锌皮,经过净化处理,与稀硫酸反应,可制得高能洁净燃料氢气,点燃氢气前一定要__。将足量的锌与490g 20%的稀硫酸反应,理论上可制得氢气__g。
(3)氯化铵是一种铵态氮肥,在施用时不能与__(填”酸性”或“碱性”)肥料混合施用,否则会使肥效丧失。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图是a、b、c三种物质的溶解度曲线,下列说法错误的是( )

A. t2℃时,溶溶解度:a=b>c
B. 随温度的升高,c物质的溶解度减小
C. t3℃℃时,将30克a加入50克水中可以得到80克溶液
D. t1℃时,a的饱和溶液和c的饱和溶液的溶质质量分数相等
相关试题

