【题目】水变成水蒸气的过程中,发生变化的是( )
A.分子质量 B.分子种类 C.分子间隔 D.分子大小
参考答案:
【答案】C
【解析】水变成水蒸气是物理变化,由液态变为气态,变化的过程中,发生变化的是C.分子间隔。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下列反应事实写出相应的化学方程式。
(1)双氧水在二氧化锰的催化作用下生成水和氧气:_______________。
(2)在尘埃的作用下,二氧化硫和氧气反应生成三氧化硫(SO3):_______________。
(3)Cu和AgNO3溶液反应,生成Cu(NO3)2溶液和Ag:_______________。
(4)少量CuSO4溶液滴人NaOH稀溶液中生成Cu(OH)2沉淀和Na2SO4溶液:_______________。
(5)一氧化碳和四氧化三铁(Fe3O4)杠高温下反应,生成铁和二氧化碳:_______________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验窒常会产生含硫酸的废水,需经处理至中性。某兴趣小组同学配制一定质量分数的氢氧化钾溶液来处理酸性废水。
(1)定性检测废水
检测废水呈酸性的方法是_____________。
(2)配制200 g质量分数为5.6%的氢氧化钾溶液
①计算
m (KOH)=_______g,V(H2O)=________mL(水的密度近似为1.0 g·mL-1)。
②称取氢氧化钾
调节托盘天平平衡后,将一只烧杯放在托盘天平的左盘,称量其质量。然后______(按操作先后顺序,填字母),直至天平平衡。
A.向烧杯中加氢氧化钾同体 B.按需要添加砝码、移动游码
③量取水;④溶解;⑤转移。
(3)定量测定废水
取酸性废水样品100 g,逐滴加入5.6%的氢氧化钾溶液,废水中硫酸的质量分数变化如右下图所示。(假设废水中其他成分不与氢氧化钾反应且不含硫酸钾)
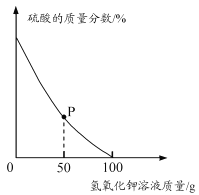
①P点对应溶液中一定存在的阳离子有_______(填离子符号)。
②酸性废水中硫酸的质量分数为______(用百分数表示,保留到0.1%)。
③计算当废水处理至中性时,溶液中硫酸钾的质量分数(写出计算过程,结果用百分数表示,保留到0.l%)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】“细菌冶金”的原理是利用氧化铁硫杆菌促使 黄铁矿(主要成分FeS2)氧化成硫酸铁和硫酸,并能为CO2和H2O合成有机物提供能量.流程如图,下列说法错误的是( )
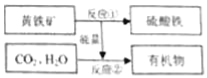
A.反应①化学方程式:4FeS2+15O2+2X=2Fe2(SO4)3+2H2SO4,X为H2O2
B.整个流程提高了能量的利用率
C.图中有机物一定不含氧元素
D.氧化铁硫杆菌在反应①中起催化作用
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )
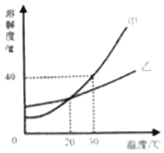
A.30℃时,甲的饱和溶液溶质质量分数为40%
B.20℃时,甲、乙的饱和溶液中所含溶质的质量一定相等
C.将等质量的甲、乙固体,分别配成30℃的饱和溶液,所需水的质量:甲>乙
D.将20℃时甲、乙的饱和溶液升温到30℃,所得甲、乙溶液的溶质质量分数相等
-
科目: 来源: 题型:
查看答案和解析>>【题目】 在20℃时,往100克饱和食盐溶液中,加入5克食盐,保持不变的是
A.溶质质量 B.溶剂质量 C.溶液质量 D. 以上皆是
-
科目: 来源: 题型:
查看答案和解析>>【题目】A~H为初中化学常见物质.其中A、E为氧化物且E为常见的液体,B、D为碱,H、G为单质,C为石灰石的主要成分,F为胃酸的主要成分;反应①为光合作用.它们之间的相互关系如图所示.其中“→”表示转化关系,“﹣”表示相互之间能发生反应(部分反应物、生成物以及反应条件省略).
请回答下列问题:
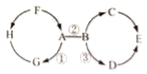
(1)C的化学式为 ;E的化学式为 .
(2)B物质的一种用途为 ;反应③的基本反应类型为 .
(3)写出下列反应的化学方程式:① ;② ;③ .
相关试题

