【题目】人类的生产和生活都离不开金属。
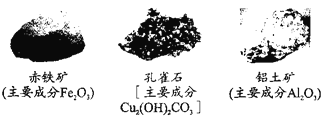
(1)金属元素在自然界中分布很广,地壳中含量最多的金属元素是_______。金属以矿物形式存在,下列矿石的主要成分属于氧化物的是_______(填化学式)。
(2)铁是应用最广泛的金属。
①工业上常用赤铁矿和一氧化碳在高温条件下炼铁,该反应的化学方程式为________。
②使用过的菜刀、铁锅等铁制品,清洗后需及时擦干放置,可以减少_______对铁锈蚀的影响。
(3)将一定量的锌加入稀硫酸、硫酸亚铁和硫酸铜的混合溶液中,充分反应后过滤,向滤渣中加入稀盐酸,有气泡产生。滤渣和滤液中一定含有的物质是_______。
参考答案:
【答案】 铝(Al) Fe2O3和Al2O3 Fe2O3+3CO![]() 2Fe+3CO2 水 铁、铜、硫酸锌
2Fe+3CO2 水 铁、铜、硫酸锌
【解析】(1)金属元素在自然界中分布很广,地壳中含量最多的金属元素是铝(Al)。氧化物是由两种元素组成,其中一种是氧元素的化合物,题中矿石的主要成分属于氧化物的是Fe2O3和Al2O3;
(2)①赤铁矿和一氧化碳在高温条件下生成铁和二氧化碳。其化学方程式为:Fe2O3+3CO![]() 2Fe+3CO2;
2Fe+3CO2;
②铁生锈是铁与水和氧气的共同作用的结果,隔绝氧气或水能防止铁生锈,清洗后需及时擦干放置,可以减少水对铁锈蚀的影响;
(3)稀硫酸、硫酸亚铁和硫酸铜的混合溶液中加入一些锌粉,充分反应,则所得滤渣中一定含有被置换出来的铜;向滤渣中加入盐酸,有气泡产生,则滤渣中一定含有铁;如果锌过量则滤渣中还含有锌;锌是否过量不能确定,滤液中是否还含硫酸亚铁也不能确定,但可以确定的是滤液中一定不含硫酸铜,锌与硫酸铜、硫酸亚铁反应时生成硫酸锌一定存在,所以滤液中一定含有硫酸锌。
-
科目: 来源: 题型:
查看答案和解析>>【题目】为了探究影响铁与盐酸反应剧烈程度的因素,某学习小组设计了下列实验:

下列说法正确的是
A.对比实验①和②,可研究盐酸的浓度对反应剧烈程度的影响
B.对比实验②和③,可研究盐酸的浓度对反应剧烈程度的影响
C.对比实验②和③,可研究温度对反应剧烈程度的影响
D.对比实验①和②,可研究温度对反应剧烈程度的影响
-
科目: 来源: 题型:
查看答案和解析>>【题目】请回忆你观察过的“用木炭还原氧化铜”的演示实验,并根据图,回答问题:

(1)写出用木炭还原氧化铜的化学方程式:______________;
(2)反应进行一段时间后,为了进一步探究试管中剩余固体的组成,待试管冷却至室温后,取剩余固体于烧杯中,再加入过量稀硫酸,充分搅拌后过滤。
①若滤纸上留有黑色、红色固体,而滤液为无色,则滤液中的溶质是_______,试管中的剩余固体为_______;
②若滤纸上留有黑色、红色固体,而滤液呈蓝色,此时滤液中的溶质是_______。
-
科目: 来源: 题型:
查看答案和解析>>【题目】金属钛因为有神奇的性能越来越引起人们的关注。常温下钛不与非金属及强酸反应,加热时却可以和常见的非金属单质反应。钛是航空、军工、电力等工业领域的重要原材料。地壳中的钛矿石之一是金红石(主要成分是TiO2),目前大规模生产钛的方法是:
(1)使金红石与炭粉混合,在高温条件下反应,再通入氯气,制得TiCl4和一种可燃性气体。该反应的化学方程式是_____________________。
(2)在氩气的气流中,高温下用过量的镁和TiCl4反应可制得金属钛。写出该反应的化学方程式:___________________________________。
(3)从上述反应的混合物中分离出金属钛。写出简单的分离步骤和有关的化学方程式。_____________________________
-
科目: 来源: 题型:
查看答案和解析>>【题目】下表提供了在一定条件下,水与一些金属发生反应的信息。
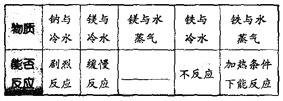
(1)请根据表中已有的知识,将表格填写完整。___________________
(2)已知铁与水蒸气在加热条件下反应生成四氧化三铁和氢气,该反应的化学方程式为_______。
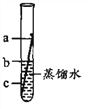
(3)铁虽然常温下不与水反应,但铁制品在潮湿环境中易生锈。某同学进行了如图所示的实验。一周以后发现铁钉表面生锈。图中a、b、e三处锈蚀情况最严重的是_______(填字母),产生该现象的原因是____________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】李红在查阅资料时发现木炭也能夺取含氧化合物中的氧,表现出还原性。如:CO2+C
 2CO,于是她对过量木炭和氧化铁在高温条件下反应,最终产生的气体是什么产生兴趣,决定进行探究。请回答下列有关问题(提示:铁、氧化铁均能与稀盐酸发生化学反应)。
2CO,于是她对过量木炭和氧化铁在高温条件下反应,最终产生的气体是什么产生兴趣,决定进行探究。请回答下列有关问题(提示:铁、氧化铁均能与稀盐酸发生化学反应)。【提出问题】过量木炭和氧化铁反应产生的气体是什么呢?
【猜想和假设】猜想①:可能是CO2;猜想②:可能是CO;猜想③:_______。
【实验方案与现象】将产生的气体通入澄清石灰水,澄清石灰水变浑浊。
【结论】猜想①正确。
【反思与评价】小雨不同意李红的观点,理由是_______________________________。
于是小雨进行如下的实验以验证猜想:
①称取3.2 g的氧化铁与2g木炭均匀混合,放进18.48 g的试管中,加热。
②完全反应后,冷却至室温,称得试管和固体的总质量为22.24 g。
③往试管中加入足量稀盐酸,然后过滤、洗涤、烘干、称量,得到1.52 g黑色粉末。
【数据处理】参加反应的碳元素的质量为_______,氧元素的质量为_______。
【得到结论】根据数据处理结果,得到原猜想③成立,理由是______________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】小明和小英要验证一块石头是否含碳酸钙。
(1)小明说:“只要取一小块石头放在烧杯中,再在石块上倒入盐酸,发现有大量气泡产生,就能证明石块含有碳酸钙。”小英说:“在石块上倒盐酸,产生的大量气泡是盐酸挥发而成的。”小英的说法对吗?_______(填“对”或“不对”)。
(2)小明和小英带着问题请教王老师,在王老师的指导下,进行了下列实验探究,其实验过程如下:①取一小块石块置于烧杯中,滴加盐酸后,发现产生了无色无味气体;②在老师的指导下,取①中的溶液检验,石块中含有钙元素;③他们又设计了如图所示的实验装置,在实验中观察到广口瓶中有浑浊现象产生。
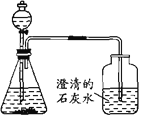
在上述实验中,他们进行的是_______实验研究(填“定性”或“定量”)。
(3)假若称取10.0 g石块与足量的稀盐酸反应(杂质不与盐酸反应),并用饱和石灰水吸收,得到的沉淀经适当处理后得干燥固体7.5 g。计算:
①石块中含碳酸钙的质量分数_______________;
②已知CO2在标准状况下的密度为1.98 g/L,则生成标准状况下CO2气体的体积为______________毫升?
相关试题

