【题目】十八世纪,拉瓦锡用放大镜聚集日光使玻璃罩内的金刚石燃烧,得到二氧化碳。坦南特进一步研究确认金刚石仅由碳元素组成。下列说法错误的是
A.金刚石属于有机物 B.金刚石燃烧过程放出热量
C.金刚石具有可燃性 D.聚集日光使温度达到金刚石的着火点
参考答案:
【答案】A
【解析】A、有机物是含有碳元素的化合物,金刚石是由碳元素组成的单质,不属有机物,错误;B、燃烧放出热量,正确;C、金刚石是由碳元素组成的,具有可燃性,正确;D、燃烧需要同时满足三个条件:一是要有可燃物,二是可燃物要与氧气接触,三是温度要达到可燃物的着火点。由资料可知用放大镜聚集日光使玻璃罩内的金刚石燃烧,聚集日光使温度达到金刚石的着火点,正确。故选A。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列有关实验现象的描述正确的是( )
A.磷在空气中燃烧产生浓厚的白雾
B.硫在空气中燃烧产生蓝紫色火焰
C.蘸有酚酞溶液的棉签放在盛有浓氨水的试管口,一会儿可观察到棉签变红
D.铝丝放入氯化铜溶液,一段时间后,铝丝表面有银白色固体出现
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列关于物质用途的描述不正确的是
A.氧气可用作燃料 B.二氧化碳可用作气体肥料
C.干冰可用于人工降雨 D.铜丝可用作导线
-
科目: 来源: 题型:
查看答案和解析>>【题目】用如图所示装置,在常温下,分别进行研究空气中氧气含量和研究燃烧条件的实验。
已知:白磷的着火点为 40℃。
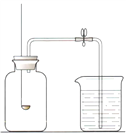
内容
【实验 1】测定空气中氧气含量
【实验 2】研究燃烧条件
实验步骤
燃烧匙中放足量白磷,烧杯中盛放足量水,用激光手电照射白磷,白磷燃烧起来。待白磷熄灭冷却至室温后,打开弹簧夹,观察到
________。
向广口瓶中加入少量二氧化锰,烧杯中盛有 80℃的热水,
在烧杯中导管口放置一小块白磷,塞紧瓶塞用注射器向瓶中注入适量H2 O2 溶液
(1)实验前检查装置气密性:打开弹簧夹,向烧杯中加水至液面浸没下端导管口,用手捂住广口瓶瓶外壁,说明装置的气密性良好的现象是________。
(2)补全实验1中的实验现象________。
(3)实验2中,推入 H2O2 溶液后,瓶内发生反应的化学方程式为________,实验过程中,能说明可燃物燃烧需要氧气的实验现象是________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】铜片在潮湿的空气中久置,表面会产生绿色的铜锈。某小组同学设计并进行实验,探究铜生锈的条件。
【查阅资料】常温下,亚硫酸钠(Na2SO3)可与O2发生化合反应。
【猜想与假设】常温下,铜生锈可能与O2、CO2、水蒸气有关。
【进行实验】通过控制与铜片接触的物质,利用下图装置(铜片长度为3 cm,试管容积为20 mL)分别进行下列5个实验,并持续观察30天。
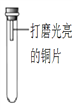
编号
主要实验操作
实验现象
1
先充满用NaOH浓溶液洗涤过的空气
再加入2 mL浓硫酸
铜片始终无明显变化
2
先加入4 mL饱和Na2SO3溶液
再充满CO2
铜片始终无明显变化
3
加入2 mL NaOH浓溶液
铜片始终无明显变化
4
先加入2 mL浓硫酸
再通入约4 mL CO2
铜片始终无明显变化
5
先加入2 mL蒸馏水
再通入约4 mL CO2
铜片表面变成绿色
【解释与结论】
(1)实验中,NaOH浓溶液的作用是___________(用化学方程式表示)。
(2)实验1的目的是________。
(3)实验2中,试管内的气体主要含有CO2、________。
(4)得出“铜生锈一定与H2O有关”的结论,依据的两个实验是________(填编号)。
(5)由上述实验可推知,铜片生锈的条件是_________________。
【反思与评价】
(6)在猜想与假设时,同学们认为铜生锈与N2无关,其理由是________。
(7)兴趣小组的同学认为不需进行上述实验,他们向铜锈中加入稀盐酸并把生成的气体通入___。
-
科目: 来源: 题型:
查看答案和解析>>【题目】空气的成分中,约占总体积21%的气体是( )
A.氮气 B.氧气 C.稀有气体 D.二氧化碳
-
科目: 来源: 题型:
查看答案和解析>>【题目】请回答下列与水有关的问题。
(1)保持水的化学性质的最小粒子是 ;
(2)除去水中不溶性杂质的操作是 ,生活中鉴别硬水和软水常加入 ;
(3)消防队用水灭火的主要原理是 ;
(4)做细铁丝在氧气中燃烧实验时,瓶底留少量水的目的是 。
相关试题

