【题目】某化学兴趣小组同学欲测定某铁粉与碳粉混合物中铁的质量分数,他们进行了如图所示的实验。请计算:
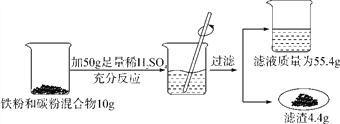
(1)反应后烧杯中稀硫酸无剩余,请计算所用稀硫酸溶液中溶质的质量分数;
(2)欲用98%的浓硫酸配制该浓度的稀硫酸200g,需要水多少克?
参考答案:
【答案】(1)生成氢气的质量为50g+10g-55.4g-4.4g=0.2g,设稀硫酸中溶质的质量为x。
Fe+H2SO4===FeSO4+H2↑
98 2
x 0.2g
![]() =
=![]() x=9.8g
x=9.8g
所用稀硫酸溶液中溶质的质量分数为![]() ×100%=19.6%
×100%=19.6%
(2)欲用98%的浓硫酸配制该浓度的稀硫酸200g,设需要水的质量为y。
(200g-y)×98%=200g×19.6%
y=160g
答:(1)所用稀硫酸溶液中溶质的质量分数为19.6%;(2)欲用98%的浓硫酸配制该浓度的稀硫酸200g,需要水160克。
【解析】铁粉与碳粉混合物中加入足量的稀硫酸,铁能与稀硫酸反应,碳不能与稀硫酸反应,根据质量守恒定律减少的质量是生成的氢气的质量,根据氢气的质量可求出硫酸中溶质的质量,再根据溶质的质量分数的计算公式进行有关的计算。
解:(1)生成氢气的质量为50g+10g-55.4g-4.4g=0.2g,设稀硫酸中溶质的质量为x。
Fe+H2SO4===FeSO4+H2↑
98 2
x 0.2g
![]() x=9.8g
x=9.8g
所用稀硫酸溶液中溶质的质量分数为![]() ×100%=19.6%
×100%=19.6%
(2)欲用98%的浓硫酸配制该浓度的稀硫酸200g,设需要水的质量为y。
(200g-y)×98%=200g×19.6%
y=160g
答:(1)所用稀硫酸溶液中溶质的质量分数为19.6%;(2)欲用98%的浓硫酸配制该浓度的稀硫酸200g,需要水160克。
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室配制50g溶质质量分数为5%的氯化钠溶液。
(1)已知:水的密度为1.0g/mL,需要称取氯化钠____________g,需要量取水____________mL。
(2)配制的操作示意图如下,该实验的正确操作顺序为__________________(填字母);玻璃棒在本实验过程中的作用是________________________________。

(3)经检测,所配制溶液的溶质质量分数偏小,其原因可能是________(填序号)。
①氯化钠固体不纯
②称量时,砝码盘忘垫质量相同的纸片
③量取水时,仰视读数
④装瓶时,有少量溶液洒出
(4)将上述配置的溶液稀释成2.5%的氯化钠溶液,则需加水________g。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列关于物质燃烧的现象的描述正确的是_______
A.木炭在氧气中燃烧,有黑烟生成
B.细铁丝在氧气中燃烧,火星四射,生成四氧化三铁
C.红磷在空气中燃烧,产生大量白烟
D.硫在氧气中燃烧,_______
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列常见仪器的使用正确的是_______
A.量筒用作反应容器 B.烧杯放在石棉网上加热
C.用温度计搅拌溶液 D.熄灭酒精灯,应该_______
-
科目: 来源: 题型:
查看答案和解析>>【题目】有关酒精的描述有:①无色液体②具有特殊气味③酒精挥发④易燃烧⑤酒精燃烧生成水和二氧化碳。根据上述文字归纳出酒精的性质和变化(填序号):
(1)物理性质______(2)化学性质_____
(3)物理变化______(4)化学变化_____
-
科目: 来源: 题型:
查看答案和解析>>【题目】某同学设计了如图所示的探究Ca(OH)2溶解度随温度变化的实验。

(1)向U形管中注入新配制的饱和澄清石灰水,用酒精灯对U形管的右侧加热,左管无明显变化,而右管中明显出现__________,这种现象称之为________(选填“结晶”或“蒸馏”),此时右管中溶液的溶质质量分数________(选填“增大”“减小”或“不变”);停止加热冷却至常温,能观察到右管中的____________消失,通过对比有效地证实了Ca(OH)2的溶解度随温度的________________的事实;
(2)上述U形管若敞口长期放置,澄清的石灰水表面会出现一层白膜,试写出有关反应的化学方程式:____________________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某温度下,在100g质量分数为20%的KNO3不饱和溶液甲中加入10gKNO3固体,恰好得到饱和溶液乙。下列说法正确的是( )
A. 该温度下,KNO3的溶解度为30g
B. 乙溶液的质量分数为30%
C. 降低温度,可以使甲溶液变成饱和溶液
D. 升高温度,甲、乙两溶液的质量分数都增大
相关试题

