【题目】地壳中含量最多的元素与含量最多的金属元素组成的物质的化学式为 ,两种元素的质量比为 。
参考答案:
【答案】9:8
【解析】
试题分析:地壳中含量最多的元素是氧元素,地壳中含量最多的金属元素是铝元素,氧、铝两种元素组成物质的化学式为:Al2O3 ,Al2O3中两种元素的质量比是27×2:16×3=9:8
-
科目: 来源: 题型:
查看答案和解析>>【题目】科学家最新发现,通过简单的化学反应,可以将树木纤维素转变为超级储能装置,如图是该反应的微观示意图,下列说法错误的是( )

A.参加反应的X,Y两物质的粒子个数之比为3:4
B.该反应不属于置换反应
C.W物质中碳元素的质量分数为75%
D.化学反应前后原子的种类、个数、质量均保持不变
-
科目: 来源: 题型:
查看答案和解析>>【题目】某同学设计了以下四个实验方案,理论上正确,操作上可行,经济上合理的是( )
A.Cu
 CuCl2
CuCl2 Cu(OH)2
Cu(OH)2B.H2O
 O2
O2 MgO
MgOC.CaCO3
 CaO
CaO Ca(OH)2
Ca(OH)2 NaOH溶液
NaOH溶液D.MgCl2
 Mg(OH)2
Mg(OH)2 Mg
Mg -
科目: 来源: 题型:
查看答案和解析>>【题目】(1)某同学对磁湖的水样进行了相关的研 究。
①磁湖水属于__________(填“纯净物”或“混合物”);
②可以采用_________来测定湖水的酸碱度(填字母);
A.酚酞试液 B.石蕊试液 C.pH试纸
③为了检验湖水是软水还是硬水,可向水样中加入___________,搅拌;
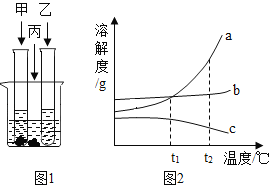
(2)在室温下,甲、乙、丙三种固体分别溶于两支试管和一个烧杯的水中,现象如图1所示,甲、丙还有剩余固体,乙固体全部溶解.升温到80℃时,发现甲固体全部溶解,乙固体析出,丙固体没有明显变化
①室温时, (选填“甲”、“乙”或“丙”)溶液可能是不饱和溶液.
②图2中能表示乙物质的溶解度曲线的是 (填“a”、“b”或“c”,下同),
③t2℃时,甲、乙、丙三种物质的等质量的饱和溶液中水的质量由大到小的顺序是
-
科目: 来源: 题型:
查看答案和解析>>【题目】能反映相关实验过程中量的变化的图象是( )

A. 用一氧化碳还原氧化铁
B. 等质量镁、锌分别和足量等质量分数的盐酸反应
C. 镁在氧气中燃烧
D. 等质量、等质量分数的双氧水完全分解
-
科目: 来源: 题型:
查看答案和解析>>【题目】初中化学中,我们学习了酸和碱发生中和反应的实质是H++OH﹣═H2O。如图,像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式。

离子方程式的书写一般按以下步骤:(以Na2SO4与BaCl2反应为例)
①写出Na2SO4与BaCl2反应的化学方程式: 。
②把易溶于水、易电解的物质写成离子形式,把难溶的物质、气体和水等仍用化学式表示。上述方程式可改写成:2Na++SO42﹣+Ba2++2Cl﹣═BaSO4↓+2Na++2Cl﹣。
③删去方程式两边不参加反应的离子:Ba2++SO42﹣═BaSO4↓。
④检查方程式两边各元素的原子个数和电荷总数是否相等。
请回答:
(1)下列各组中的离子,在pH=3的水溶液中能大量共存的是 。
A.Na+、Mg2+、Cl﹣、SO4 2﹣
B.Na+、K+、Cl﹣、OH﹣
C.Na+、Cu2+、Cl﹣、SO42﹣
D.Na+、K+、Cl﹣、CO32﹣
(2)写出稀盐酸滴在石灰石上所发生反应的离子方程式 。
(3)写出一个与离子方程式Mg+2H+═Mg2++H2↑相对应的化学方程式 。
(4)酸、碱、盐在水溶液中发生的复分解反应实质上就是两种化合物在溶液中相互交换离子的反应,只要具备生成物中有气体或沉淀或 生成,反应就能发生。
-
科目: 来源: 题型:
查看答案和解析>>【题目】我市某著名的纸面石膏板企业,用热电厂燃烧煤产生的炉渣来生产石膏板。原理是:发电过程中产生的烟气中含有大量的SO2,热电厂用“碱﹣石灰﹣石膏CaSO42H2O)”的方法使烟气脱硫从而生成石膏。
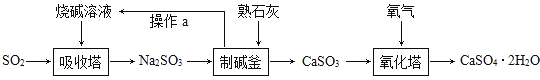
(1)工业烟气没经处理直接排放到空气中易形成______,会污染、破坏环境;
(2)写出吸收塔内发生反应的化学方程式_______,工业上用分离液态空气法制氧气:是利用空气中各成分的___不同进行分离的;
(3)化学反应类型有不同的分法,其中反应前后,有元素化合价变化的化学反应是氧化还原反应。有元素化合价升高的反应物是还原剂,有元素化合价降低的反应物是氧化剂。化学反应前后元素化合价没有变化的化学反应是非氧化还原反应。则下列说法正确的是_____
A.吸收塔、制碱釜中发生的反应属于氧化还原反应
B.制碱釜中的反应物Na2SO3作氧化剂
C.氧化塔中发生的反应属于氧化还原反应
D.氧化塔中的反应物CaSO3作还原剂
(4)生产流程中生成的______可循环利用,节约成本。
相关试题

